 1
1
钨酸钠作为一种重要的钨化合物,其在水中的溶解度特性对它的制备、分离和应用具有重要影响。深入研究钨酸钠的溶解度行为,对于优化其生产工艺和拓展其应用领域具有重要意义。
简介:
钨酸钠是一种无机物,化学式为Na2WO4。钨酸钠呈无色或白色斜方晶体,通常呈现光泽的片状晶体或粉末。它可溶于水,形成微碱性的水溶液,但不溶于乙醇,仅微溶于氨水。钨酸钠在空气中会风化,加热至100℃时会失去结晶水转变为无水钨酸钠。在强酸(氢氟酸除外)中,钨酸钠会生成不溶于水的黄色钨酸。它还会与磷酸或磷酸盐反应生成磷钨杂多酸络合物,与酒石酸、柠檬酸、草酸等有机酸反应则形成相应的有机酸络合物。
1. 钨酸钠可溶吗?
钨酸钠的溶解度为:
(1)水中溶解度
57.5 g/100 mL (0 ℃)
74.2 g/100 mL (25 ℃)
96.9 g/100 mL (100 ℃)
(2)其他溶剂中的溶解度
微溶于氨
不溶于醇、酸
2. 钨酸钠的溶解度研究
2.1 报道一
测量了钨酸钠 (Na2WO4) 在熔融氢氧化钠 (NaOH) 浴中的溶解度及其对水蒸气分压的依赖性。这是一项正在进行的研究的一部分,该研究使用熔融 NaOH 进行新的钨 (W) 回收工艺。首先,通过在浴中添加过量的氧化钨作为钨酸根离子源来确认熔融 NaOH 浴中平衡固相中化合物的性质。X 射线衍射分析表明,无水 Na2WO4 是与饱和 Na2WO4 的熔融 NaOH 的液相平衡的固相。然后,在不同水蒸气分压下测量了无水 Na2WO4 的溶解度。结果表明,无水 Na2WO4 的溶解度随水蒸气分压和浴温的升高而急剧增加,摩尔分数从 0.06 增加到 0.17。该值远高于之前报道的熔融硝酸盐和亚硝酸盐的值。
该实验研究了 Na2WO4 在 NaOH 熔体中的溶解度,实验结果总结如下:
(1)确认在 723 K 下与Na2WO4–NaOH–H2O 体系达到平衡的固相化合物为无水 Na2WO4。
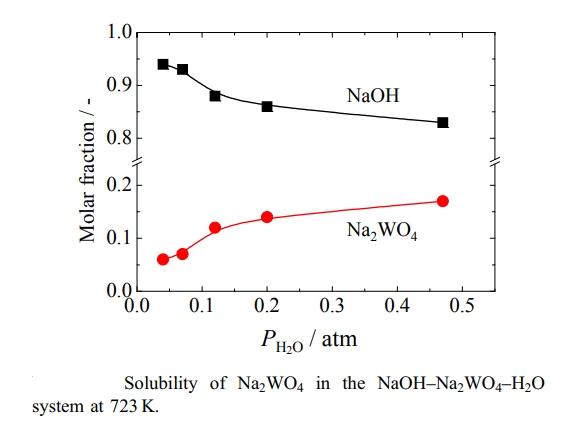
(2)Na2WO4 的溶解度随水蒸气分压和浴温的升高而增加。
(3)获得的溶解度范围为 1.5 至 5.2 mol-Na2WO4/kg-熔体,远高于报道的亚硝酸盐和硝酸盐熔体的溶解度。
2.2 报道二
Pengge Ning等人测定了Na2MoO4·2H2O和Na2WO4·2H2O在Na2MoO4–Na2WO4–Na2SO4–H2O中的溶解度。研究采用动态法测定了二水钨酸钠在(0.1–1.0)mol·kg?1硫酸钠溶液中(温度范围为(293.15至343.15)K)的溶解度。结果表明,二水钨酸钠的溶解度随温度的升高而增大,随硫酸钠浓度的增加而减小。二水钨酸钠的溶解是吸热过程,考虑到硫酸钠的作用,Na+的同离子效应更为显著。
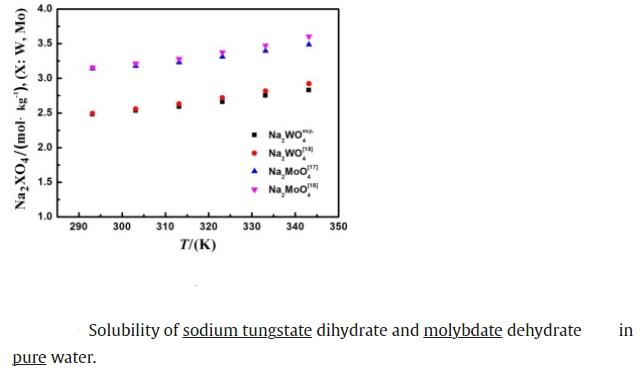
3. 影响钨酸钠溶解度的因素
(1)温度和溶解度
钨酸钠的溶解度受温度的显著影响。通常,随着溶剂温度的升高,钨酸钠在水中的溶解度也会升高。这种趋势是由于许多盐(包括钨酸钠)的溶解过程具有吸热性质。当温度升高时,额外的热能有助于克服固体的晶格能,并促进盐溶解为其组成离子。对于钨酸钠而言,这意味着在较温暖的条件下,更多的盐可以溶解在水中,从而导致溶液中的浓度更高。
(2)pH 和溶解度
溶液的 pH 值也会影响钨酸钠的溶解度。虽然钨酸钠通常被认为在很宽的 pH 范围内溶于水,但极端的 pH 条件可能会影响其溶解度。例如,非常酸性或碱性的环境可能会导致形成不溶性钨酸盐化合物。保持 pH 值在合适的范围内很重要,以确保钨酸钠完全溶解并防止不必要的沉淀。
(3)溶剂和条件
溶剂的选择和测试溶解度的具体条件也起着关键作用。钨酸钠最常溶于水,其溶解度受温度和 pH 值的影响,如前所述。然而,由于极性和溶剂-溶质相互作用的差异,其他溶剂(如醇或有机溶剂)可能无法有效溶解钨酸钠。此外,溶液的离子强度、竞争离子的存在,甚至搅拌速率等因素都会影响溶解过程。了解这些变量对于优化钨酸钠在各种工业和实验室应用中的溶解度至关重要。
4. 如何溶解钨酸钠?
钨酸钠最容易溶解在水中。使用去离子水或纯净水作为溶剂是最常见的做法。钨酸钠在水中的溶解度较高,特别是在温暖的水中。如果需要更高的溶解度,可以考虑使用温热水。溶解钨酸钠时,搅拌可以加速溶解过程。用搅拌棒或磁力搅拌器持续搅拌溶液,有助于钨酸钠均匀溶解。对于大批量的钨酸钠,搅拌时间可能需要延长。
如果溶液中存在其他高浓度的离子,可能会影响钨酸钠的溶解度。保持溶液中的其他离子浓度在适当范围内,以避免对溶解过程产生负面影响。
5. 钨酸钠溶解度的工业应用
钨和钼是稀有的难熔金属。它们既耐高温,又具有优良的导电性,因此成为重要的国家战略资源。这两种金属的回收和纯化通常在湿法冶金过程中占据中心地位,吸引了许多研究人员的关注。由于它们各自的优点,人们使用了许多方法来收集钨和钼,例如沉淀法、溶剂萃取法、离子交换法和吸附法。在这些方法中,沉淀法和溶剂萃取法在某些行业中更受欢迎和应用。然而,任何一种处理方法总会有额外的缺点或不足。
回收这两种金属的最大挑战来自于它们相似的性质。钨和钼属于同一亚族元素,具有非常相似的化学和物理性质。此外,钨和钼经常共存于同一矿石或同一二次资源中,增加了提取难度。此外,钨和钼的水化学性质都很复杂。在含钨或钼的水溶液中,酸聚合总是产生异构酸。在含钨钼的水溶液中,水解和聚合反应不仅会产生异构酸,还会生成杂多酸。在所有因素中,pH值和金属浓度是决定金属种类的主要因素。
溶剂萃取法因其产品纯度高、操作简单、分离效率高等优点而被认为是一种很有前途的方法。根据不同的机理,有多种利用溶剂萃取回收钨或钼的方法。因此,研究不同条件下钨和钼在水溶液中的物种分布和热力学性质非常重要。
参考:
[1]Oishi T, Yaguchi M. Solubility of sodium tungstate in molten sodium hydroxide[J]. Electrochemistry, 2018, 86(2): 61-65.
[2]https://www.sciencedirect.com/science/article/abs/pii/S002196141600032X
[3]https://baike.baidu.com/item/%E9%92%A8%E9%85%B8%E9%92%A0
[4]https://en.wikipedia.org/wiki/Sodium_tungstate
[5]https://www.sciencedirect.com/topics/chemistry/sodium-tungstate
[6]中南大学. 一种从粗钨酸钠溶液制备钨产品的方法:CN201810362727.2[P]. 2020-07-31.