吡唑-3-甲酸,化学式为C?H?N?O?,是一种含有吡唑环和羧酸基团的有机化合物。在常温下,它通常以白色或淡黄色的结晶粉末形式存在,具有一定的稳定性和热稳定性。吡唑-3-甲酸易溶于有机溶剂如乙醇、乙醚等,而难溶于水,这一性质为其在有机合成中的应用提供了便利。吡唑环作为吡唑-3-甲酸的核心结构,具有独特的共轭体系和芳香性,使得该分子在化学反应中表现出丰富的化学性质。羧酸基团则赋予了吡唑-3-甲酸良好的反应活性,可以参与酯化、酰化、酰胺化等多种有机反应,为合成复杂有机分子提供了可能[1-2]。

吡唑-3-甲酸的性状
高锰酸钾氧化法:一种常见的合成吡唑-3-甲酸的方法是通过高锰酸钾(KMnO?)氧化3-甲基吡唑或其衍生物。例如,将3-甲基-1(2)H-吡唑溶解在水中,加入高锰酸钾的水溶液,加热回流数小时。反应结束后,将混合物冷却、过滤并酸化滤液,最终得到吡唑-3-甲酸。此方法操作简单,产率较高,是实验室和工业上常用的合成方法之一。
吡啶溶液回流法:另一种合成吡唑-3-甲酸的方法是将3-甲基吡唑溶于水和吡啶的混合溶液中,加热回流并分批加入高锰酸钾。反应完成后,通过过滤、萃取和浓缩等步骤,可以得到吡唑-3-甲酸。这种方法利用了吡啶对反应的促进作用,提高了反应效率和产物的纯度[2-3]。
医药领域:吡唑-3-甲酸及其衍生物在医药合成中扮演着重要角色。它们可以作为合成具有抗菌、抗炎、抗肿瘤等生物活性的药物分子的关键原料。通过合理的分子设计和合成策略,可以开发出新型的高效低毒药物,为人类的健康事业做出贡献。
农药领域:吡唑-3-甲酸类化合物在农药领域也表现出良好的应用潜力。它们可以作为杀虫剂、除草剂等农药的活性成分,通过干扰害虫或杂草的生理代谢过程,达到防治病虫害的目的。同时,由于其独特的化学结构和生物活性,吡唑-3-甲酸类农药还具有高效、低毒、环保等优点[1-4]。
[1] 李家星,杨洪利,倪萌,等.吡唑-3-甲酸、铅配位聚合物的合成、晶体结构和荧光性质[J].信阳师范学院学报:自然科学版, 2017, 30(4):4.
[2] 蒋秀燕,荣念新,邱田田,等.吡唑-3-甲酸Cu(Ⅱ)/Mn(Ⅱ)配合物的合成、表征及常压下对二氧化碳催化转化[J].无机化学学报, 2017(33):2310.
[3] 杨洪利,倪萌,李家星,等.吡唑-3-甲酸配合物的合成、晶体结构及磁性质研究[J].化学研究与应用, 2018, 30(1):5.
[4] 张秀清,陈芳,贺雄,等.吡唑-3-甲酸配合物的合成,结构及性质研究[J].信阳师范学院学报:自然科学版, 2020, 33(2):7.
5-氨基-吡唑-3-甲酸乙酯是一种有机中间体,可通过特定原料的反应得到。该化合物在制备3-溴吡唑啉[1,5-α]吡嘧啶-2-甲酸方面具有应用潜力。

在特定条件下,通过反应原料的加热和旋蒸等步骤,可以得到5-氨基-吡唑-3-甲酸乙酯。该合成方法的产率较高。
5-氨基-吡唑-3-甲酸乙酯在合成3-溴吡唑啉[1,5?α]吡嘧啶?2?胺的过程中起到关键作用。通过与其他化合物反应,可以生成具有高钾离子调解活性的酰胺。这些酰胺能够调节细胞膜上钾离子的数量和速率。
[1] [中国发明] CN201210050804.3 7-溴吡唑并[1,5-a]嘧啶-3-甲酸酯类化合物、合成方法及应用
[2] [中国发明] CN201210328094.6 3-溴吡唑啉[1,5-α]吡嘧啶-2-甲酸的合成工艺
5-溴-吡唑-3-甲酸是一种有机合成中间体和医药中间体,可用于实验室研发过程和化工医药合成过程中。

为了制备5-溴-吡唑-3-甲酸,首先将2.46g 3-氨基巴豆腈(1)与20mL的质量分数为25%水合肼水溶置于50mL三口烧瓶中。然后,在80℃下加热至回流反应8小时。反应结束后,将多余的水合肼真空下抽干,并对残渣进行蒸馏,得到3-氨基-5-甲基吡唑(2),产率为75%。
接下来,将1.9g 3-氨基-5-甲基吡唑(2)、15mL浓氢溴酸和2.8g溴化亚铜混合置于100mL三口烧瓶中,加热至70℃。然后,取约1.5g亚硝酸钠溶于5mL水中,使用恒压漏斗缓慢滴加入三口烧瓶中。加料完成后,将反应液于70℃搅拌反应30分钟,之后冷却至室温,加入20mL THF和20mL水。使用30mL乙醚萃取三次,将有机层用硫代硫酸钠溶液洗涤后使用硫酸镁干燥。之后使用硅胶过滤,减压蒸馏除去溶剂,得到3-甲基-5-溴吡唑(3),产率为62%。
最后,将1.7g 3-甲基-5-溴吡唑(3)溶于20ml 0.1M盐酸中,置于100mL三口烧瓶中,加热至50℃。然后,取约1.5g高锰酸钾溶于5mL水中,使用恒压漏斗缓慢滴加入三口烧瓶中。加料完成后,将反应液于70℃搅拌反应30分钟,之后冷却至室温,将溶液pH调至酸性,加入20mL EtOAc,萃取三次,有机层pH调至碱性,加水洗涤,得到5-溴-1H-3-吡唑甲酸(4),产率为85%。

氯虫苯甲酰胺是一种广谱杀虫剂,由杜邦公司发现并开发。氯虫苯甲酰胺的ISO通用名为Chlorantraniliprole,化学名为3-溴-N-{4-氯-2-甲基-6-[(甲氨基)羰基]苯基}-1-(3-氯-2-吡啶基)-1H-吡唑-5-酰胺,CAS登记号为500008-45-7。1-(3-氯-2-吡啶基)-3-溴-1H-5-吡唑甲酸是合成氯虫苯甲酰胺的一个重要中间体。5-溴-吡唑-3-甲酸可用于制备1-(3-氯-2-吡啶基)-3-溴-1H-5-吡唑甲酸。
制备1-(3-氯-2-吡啶基)-3-溴-1H-5-吡唑甲酸的方法是将1eq 5-溴-1H-3-吡唑甲酸(4)与1eq 2,3-二氯吡啶溶于适量乙醇溶液中,加入2eq碳酸钾固体,升温回流反应24小时。之后冷却至室温,使用乙酸乙酯洗涤三次,再向水层加入1M盐酸溶液使反应液pH调至酸性,使用EtOAc萃取三次,将有机层无水硫酸钠干燥。干燥后过滤浓缩得到中间体1-(3-氯-2-吡啶基)-3-溴-1H-5-吡唑甲酸(5),产率为70%。
[1] CN201510201127.4 一种中间体1-(3-氯-2-吡啶基)-3-溴-1H-5-吡唑甲酸的合成方法
5-氨基-吡唑-3-甲酸乙酯是一种有机中间体,可以通过3-硝基-吡唑-3-甲酸酯化后还原硝基得到。

在室温下,将3-nitro-1H-pyrazole-5-carboxylic acid(50g,318.3mmol)溶解在EtOH(300mL)中,在冰水浴0℃下滴加SOCl2(49g,412mmol),加完后回流搅拌8小时。经TLC监测反应完全后,减压浓缩得到粗产品,将其溶解在CH2Cl2(30mL)中,用饱和NaHCO3水溶液调pH=7~8,经CH2Cl2萃取(3×30mL),饱和食盐水(10mL)洗涤,干燥,抽滤,浓缩滤液后得到白色固体化合物B-1(58.7g,收率99.6%)。ESI[M+H]+=186.1
在室温下,将B-1(58.7g,317mmol)和10%湿钯碳(6g)溶于EtOH(200mL)中,用氢气置换体系三次,将反应体系置于氢气环境中室温搅拌18小时。经TLC监测反应完全后,抽滤,滤饼用EtOH(3×30mL)洗涤,将滤液减压浓缩得到粗产品,粗产品经硅胶柱层析纯化(乙酸乙酯/石油醚(v/v)=1/20~1/1),TLC(乙酸乙酯/石油醚(v/v)=1/1)监测,收集Rf=0.4~0.5部分,得到灰色固体化合物5-氨基-吡唑-3-甲酸乙酯(43.5g,收率88%)。ESI[M+H]+=156.1
3-溴吡唑啉[1,5-α]吡嘧啶-2-甲酸是合成3-溴吡唑啉[1,5-α]吡嘧啶-2-胺的关键中间体。5-氨基-吡唑-3-甲酸乙酯作为原料与1,1,3,3-四甲氧基丙烷缩合得到吡唑啉[1,5-α]吡嘧啶-2-酸乙酯,再与NBS反应得到3-溴吡唑啉[1,5-α]吡嘧啶-2-酸乙酯,最后在氢氧化钠水溶液中水解得到3-溴吡唑啉[1,5-α]吡嘧啶-2-酸。这个合成路线简洁、工艺选择合理、原料成本低、操作和后处理方便,总收率高,不使用剧毒试剂,易于放大,可用于大规模生产。相比现有文献工艺,它解决了原料昂贵、收率低、需要微波条件、操作复杂、后处理困难、不易放大等问题。
[1] [中国发明] CN202011073826.2 酮取代杂环化合物及其麻醉作用
[2] CN201210328094.63-溴吡唑啉[1,5-α]吡嘧啶-2-甲酸的合成工艺
1,4,5,6-四氢环戊并吡唑-3-酰肼是一种常用的医药中间体。它可以通过环戊酮和草酸二乙酯作为起始物料,先制备1,4,5,6-四氢环戊并吡唑-3-甲酸乙酯,再与水合肼反应得到。制备过程如下:


首先,在搅拌下,向500mL的三口瓶中加入环戊酮和草酸二乙酯。然后,向三口瓶中滴加乙醇钾和乙醇的混合液,并在室温下加入浓盐酸,调节pH值。保持温度不超过40℃,搅拌反应20分钟后,将反应液冷却至室温,缓慢滴加水合肼。滴加过程中会产生白色烟雾,继续搅拌反应1.5小时,直到原料完全消耗。最后,加入纯水,蒸干后得到黄色固体1,4,5,6-四氢环戊并吡唑-3-甲酸乙酯。

接着,将1,4,5,6-四氢环戊并吡唑-3-酰肼和肼加入乙醇中,加热至回流1天。在此阶段结束时,蒸发乙醇,并通过过滤收集沉淀物,用乙酸乙酯和水洗涤得到最终产物。
[1] [中国发明] CN201310729455.2 一种医药中间体1,4,5,6-四氢-3-环戊并吡唑甲腈的合成工艺
[2] From PCT Int. Appl., 2013162469, 31 Oct 2013
卤素取代的1H-吡唑-3-甲酸酯在医药领域有着广泛的应用,例如可用于制备脂质合成的杂环调节剂化合物以及其药学上可接受的盐,合成11-β羟基类固醇脱氢酶类型1抑制剂和V1b受体拮抗体等。现有报道的方法存在以下不足:该合成路线总收率为15.3%,收率较低;b步骤中加氢反应有一定的危险性;c步骤中重氮化反应有火灾危险性,重氮化反应所产生的重氮盐,在温度稍高或光的作用下,即易分解,有的甚至在室温时也能分解,在干燥状态下,有些重氮盐不稳定,活力大,受热或摩擦、撞击,能分解爆炸。在文献报道以3-溴吡唑为原料,先与二甲基硫酰氯反应形成N-二甲基硫酰基衍生物以保护氮,然后在-70℃下与二异丙氨基锂作用,并用二氧化碳淬灭,最后用甲醇酯化,得到3-溴-1H-吡唑-5-甲酸甲酯。5-氟-1H-吡唑-3-羧酸乙酯的报道较少。
5-氟-1H-吡唑-3-羧酸乙酯的制备如下:

1)化合物II制备化合物III:将化合物II(120.0g,0.705mol,1.0e.q.)加入二甲苯(1200mL),再加入三氟乙酸(4.02g,0.0353mol,0.05e.q.),加完后升温至140℃,反应6小时,GC检测原料反应完,加入饱和碳酸钠水溶液洗涤,用乙酸乙酯萃取(3×900mL),用无水硫酸镁干燥,过滤,滤液浓缩干得化合物III黄色液体108.0g,收率90.0%。
2)化合物III制备化合物IV:将化合物III(70.0g,0.411mol,1.0e.q.)溶解在THF(700mL)中,氮气保护下,-78℃滴加2.5M正丁基锂/正已烷(197mL,0.494mol,1.2e.q.),滴毕-78℃保温20分钟,缓慢通入干燥的二氧化碳气体约15分钟后,停止通入二氧化碳,开始滴加1N的盐酸水溶液,调节pH=2,加入1L的乙酸乙酯萃取,干燥浓缩得黄色油状物,加入500mL的石油醚打浆,析出固体,过滤,得到化合物IV白色固体70.5g,收率80.0%。
3)化合物IV制备化合物5-氟-1H-吡唑-3-羧酸乙酯I-1:将化合物IV(70.0g,0.327mol,1.0e.q.)溶于甲醇(500mL)中,冰水浴条件下,滴加氯化亚砜(77.8g,0.654mol,2.0e.q.),滴毕回流10h,浓缩反应液,用饱和碳酸氢钠调节pH=8,再用乙酸乙酯(500mL×2)萃取,干燥浓缩,浓缩液用乙酸乙酯与石油醚(体积:体积=1:50)打浆,得化合物I-1白色固体36.9g,收率78.2%。
[1] CN201710753540.0一种5-氟-1H-吡唑-3-甲酸酯中间体及其合成方法
利奥西呱是一种可溶性鸟苷酸环化酶激动药,用于治疗肺动脉高压和慢性阻塞性肺动脉高压。本文介绍了利奥西呱的合成方法及工艺改进。
利奥西呱的合成方法包括使用邻氟苄肼和氰基丙酮酸钠盐反应闭环得到5-氨基-1-(2-氟苄基)吡唑-3-甲酸乙酯,然后经过一系列官能团转化得到最终产物1。
本研究对利奥西呱的合成进行了工艺改进。改进包括使用邻氟溴苄和水合肼反应制备起始原料2,使用1,1,3,3-四甲氧基丙烷替代昂贵的N,N-二甲胺基丙烯醛制备中间体5,简化了操作流程。此外,在制备化合物8和12时,优化了反应条件,使得纯化操作更加简便。经过工艺改进后,利奥西呱的总收率达到12.4%,且工艺更加经济高效。
实验部分包括了各个中间体的合成步骤。
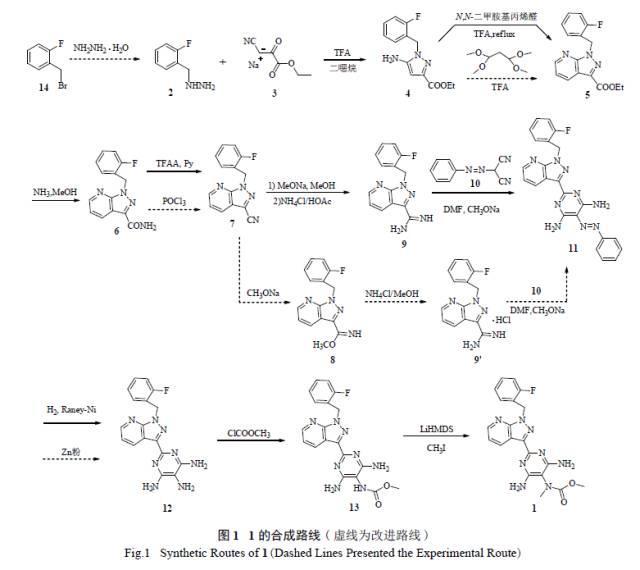
2-氟苄肼(2)
1-(2-氟苄基)-1H-吡唑并[3,4-b]吡啶-3-甲酸乙酯(5)
1-(2-氟苄基)-1H-吡唑并[3,4-b]吡啶-3-甲酰胺(6)
3-氰基-1-(2-氟苄基)-1H-吡唑并[3,4-b]吡啶(7)
1-(2-氟苄基)-1H-吡唑并[3,4-b]吡啶-3-甲酰亚胺酸甲酯(8)
1-(2-氟苄基)-1H-吡唑并[3,4-b]吡啶-3-甲脒盐酸盐(9')
2-[1-(2-氟苄基)-1H-吡唑并[3,4-b]吡啶-3-基]-5-[(E)-苯基二氮烯基]-4,6-嘧啶二胺(11)
2-[1-(2-氟苄基)-1H-吡唑并[3,4-b]吡啶-3-基]-4,5,6-嘧啶三胺(12)
4,6-二氨基-2-[1-(2-氟苄基)-1H-吡唑并[3,4-b]吡啶-3-基]-5-嘧啶基氨基甲酸甲酯(13)利奥西呱(1)
来源:中国医药工业研究总院上海医药工业研究院,创新药物与制药工艺国家重点实验室,上海 201203
2,2-二甲基哌啶-4-醇盐酸盐是一种常用的医药合成中间体,广泛应用于实验室研发和化工医药合成过程中。
2,2-二甲基哌啶-4-醇盐酸盐可用于医药合成中间体的制备。例如,可以用它来合成(1-(3,5-二氯苯基)-7-甲氧基-8-(吡啶-2-基)-1,4-二氢苯并吡喃并[4,3-c]吡唑-3-基)(4-羟基-2,2-二甲基哌啶-1-基)甲酮。

制备方法如下:
1)在室温下,将8-溴-1-(3,5-二氯苯基)-7-甲氧基-1,4-二氢苯并吡喃并[4,3-c]吡唑-3-甲酸(500mg,1.07mmol)溶解在DMF(20mL)中,然后加入2,2-二甲基哌啶-4-醇盐酸盐(166mg,1.28mmol)、HATU(407mg,1.07mmol)和二异丙基乙胺(0.57mL,3.21mmol)。在室温下搅拌3小时。用碳酸氢钠(10mL,10%)淬灭反应,然后用EtOAc(2x50mL)萃取。将有机层用盐水(30mL)洗涤,然后用无水Na2SO4干燥。去除溶剂后,用石油醚和乙酸乙酯(5∶1)进行柱色谱纯化,得到白色固体的目标化合物(8-溴-1-(3,5-二氯苯基)-7-甲氧基-1,4-二氢苯并吡喃并[4,3-c]吡唑-3-基)(4-羟基-2,2-二甲基哌啶-1-基)甲酮(500mg,80%)。
2)在室温下,将(8-溴-1-(3,5-二氯苯基)-7-甲氧基-1,4-二氢苯并吡喃并[4,3-c]吡唑-3-基)(4-羟基-2,2-二甲基-N-二甲基哌啶-1-基)甲酮(200mg,0.35mmol)溶解在DMF(5mL)中,然后加入2-(三丁基甲锡烷基)吡啶(193mg,0.53mmol)和Pd(dppf)Cl2(29mg,0.07mmol)。在120℃下用微波加热2小时。通过制备型HPLC纯化混合物,得到黄色固体的目标化合物(30mg,15%)。
1HNMR(400MHz,CDCl3): δ8.98(d,1H), 8.07(t,J=7.8Hz,1H), 7.67(d,J=7.8Hz,1H), 7.53(d,J=1.8Hz,3H), 7.46(t,J=1.8Hz,1H), 7.22(s,1H), 6.74(s,1H), 5.54(q,J=13.8Hz,2H), 4.23-4.04(m,2H), 3.87(s,3H), 3.68-3.59(m,1H), 2.16(s,1H), 1.90(dd,J=13.5,4.9Hz,1H), 1.75(dd,J=24.2,10.9Hz,1H), 1.68(s,3H),1.53(s,3H)。
[1] CN201480081442.1作为FSHR调节剂的吡唑化合物及其用途