吡啶氢氟酸盐是一种无色至棕色的液体。它作为氟化试剂,在有机合成中表现出高度的活性和选择性。吡啶氢氟酸盐可以看作是氟化氢与吡啶形成的络合物,这种结构使其具有较高的沸点和独特的反应性质。根据文献报道,吡啶氢氟酸盐的分子量约为99.10620,密度约为1.1 g/mL,沸点为115.3°C(在760 mmHg下),闪点为20°C。这些物理性质为其在实验室和工业中的应用提供了便利[1]。

吡啶氢氟酸盐的性状
吡啶氢氟酸盐在有机合成中扮演着重要角色。作为氟化试剂,它可以参与多种有机物的氟化反应,生成具有特定官能团的化合物。这些氟化产物在药物合成、农药开发、材料科学等领域具有广泛应用。例如,在药物合成中,氟原子的引入可以改变分子的生物活性和药代动力学性质,从而提高药物的疗效和安全性。吡啶氢氟酸盐还可以用于构建复杂结构的化合物骨架,为新药研发提供有力支持。
吡啶氢氟酸盐经口、吸入或皮肤接触均可引起急性中毒。其中,经口摄入的毒性尤为严重,可能导致致命的后果。因此,在使用和储存过程中必须严格遵守安全操作规程,避免直接接触和误食。此外,吡啶氢氟酸盐具有强烈的皮肤腐蚀性,能够迅速破坏皮肤组织并引起严重的灼伤。一旦发生皮肤接触,应立即用大量清水冲洗,并尽快就医治疗。同时,应穿戴适当的防护装备,如防护服、手套和护目镜等,以减少皮肤接触的风险[1]。
[1]佚名.一种吡啶氢氟酸盐的制备方法及其应用:CN202410204584.8[P].CN118084158A[2024-07-14].
[2]张涵.吡啶氢氟酸盐介质中铝缓蚀剂的研制及缓蚀性能研究[D].辽宁师范大学,2015.
吡啶氢氟酸盐化合物在农药、医药、材料领域具有广泛的应用。其独特的吡啶结构在各类药物研究中扮演着重要角色。作为重要的化工中间体,吡啶氢氟酸盐广泛应用于医药、农药、染料以及其他有机合成中。它在复杂结构的化合物骨架构建、药物中间体合成、天然产物合成以及荧光材料开发等多个领域都有应用。总之,吡啶氢氟酸盐具有特殊的化学性质和药用活性,是许多医药、农药的中间体,具有广阔的应用前景。随着有机合成化学领域的快速发展,不断涌现出新的催化剂、合成方法和合成工艺。

图1 展示了吡啶氢氟酸盐的合成路线。为了合成吡啶氢氟酸盐,需要将吡啶固化后,通过入口管将无水氟化氢冷凝到瓶中。然后,将溶液加热至室温,最终得到吡啶氢氟酸盐。
在吡啶氢氟酸盐的运输过程中,应避免日晒和雨淋,并且不得与有毒、有害物品混运。吡啶氢氟酸盐属于非危险品,可按照一般化学品运输的标准进行。
吡啶氢氟酸盐化合物应贮存在干燥、清洁、避光的环境中,严禁与有毒物质混放,以免污染。同时,应将其储存于阴凉、通风的库房,远离火源、热源和水源。吡啶氢氟酸盐也应与氧化剂分开存放,切忌混储。此外,储存区应配备相应品种和数量的消防器材,并备有泄漏应急处理设备和合适的收容材料。
[1] Boateng, Kenneth A.; et al. Removal of light fluoroalkanes from hydrocarbon streams by contacting with strong acid functionality adsorbent. United States.
吡啶氟化氢是一种有机-无机化合物,它是一种无色、有刺激性气体,常温下为液态。
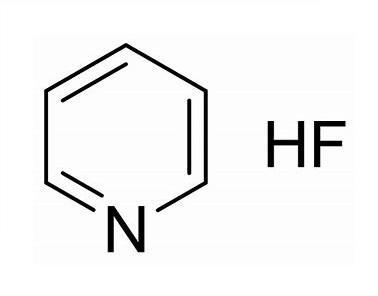
密度:1.1g/mL at 20°C(lit.);
氟化氢吡啶溶液;
沸点:50℃/1mmHg。
氟化氢吡啶是由氟化氢(HF)和吡啶(C5H5N)形成的化合物。氟化氢是一种强酸,而吡啶则是一种弱碱。它们在一起反应会形成络合物,即氟化氢吡啶络合物。氟化氢吡啶络合物的形成是因为氟化氢和吡啶之间的氢键形成了一种稳定的化学结构。
氟化氢吡啶在有机合成、药物制造、表面活性剂、催化剂以及制备高纯度半导体材料等领域有广泛应用。在有机合成领域中,氟化氢吡啶络合物作为氟化试剂,可以为分子引入氟原子,提高化合物的药物活性和光学活性。在表面活性剂中,氟化氢吡啶络合物可以被用作染色剂、洗涤剂和清洁剂成分。在催化剂中,氟化氢吡啶络合物可以催化有机反应。在半导体材料中,氟化氢吡啶可以用于清洗晶圆表面,制备高纯度的硅晶圆。
此外,氟化氢吡啶络合物还可以用于生产氟化物盐酸盐、氢氟酸酯和氟化硅等化学品。同时,它也是氟离子探测测定的试剂。
危险代码:T+
危险等级:26/27/28-35
安全等级:26-28-36/37/39-45
联合国编号:UN1790
3-氟苯酚是一种有机化合物,化学式为C6H5F,它是苯环上的3号位置被一个氟原子取代的苯酚衍生物。在化学和药物领域中,3-氟苯酚具有一定的应用,可用作有机合成中的试剂和中间体。
制备3-氟苯酚的方法如下:
1、将原料间的氨基苯酚完全溶解于有机溶剂中,并将温度降至10~15℃。在搅拌下缓慢滴加无水氢氟酸,直到滴加完毕后继续搅拌反应,直到原料完全转化为氢氟酸盐。原料间的氨基苯酚与有机溶剂的体积比为1∶3~5,与无水氢氟酸的摩尔比为1∶3~35。
2、当反应体系完成后,将体系冷却至-10℃,然后均匀加入固体KNO,并在-5℃控制下进行反应。原料间的氨基苯酚与固体亚硝酸钠的摩尔比为1∶105~125。
3、分段升温进行热解反应。以每小时5℃的速率升温至65℃,停止加热,并待系统不再继续升温后,将温度降至10℃。在反应体系中缓慢滴加10%的KOH水溶液进行中和,保持中和反应的温度为30℃,直到体系的pH值达到7后,停止搅拌,使体系静置分层。
4、将分离出的有机相进行两次水洗,然后用有机溶剂将分离的水相进行萃取,将合并的有机相通过过滤去除固体残留物后,再次分离水相,并进行精馏。
5、进行常压精馏以分离有机溶剂,并进行回收。然后进行减压精馏,得到产品3-氟苯酚。

注意事项:
1、上述3-氟苯酚的制备方法,所用的有机溶剂为甲苯、氟苯、氟代甲苯、吡啶中的一种或者混合物,间氨基苯酚与有机溶剂的体积比为1∶3~5,氟化介质为无水氢氟酸,间氨基苯酚与无水氢氟酸的摩尔比为1∶3~35。
2、根据权利要求1所述的3-氟苯酚的制备方法,重氮化试剂选用KNO,间氨基苯酚与 KNO的摩尔比为1∶105~125。
[1]阜新四维卤化物有限公司.一种3-氟苯酚的制备方法:CN104276929A[P].2015-01-14.
4-氟吡啶盐酸盐是一种有机中间体,可通过对4-氨基吡啶进行重氮化反应制备。

将4-氨基吡啶(7.06 g, 75.1 mmol)悬浮于40 mL无水二氯甲烷中,在-78°C下搅拌15分钟,然后将其加入已冷却至-78°C的无水氢氟酸(31.2 g, 1.6 mol)中。将反应混合物升温至-5°C,并在10分钟内分批加入NaNO2(6.22 g,90.1 mmol),同时保持温度在-5°C和0°C之间。将混合物升温至室温,然后加热至40-50°C,反应1.5小时。加入二氯甲烷(50 mL),冷却至-10°C后,滴加30% NH4OH水溶液,调节pH至10。过滤破乳,进行二氯甲烷萃取。在硅胶上干燥后,通过HCl气体鼓泡溶液,进行溶剂的真空蒸发,得到4.9 g(37.1 mmol,50%)淡黄色盐。
4-氟吡啶盐酸盐可用于制备具有Bub1抑制剂结构的化合物。Bub1抑制剂具有治疗温血动物(如人类)中与不受控制的细胞增殖过程相关的增殖性病症的治疗价值,例如癌症、炎症、关节炎、病毒性疾病、心血管疾病或真菌性疾病。

4-氟吡啶盐酸盐还可用于制备具有PIM抑制剂结构的化合物。

PIM-1、PIM-2和PIM-3通常对生长因子和细胞因子的刺激产生反应,从而对造血细胞的生存和扩散起作用。剔除PIM-1、PIM-2和PIM-3基因的小鼠能够正常存活,但个体较小,并且在造血细胞扩散过程中对生长因子的反应也减弱。如果只剔除其中一种PIM基因,对小鼠没有明显影响,这表明三种PIM的功能有所重叠。PIM激酶的底物包括调节细胞凋亡的Bcl-2家族成员BAD、调节细胞周期的p21、CDC25A和C-TA,以及调节蛋白质合成的4EBP1。PIM激酶的这些作用显示其具有防止细胞凋亡和促进细胞生长和扩散的功能。因此,在肿瘤中过度表达的PIM激酶对癌细胞的存活和扩散起到作用。因此,抑制肿瘤中过度表达的PIM激酶是治疗癌症的有效方法。除了治疗癌症外,PIM激酶抑制剂还可用于治疗自免疫疾病、过敏和器官移植的免疫反应。
[1] Journal of Organic Chemistry, 66(12), 4220-4226; 2001
[2] PCT Int. Appl., 2013092512, 27 Jun 2013
[3] PCT Int. Appl., 2010022076, 25 Feb 2010
间氟硝基苯作为重要的化合物,其合成方法备受关注。本文旨在探讨目前常见的关于合成间氟硝基苯的重氮化氟化法和氟代脱硝法。
背景:大多数芳香族氟化物是通过间接方法制得的。其氟化的方法主要可分为三大类,即:芳胺的重氮化氟化法(主要是Balz-Schiemann反应),卤素交换法,催化氟化及特殊氟化剂氟化法。
鉴于实验条件的可操作性,催化氟化和特殊氟化剂氟化法逐渐被淘汰。至于卤素交换法,一般由相应的氯或溴化物,与氟化碱金属,在惰性的极性溶剂中,在铵离子存在下进行交换,制得氟化物。该法对于邻或对位取代的含氟芳香族化合物的合成是有效的,但一般不易得到间位取代物。间氯硝基苯较难氟化,需要较长的反应时间达到较好的转化率。温度高于200℃时,尽管反应速率提高,但是由于一些不明的副反应,碳回收率降低。近年来发现,氟代脱硝可以高收率合成间氟芳香族化合物,其条件是芳环上具有吸电子基团。因此,近年来的研究逐渐侧重于重氮化氟化法和氟代脱硝法。
1. 以间硝基苯胺为原料的重氮化氟化法
1.1 在氟硼酸中重氮化

重氮化过程:将34g(0.4mol)间硝基苯胺溶解于110mL 40%(0.5mol)氟硼酸中,在0℃下滴加亚硝酸钠溶液(17g亚硝酸钠溶于34mL水)进行重氮化,滴加完继续反应30min。过滤,用冷氟硼酸、乙醇和乙醚洗涤滤饼,干燥,得53g固体,收率89%。
热解过程:将13g重氮盐和25g高沸点矿物油加热至分解。当反应缓和后,继续加热一小段时间。产物通过水蒸汽蒸馏达到分离目的,馏出物用乙醚萃取,萃取液用25mL 5%氢氧化钠溶液洗涤,干燥,蒸馏,收集bp:96~97℃(23mm Hg) 的馏分,得到4.3g液体,收率57%。
1.2 在吡啶聚氢氟酸盐中重氮化

可以在无水氟化氢中进行重氮化反应。苯胺和吡啶鎓聚合物(HF)反应制备氟苯。
氟苯的制备方法如下:将1.86克(0.02摩尔)苯胺溶解于50毫升吡啶鎓聚合物(HF)中,缓慢加入2.1克(0.03摩尔)亚硝酸钠,室温搅拌1小时,然后将反应液转移到不锈钢容器中,加热至85℃,经过1小时后,用冰水冷却反应,250毫升乙醚分三次萃取,萃取液用5%碳酸钠溶液中和,后干燥,蒸发溶剂,得到1.33克氟苯,收率为70%。
2. 以间二硝基苯为原料的氟代脱硝法
2.1 以氟化钾为氟代脱硝试剂

在三口烧瓶中加入4.32g氟化钾,6.72g间二硝基苯和0.2g邻苯二甲酰氯 (PDC),迅速加入极性非质子溶剂环丁砜30m L,在油浴锅里回流反应6h。反应结束后,抽滤除出固体物,并用苯洗涤滤饼数次,合并滤液及洗液。用水蒸汽蒸馏,分出馏出液。用苯萃取馏出液中水相2~3次,合并有机相,蒸馏除去苯,得粗产物间氟硝基苯,收率65.4%。
2.2 以四烷基氟化铵为氟代脱硝试剂

四烷基氟化铵(R4NF)的制备:将过量30%的氟化钾与四烷基氯化铵在含水5%的甲醇溶液中搅拌回流4h后,冷却,过滤,滤液减压浓缩后得白色固体, 即为R4NF。R=CH3时,收率95%,含量85%;R=C2H5时,收率94%,含量86%。
氟代脱硝反应:将过量25%的R4NF加入到40mL苯和90mL二甲亚砜的混 合溶剂中,加热,用苯水共沸的方法将体系处理至无水,蒸去苯,然后加入0.1mol 的间二硝基苯,在指定的温度下搅拌反应2h后,以80mL环己烷抽提反应混合物,减压精馏得纯间氟硝基苯,收率80%。
在这种反应条件下,由于温度低、氟化剂活性强,反应可以迅速完成。因此生成的酚及其衍生物相比KF高温氟化的情况要少,没有检测到氧化副产物。而在KF高温氟化反应条件下,这些物质都是可检测到的。因此,四烷基氟化铵作为氟化剂具有降低反应温度、缩短反应时间、减少副反应等优点,是一种具有前景的氟化剂。
参考文献:
[1]胡玉锋;罗军;梁政勇;黄成美;吕春绪. 氟代脱硝制备含氟硝基苯 [J]. 应用化学, 2008, (11): 1356-1360.
[2]夏文娟. 3-氟-4-硝基苯酚的合成研究[D]. 天津大学, 2008.