左旋羟丙哌嗪是一种新型镇咳药,具有较好的镇咳效果。它是羟丙哌嗪的消旋体,克服了基消旋体对中枢神经的副作用。该药品于1988年在意大利上市,并在临床使用中受到广泛关注。


在搅拌下,将环氧氯丙烷(1200g,10mL)加入含浓硫酸(3g)的温水(600mL,56~60℃)溶液中,反应2小时。然后,在约90℃的条件下继续反应5小时。加入碳酸钙粉末(5g)并搅拌0.5小时后,进行减压蒸馏。收集100~108℃/0.4kPa的馏分,得到无色油状的3-氯-1,2-丙二醇。平均产量为864g,平均收率为69.4%(以环氧氯丙烷实际消耗量计),含量达99.5%以上(HPLC)。
在搅拌下,将适量浓盐酸(750mL,8.7mol)缓慢滴加到苯胺(364mL,4mol)中,反应2小时。将温度升至240~250℃并继续反应6小时。然后,将反应液冷却至约140℃,加入400mL水使其溶解。再将其加入质量分数约45%的NaOH水溶液中,并调节pH值到11左右。分离碱液层,用水洗涤油层,使其pH值接近8。分离棕红色油状液层,进行减压蒸馏。收集126~136℃/0.7kPa的馏分,得到无色或黄色油状液的苯基哌嗪。平均产量为372g,平均收率为66%(以苯胺实际消耗计),含量达92%以上(HPLC)。
将无水碳酸钾(276.4g,2mol)、3-氯-1,2-丙二醇(221g,2mol)、苯基哌嗪(314g,1.94mol)依次加入丙酮(100mL)中,在搅拌下回流7小时。趁热过滤滤液,并在冰浴中结晶。结晶粗品再用丙酮重结晶两次(700mL×2),得到白色结晶状的外消旋羟丙哌嗪,熔点为111℃。平均产量为302g,平均收率为66%(以苯胺实际消耗计),含量达92%以上(HPLC)。
[1]熊俊如,张淑琼,曹优明.新型镇咳药左旋羟丙哌嗪的合成研究[J].四川师范大学学报(自然科学版),2001(02):174-176.
左羟丙哌嗪是一种有效的止咳药物,特别适用于急性上呼吸道感染和急性支气管炎的治疗。它对于干咳和持续性咳嗽也有良好的缓解作用。作为一种广泛使用的镇咳祛痰药,左羟丙哌嗪的副作用较少,对心血管和呼吸系统的影响也较小。
左羟丙哌嗪作为外周性镇咳药,通过选择性抑制气管和支气管的C-纤维外周作用来发挥镇咳作用。它的作用部位是与感觉性神经肽相关的外周结后位点。
左羟丙哌嗪的镇咳作用强且持久,因此对于长期咳嗽症状的患者来说,它是一种很好的治疗选择。由于不影响β肾上腺素受体、M胆碱受体和阿片受体,因此它的中枢抑制作用较小,是一种高效且安全的镇咳药物。正因如此,左羟丙哌嗪的使用范围也很广泛。
在选择镇咳药物时,市面上有很多选择,临床上的产品种类也很丰富。但应根据患者的具体情况和症状进行分析,不能盲目选择药物。左羟丙哌嗪虽然效果好,但也有一些禁忌症和不良反应,如嗜睡和头痛等。因此,在使用前建议咨询医生的意见。
在秋冬季节的时候,最常见的症状之一就是感冒咳嗽。为了避免出现其他肺气肿等疾病,我们需要积极治疗咳嗽。据说使用左羟丙哌嗪可以有效改善镇咳效果。那么,左羟丙哌嗪到底是什么药物?它是否具有镇咳效果?
左羟丙哌嗪的熔点约为98到100摄氏度,沸点约为142.7摄氏度。这种药物最早在意大利上市,可用作手性镇咳药物,对于治疗剧烈的无痰干咳有良好的效果。与其他镇咳药物相比,左羟丙哌嗪属于外周性镇咳药物,不会对中枢神经产生影响,也不会对身体产生其他不良反应。它的镇咳作用被广泛认可,并且不会导致依赖性、呼吸抑制或嗜睡等症状。
现在我们对左羟丙哌嗪是否是一种有效的镇咳药物有了更好的了解。除了发挥镇咳和止咳作用外,它还可以辅助治疗咽喉炎、气管炎和支气管炎等疾病引起的干咳或持续性咳嗽等症状,效果非常好。当然,不同的咳嗽症状需要注意不同的用药量。
随着秋冬季节的到来,天气逐渐寒冷,易导致感冒发烧、咳嗽等症状。当出现这些症状时,我们应积极治疗并及时报告。尤其是当高温不退时,更需要引起特别重视。咳嗽是最常见的症状之一。据说使用左羟丙哌嗪后,对于镇咳祛痰效果非常好。
左羟丙哌嗪的熔点约为98到100摄氏度,沸点为412.7摄氏度。在存放时,我们不能忽视相关的存储条件。一般建议在室内存放。左羟丙哌嗪是一种镇咳药物,对改善呼吸道系统有很好的效果,特别适用于治疗剧烈的无痰干咳。与其他镇咳药物相比,它属于一种外周性镇咳药物。不用担心会对中枢神经系统产生影响,且具有较好的选择性。它的镇咳作用非常强大,且不会引起嗜睡或其他依赖性症状,可以放心使用,副作用较小。
现在我们对左羟丙哌嗪是一种镇咳药物有了更好的了解。正确使用这种药物对改善气管或支气管等问题非常有帮助。然而,在使用时需要注意不同年龄患者或病情严重程度不同,使用方法和剂量可能会有所不同。
呼吸系统疾病是一种常见病、多发病,主要病变在气管、支气管、肺部及胸腔。咳、痰、喘是呼吸系统疾病的主要临床症状,多为感染、药物的不良反应或变态反应等多种因素所致。在我国,由于人口密集、吸烟人口多,以及环境污染等因素,近年的呼吸系统的发病率及病死率均居高不下。

左羟丙哌嗪最早由意大利一家公司开发,1988年10月在意大利上市,随后相继在一些欧洲国家上市。在国外上市后很快被列入非处方药,并迅速占领欧美止咳药物市场。适应于继发于咽喉炎、气管炎、支气管炎以及阻塞性病因等呼吸系统疾病引起的干咳和持续性咳嗽。以及药物不良反应引起的干咳,如卡托普利等。
左羟丙哌嗪是一种止咳作用非常不错的产品,在急性上呼吸道感染和急性支气管炎的治疗当中,左羟丙哌嗪能够发挥比较好的作用。对于干咳和持续性咳嗽的症状,也可以带来良好的缓解作用。作为一种使用比较广泛的镇咳祛痰药,左羟丙哌嗪的副作用较少,而且不会对心血管及呼吸系统产生明显的作用。
在作用原理上,左羟丙哌嗪作为外周性镇咳药,通过对气管、支气管C-纤维外周选择性抑制作用而发挥镇咳作用。它的作用部位在外周结后与感觉性神经肽相关的位点。
此外,左羟丙哌嗪的镇咳作用强,维持时间长,所以对于很多有长期咳嗽症状的患者而言,左羟丙哌嗪是一种非常不错的治疗方案。由于与β肾上腺素受体、M胆碱受体和阿片受体均无作用,因此它的中枢抑制的不良反应较少,是一种高效安全的镇咳药物。
正是因为如此,左羟丙哌嗪在使用范围上面也比较广泛。目前市面上的镇咳药物非常多,在临床上面的产品数量亦非常丰富,到底应该选择一种什么样的药物?还是需要根据患者的具体情况,以及其所面临的症状来分析,不能够盲目的选择药物。左羟丙哌嗪的作用虽然好,但也会有一些禁忌的症状,还有临床的不良反应,主要包括嗜睡,头痛等,所以患者在使用过程当中也是需要注意的。一般建议在用药之前咨询一下医生。
N-苯基哌嗪是药物化学中一种重要的化合物,是镇咳药左羟丙哌嗪的主要中间体。
N-苯基哌嗪的工业制备方法有两种:一种是使用苯胺与双-(2-卤代乙基)胺盐酸盐在不同溶剂中发生环化反应制得;另一种是使用不同卤代苯与哌嗪发生缩合反应制得。第一种方法虽然原料易得,但反应时间长,产率较低,且会产生大量酸性废气废液,不利于环境保护;第二种方法需要贵重金属催化剂,副反应多,成本较高。因此,开发出适于工业化生产、低成本、低污染的N-苯基哌嗪制备方法具有特别重要的意义。
根据CN103980229B的公开内容,一种制备N-苯基哌嗪的方法是使用苯胺与双-(2-氯乙基)胺盐酸盐为原料,在设定的反应温度下熔融反应,得到N-苯基哌嗪盐酸盐;反应结束后,通过碱性水溶液处理反应液,得到粗品,再经过减压蒸馏得到纯度符合要求的产品。
苯胺与双-(2-氯乙基)胺盐酸盐的摩尔比应在1.0:1.0至2.0之间。
设定的反应温度应在160℃至250℃之间。
该方法操作简单、收率高、废液较少、成本低,纯度(HPLC)达到99.5%以上,收率在75%以上。因此,该方法适合于工业化生产N-苯基哌嗪。
CN103980229B
N-三(羟甲基)甲氨酸-2-羟基丙磺酸是一种常用的离子缓冲液,同时也是有机合成和医药中间体。它在实验室研发和化工医药合成过程中起着重要作用。

制备N-三(羟甲基)甲氨酸-2-羟基丙磺酸的方法如下:首先将242.28克(2摩尔)的三(羟甲基)氨基甲烷、500毫升水和196.5克(1摩尔)的3-氯-2-羟丙基磺酸钠混合物放入带有搅拌器和冷凝器的1升2颈烧瓶中。然后在回流条件下剧烈搅拌3小时。待冷却至25℃后,通过Dowex50,氢形式的阳离子交换树脂柱,除去钠阳离子并形成游离酸。从柱中洗脱液中得到稠油,经过酒精稀释后,产物结晶出来。通过过滤、酒精洗涤和干燥,最终得到160克白色产物N-三(羟甲基)甲氨酸-2-羟基丙磺酸,其熔点为226℃(分解)。该产物的碳含量为32.7%,氢含量为6.52%,氮含量为5.39%。计算得出的理论值为32.4%的碳、6.6%的氢和5.4%的氮。该产物在20℃的pKa为7.7。
N-三(羟甲基)甲氨酸-2-羟基丙磺酸可用于制备细胞结合剂-细胞毒性剂缀合物。在具有高离子强度的缓冲溶液中,细胞结合剂与具有反应性基团(如胺反应性基团)的细胞毒性剂或细胞毒性剂-接头化合物在pH 4至9之间反应。常用的缓冲溶液包括MES(2-(N-吗啉代)乙磺酸)缓冲液、双-三甲烷(2-[双(2-羟乙基)氨基]-2-(羟甲基)丙烷-1,3-二醇)缓冲液、ADA(N-(2-乙酰氨基)亚氨基二乙酸)缓冲液、ACES(N-2-氨基乙磺酸)缓冲液、PIPES(哌嗪-N,N′-双(2-乙磺酸))缓冲液以及N-三(羟甲基)甲氨酸-2-羟基丙磺酸等。
[1]US4169950
[2]CN201780009779.5用于制备细胞结合剂-细胞毒性剂缀合物的有效方法
2-哌嗪甲醇二盐酸盐是一种医药中间体,可用于制备PARP抑制剂。PARP-1是PARP酶家族的成员,该酶家族包括PARP-1、PARP-2、PARP-3和Vault-PARP等。PARP在DNA链断裂的修复中起着重要作用,因此抑制PARP是一种常用的癌症治疗方法。特别是在与DNA损伤治疗结合使用时,如电离辐射、甲基化试剂、拓扑异构酶I抑制剂以及其他化学治疗剂如顺铂和博来霉素等,PARP抑制剂表现出特别高效的治疗效果。

2-哌嗪甲醇二盐酸盐可用于制备一种PARP抑制剂,该化合物的结构为6-[3-(羟甲基)-4-[3-(4-氧代-3H-喹唑啉-2-基)丙酰基]哌嗪-1-基]吡啶-3-甲腈。

制备方法如下:
将2-哌嗪甲醇二盐酸盐(100mg,0.53mmol)溶解在DMSO(3mL)中,室温下加入6-氯吡啶-3-甲腈(88mg,0.63mmol)、K2CO3(146mg,1.062mmol)和Cu(MeCN)4PF6(3.9mg,0.01mmol)。将反应混合物在140℃下加热12小时,直到TLC显示起始物完全消耗。然后用水(10mL)淬灭反应并用EtOAc(3x 10mL)萃取。将合并的有机萃取物经过Na2SO4干燥,减压浓缩得到粗残余物,通过柱色谱纯化(100-200硅胶,5g,5%MeOH-DCM)得到白色固体状的6-[3-(羟甲基)哌嗪-1-基]吡啶-3-甲腈盐酸盐(50mg,32%)。LCMS:m/z:219[M+H]+。
将6-[3-(羟甲基)哌嗪-1-基]吡啶-3-甲腈盐酸盐(120mg,0.55mmol)和3-(4-氧代-3H-喹唑啉-2-基)丙酸(120mg,0.55mmol)溶解在干燥DMF(2mL)中,室温下加入EDC·HCl(157mg,0.825mmol)、HOBt(113mg,0.825mmol)和DIPEA(0.2mL,1.1mmol),并搅拌反应16小时,直到TLC显示起始物完全消耗。然后用冷水(20mL)淬灭反应并用EtOAc(3x 10mL)萃取。将合并的有机萃取物经过Na2SO4干燥,减压浓缩得到残余物,通过制备型HPLC纯化得到白色固体状的6-[3-(羟甲基)-4-[3-(4-氧代-3H-喹唑啉-2-基)丙酰基]哌嗪-1-基]吡啶-3-甲腈(26mg,11%)。
[1] [中国发明] CN201780082024.8 聚-ADP核糖聚合酶(PARP)抑制剂
引言:
莫吉司坦作为一种非麻醉性镇咳药物,具有广泛的临床应用。它在缓解各种刺激引起的咳嗽和气道炎症方面展现了显著效果。
简介:
莫吉司坦(Moguisteine),化学名为3-[2-(乙氧羰基)乙酰基]-2-(2-甲氧基苯氧甲基)噻唑烷,1984年由瑞士ROCH公司开发,2004年在意大利批准上市。莫吉司坦作为一种外周性非麻醉性镇咳药物,适用于有咳嗽症状的呼吸系统疾病患者。在一项小型双盲、随机对照试验中,与安慰剂相比,每天服用 3 次 200 mg 莫吉司坦混悬液可显着降低 COPD 患者的咳嗽频率。它还在小型试验中进行了研究,与可待因和右美沙芬相比,与两者具有相似的疗效。它尚未被批准在美国使用。莫吉司坦的合成工艺如下:
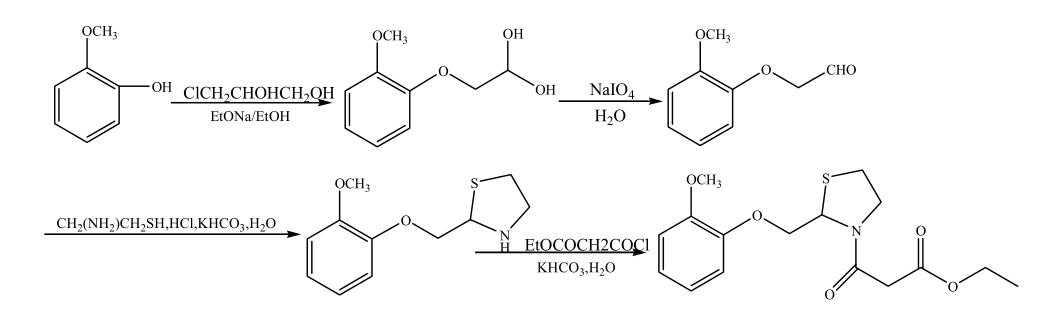
1. 莫吉司坦的用途
咳嗽是一种保护性机制,是许多呼吸系统疾病的重要症状。当咳嗽只是一种令人烦恼的反射,而不能起到清除痰液的作用,导致患者疲劳或衰竭,加重病理状态时,可能需要使用止咳药物。
莫吉司坦主要用于医疗领域,因为它能有效控制呼吸系统疾病。其核心应用在于治疗呼吸系统疾病,可作为强效止咳药。通过针对咳嗽的根本原因,莫吉司坦可缓解各种呼吸系统疾病引起的不适和刺激。这使其成为治疗慢性阻塞性肺病 (COPD) 和其他以持续咳嗽为特征的呼吸系统疾病的有效工具。除了在呼吸护理中已确立的作用外,莫吉司坦还在其他领域展现出潜在益处。虽然研究仍在进行中,但初步研究表明它可能具有其他治疗特性。然而,必须注意的是,这些潜在应用需要进一步研究和临床验证,才能得出明确结论。
2. 莫吉司坦的物理性质
莫吉司坦是一种乙酰胆碱拮抗剂,作为外周性非麻醉性镇咳药物,它不影响中枢神经系统且不具有成瘾性。莫吉司坦可以缓解由各种刺激引起的豚鼠气道炎症。大量动物实验结果表明,该药具有显著的镇咳效果,其机制并不涉及阿片受体,而是由纳络酮所决定。此外,经过动物和人体实验验证,莫吉司坦被证明是非常安全且有效的,其活性水平与可待因和右旋吗啡相当,但高于羟丙哌嗪。
莫吉司坦在动物和人类体内被快速代谢为相应的羧酸-2-[(2-甲氧基苯氧基)甲基]-β-氧代-1,3-四氢噻唑-3-丙酸,并部分地氧化成亚砜类的非对应异构体2-[(2-甲氧基苯氧基)甲基]-β-氧代-1,3-四氢噻唑-3-丙酸-1-氧化物。仅仅在鼠类体内有少量的 2-[(2-羟基苯氧基)甲基]-β-氧代-1,3-四氢噻唑-3-丙酸,2-[(2-甲氧基苯氧基)甲基]-β-氧代-1,-四氢噻唑-3-丙酸的苯酚的衍生物的混合物。所有的这些羧酸对于咳嗽在化学模式上显示出相似的活性,然而在对 2-[(2-甲氧基苯氧基)甲基]-β-氧代-1,3-四氢噻唑-3-丙酸的电刺激测试中未显示出药理活性。乙基 2-[(2-甲氧基苯氧基)甲基]-α,α-双甲基-β-氧代-1,3-四氢噻唑-3-丙酸盐也被追踪到相应的止咳活性。
3. 莫吉司坦的疗效和安全性
莫吉司坦是在寻找噻唑烷类祛痰药时偶然发现的,当时有止咳作用的化合物,而莫吉司坦被选为该类药物中最有效、最安全的代表。
(1)报道一
R Barnabè等人进行了一项多中心、双盲、平行组研究,以比较新型镇咳药莫吉司坦(100 毫克,每日三次)与参考标准可待因(15 和 30 毫克,每日三次)的临床疗效。两种药物均口服两天。六个参与中心招募了 119 名患者(平均年龄 54 岁;61 名女性和 58 名男性),他们患有慢性、干咳或轻微咳痰,伴有各种呼吸系统疾病(包括慢性阻塞性肺病、呼吸道恶性肿瘤和肺纤维化)。研究结果为:莫吉司坦 100 毫克,每日三次是安全的,并且似乎具有与可待因 15-30 毫克,每日三次相似的镇咳作用。
(2)报道二
M. Del Donno等人评估了莫吉司坦(一种具有外周作用机制的新型止咳药)在 124 名因各种呼吸系统疾病而持续咳嗽的成年患者中的疗效和安全性。约 50% 的研究人群报告患有阻塞性慢性支气管炎,这是最常见的潜在诊断。研究人员在 7 个中心进行了一项随机单盲短期治疗试验,比较了莫吉司坦(3 剂 200 毫克,2 天)和右美沙芬(3 剂 30 毫克,2 天)。主要疗效变量是服用研究药物最后一剂后早晨 6 小时内录音带记录的咳嗽次数与基线 6 小时记录的咳嗽次数相比减少的百分比。患者主观评估的夜间和早晨咳嗽频率和咳嗽麻烦的视觉模拟量表 (VAS) 评分被视为次要疗效变量。通过常规临床实验室测试和不良事件监测评估安全性。
两种药物的服药后咳嗽次数减少的百分比接近 30%。两组的咳嗽频率和咳嗽麻烦的 VAS 评分均显着降低,治疗之间没有显着差异。 61 名服用莫吉司坦的患者中有 3 名报告了可能或很可能的药物相关不良事件(1 例胃灼热、1 例胃痛、1 例腹泻),63 名服用右美沙芬的患者中有 4 名报告了可能或很可能的药物相关不良事件(1 例鼻炎和白细胞计数轻微下降、1 例晕厥、1 例胃部不适、1 例腹泻)。只有 1 名患者在服用第一剂右美沙芬后出现晕厥,因此需要停止治疗。
结果表明,使用莫吉司坦治疗可迅速缓解咳嗽,耐受性良好,效果与右美沙芬一样好。
参考:
[1]黄剑,陈年根,钟霞. 莫吉司坦的合成工艺的改进 [J]. 海南医学院学报, 2011, 17 (08): 1015-1016+1020. DOI:10.13210/j.cnki.jhmu.2011.08.049.
[2]甘英健. 含异噁唑的甘草次酸酰胺衍生物和莫吉司坦的合成研究[D]. 天津大学, 2009.
[3]https://en.wikipedia.org/wiki/Moguisteine
[4]Del Donno M, Aversa C, Corsico R, et al. Efficacy and safety of moguisteine in comparison with dextromethorphan in patients with persistent cough[J]. Drug Investigation, 1994, 7: 93-100.
[5]Barnabe R, Berni F, Clini V, et al. The efficacy and safety of moguisteine in comparison with codeine phosphate in patients with chronic cough[J]. Monaldi archives for chest disease= Archivio Monaldi per le malattie del torace, 1995, 50(2): 93-97.
1,4-苯并二恶烷-2-羧酸是一种重要的多沙唑嗪类药物中间体,化学式为C11H10O4,分子量为206.19,熔点为196-198°C。目前国内外报道了几种合成1,4-苯并二恶烷-2-羧酸的方法,其中包括使用邻苯二酚和2,3-二溴丙腈作为原料,在碱性条件下进行分子间消去反应生成1,4-苯并二恶烷-2-甲腈,然后在酸性条件下水解生成1,4-苯并二恶烷-6-丙烯酸的方法。然而,这些方法使用的原料价格较高,且2-氯丙烯腈具有剧毒性,同时还会产生含溴含氯的副产物,对环境造成一定的污染。

1,4-苯并二恶烷-6-丙烯酸
1)将甘氨酸乙酯盐酸盐(28g,0.2mol)溶于30mL水中,加入100mL二氯乙烷,降温至-15℃,滴加亚硝酸钠(15.2g,0.22mol)溶于20mL水的溶液,滴加时间为30分钟。滴加完毕后,继续在-15℃下反应2小时。然后加入饱和碳酸钠溶液调至pH=6,静置分液,取有机相冷却待用,该有机相即为重氮乙酸乙酯的二氯乙烷溶液。
2)将1,2-亚甲二氧基苯(8.13g,0.067mol)溶于40mL二氯乙烷中,再加入氯化亚铜0.5g,加热至60℃,滴加步骤1)所得的重氮乙酸乙酯的二氯乙烷溶液(内含重氮乙酸乙酯0.14mol),滴加时间为6小时。滴加完毕后,继续在60℃下反应1小时,然后冷却至室温,脱溶剂二氯乙烷后,在30Pa下减压蒸馏收集100℃-110℃的馏分,即得到1,4-苯并二恶烷-6-丙烯酸乙酯。
3)将上述制备的全部1,4-苯并二恶烷-6-丙烯酸乙酯加入NaOH(8g,0.2mol)溶于50mL水的溶液中,升温至80℃进行水解反应2小时,然后用质量浓度为15%的盐酸溶液调至pH=6后过滤。将所得的棕黄色固体在乙醇(20mL)中重结晶后,得到白色固体--1,4-苯并二恶烷-6-丙烯酸(10.5g,熔点125-127℃),收率为87.1%。
[1] 顾文鑫, 武同兴, 陈小川, & 潘鑫复. (2001). (2r,3r)-和(2s,3s)-2-(4-羟基-3-甲氧基)-3-羟甲基-1,4-苯并二氧六环-6-醛的对映选择性合成. 高等学校化学学报, 022(001), 70-71.
[2] 孔小林, & 刘波. (1999). N-(1,4-苯并二恶烷-2-羰基)哌嗪盐酸合成方法的改进. 浙江化工, 30(1), 17-18.
[3] 孔卓. (2020). 2,3-二氢-1,4-苯并二氧六环基查尔酮衍生物的设计,合成及其抑制单胺氧化酶B的活性研究. (Doctoral dissertation, 遵义医科大学).