 1
1
硝酸氧锆是一种白色结晶粉末状的无机化合物,具有潮解性,并带强酸味。它易溶于水和乙醇,其水溶液呈酸性。在受热时,硝酸氧锆会分解,产生有毒的氮氧化物蒸汽。

图一 硝酸氧锆
按实验所需物质的量取一定量Pb(CH3COO)2及硝酸氧锆于烧瓶中,加入适量乙二醇于80°C回流0.5h,再按计量比加入Ti(O-n -C4H9)4 继续回流直至混合液变得澄清透明。一束白光通过液体时可产生明显 Tyndall 现象,说明已形成稳定溶胶。溶胶于选定温度下恒温干燥直至干凝胶形成。将干凝胶置于马弗炉中,以5°C/min 加热到350°C,恒温0.5h,使有机物彻底燃烧分解,然后以10°C/min 升温至450°C,恒温2h,即可得锆钛酸铅[Pb(ZrxTi1-x)O3,PZT]纳米晶[1]。
称取1.6g(0.04μM)氢氧化钠溶于15ml去离子水中,在溶液中加入步骤(1),反应0.5h,称取4.3g(0.01μM)硝酸盐溶于20ml去离子水中配制成溶液,加入酒石酸铜钠溶液,加热至70°C,反应3h,然后冷却、静置,将沉淀物与去离子水多次洗涤、过滤、干燥,可得到蓝黑色酒石酸铜锆双金属化合物4.6g,收率90.2%[2].
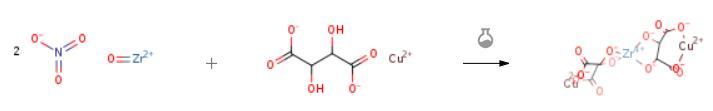
图二 硝酸氧锆的应用
将1克Leucas aspera叶提取物溶解在100毫升双蒸馏水中。将Sm2O3溶解在化学计量计算量为1:1的HNO3中,将其转化为硝酸氧锆。通过将过量硝酸放入80℃的砂浴中并使其蒸发以获得透明的硝酸钐溶液来去除过量硝酸。随后将LA叶提取物(10 ml)和硝酸锆水溶液加入圆柱形pyrex盘中的硝酸钐溶液中,用磁力搅拌器持续搅拌约10分钟。然后将其引入预热至450±10℃的炉中,溶液沸腾并脱水,然后分解金属硝酸盐。将所得产物研磨成细粉。制备不同掺杂浓度(3-11mol%)的纯NMs和ZrO2:Sm3+NMs[3].
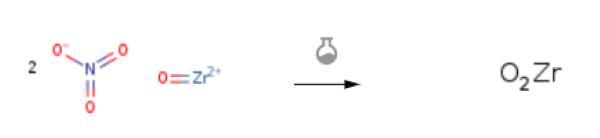
图三 硝酸氧锆的应用2
[1]刘大格,蔡伟,张洪喜,等.以硝酸氧锆为锆源溶胶-凝胶合成PZT纳米晶的研究[J].硅酸盐学报,1998,(03):41-46.
[2]汪营磊,赵凤起,高福磊,等.一种酒石酸铜锆化合物及其制备方法和应用[P].陕西省:CN201410379542.4,2017-01-18.
[3]Gurushantha K ,Anantharaju K ,Sharma S , et al.Bio-mediated Sm doped nano cubic zirconia: Photoluminescent, Judd–Ofelt analysis, electrochemical impedance spectroscopy and photocatalytic performance[J].Journal of Alloys and Compounds,2016,685761-773.