异氰酰乙酸乙酯(Ethyl isocyanatoacetate)是一种有机化合物,化学式为C5H7NO3。它属于羧酸酯类有机物,可以作为有机试剂使用。

图一 异氰酰乙酸乙酯
在惰性气氛下,将三乙胺(0.76 g, 7.5 mmol, 1.2 当量)加入到丙二酸乙酯(1.5 g, 6.25 mmol, 1.0 当量)的悬浮液中,然后缓慢加入二苯基磷酰叠氮(1.90 g, 6.87 mmol, 1.1 当量)。反应混合物在室温下搅拌15 min,加热至80℃1h,观察氮气的析出情况。溶剂在减压下被除去。采用下列方法提取异氰酰乙酸乙酯。残渣在己烷(10 mL/mmol)中搅拌,收集上清。己烷提取重复2次。结合己烷层蒸发得到粗异氰酸酯,无需进一步提纯[1].

图二 异氰酰乙酸乙酯的合成
取1L干净的三口烧瓶,先后加入15-20g二(三氯甲基)碳酸酯和约200ml二氯甲烷液体,搅拌至溶解,在氮气保护下冷却至-18℃,缓慢滴加15 -35g甘氨酸乙酯盐的溶液,配制成55-65g三乙胺和600ml二氯甲烷。这个循序渐进的添加过程大约需要0.5h。滴加后,将三颈烧瓶置于低温浴中。将三颈烧瓶内温度控制在0-5℃,保持反应0.5h,取样检查原料反应是否完全,反应完全后,滴加(二甲胺)苯基]胺和200ml二氯甲烷液体。滴加过程耗时约0.25h。此时将三颈烧瓶从低温浴中取出,缓慢升高至室温,在室温下进行16h的反应,取样检测原料的反应是否结束;将得到的反应溶液过滤得到相应的滤液,减压浓缩,然后用5%的稀盐酸调节pH值为1;用20ml乙酸乙酯提取浓缩液,重复三次,所得水相用5%氢氧化钠溶液中和,pH值为6;然后用20ml二氯甲烷进行萃取,此步骤重复三次;在干燥有机相并减压浓缩,得到15-20g的无色液体异氰酰乙酸乙酯[2].
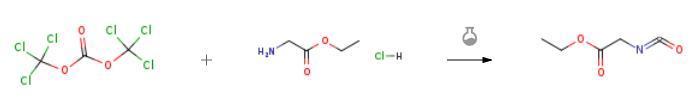
图三 异氰酰乙酸乙酯的合成2
[1]Kondaskar A ,Kondaskar S ,Fishbein C J , et al.Structure-based drug design and potent anti-cancer activity of tricyclic 5:7:5-fused diimidazo[4,5- d :4′,5′- f ][1,3]diazepines[J].Bioorganic & Medicinal Chemistry,2013,21(3):618-631.
[2]陆林林.一种N-(羧甲基氨基羰基)-4,4′-双(二甲氨基)二苯胺钠盐的制备方法[P].江苏省:CN202011605405.X,2022-07-01.
2023年2月1日,FDA比准葛兰素史克公司(GSK)开发的达普司他(daprodustat)用于接受透析至少4个月的成人慢性肾病(CKD)引起的贫血。Daprodustat的商品名为Jesduvroq,为口服片剂,包含5种剂量:1、2、4、6、8mg。它的中文化学名称:N-[(1,3-二环己基六氢-2,4,6-三氧代-5-密啶基)羰基]甘氨酸,英文化学名称:N-[(1,3-dicyclohexyl-2,4,6-trioxohexahydropyrimidin-5-y)carbonyl]-glycine,分子式为C19H27N306。

图一 达普司他
文献报道了达普司他的合成路线:先由N,N-二环己基碳二亚胺和丙二酸环合生成中间体1,3-双环己基巴比妥酸,或在酸性条件下由N,N-二环己脲与丙二酰氯或丙二酸环合得到,然后在碱性条件下与异氰酰乙酸乙酯经偶联反应得到中间体达普司他乙酯,最后在碱性条件下经酯水解反应生成达普司他(daprodustat)。合成路线如图二所示[1]。

图二 达普司他的合成
达普司他是一种新型的口服脯氨酰羟化酶抑制剂(HIF-PHl)类药物,适用于接受透析至少4个月的成年人(未被比准用于未接受透析患者)。在一项2964名接受透析的成年人的随机研究中,患者接受口服Jesduvroq或注射重组人促红细胞生成素(慢性肾脏病所致贫血患者的标准护理治疗),数据结果显示,Jesduvroq将血红蛋白(红细胞中携带氧气的蛋白质,是衡量贫血的常用指标)提高并维持在100~110gL的目标范围内,与重组人促红细胞生成素的水平相似[1]。
达普司他作为一种药物,在临床使用中可能会产生一些不良反应。根据报道,最常见的不良反应包括高血压、血栓性血管事件、腹痛、头晕以及过敏反应。患者在使用时应密切监测这些症状,并在出现严重反应时及时就医。医生在开具此药时也应评估患者的风险因素,并在必要时调整治疗方案。
[1]秦望智,赵临襄.达普司他(Daprodustat,Jesduvroq)[J/OL].中国药物化学杂志,1[2024-07-23].
3-乙酰基-5-氯噻吩-2-磺酰胺是制备布林佐胺的中间体,布林佐胺是一种新型的局部碳酸酐酶抑制剂,具有高度的选择性和亲和力,并且明显地抑制碳酸酐酶的活性,有效的降低眼压。布林佐胺半衰期较长,对眼部刺激较小,其生理性pH值和混悬液设计使滴眼舒适,耐受性和安全性良好,不良反应较小(通常情况下无需治疗就可以自行缓解),是一种非常有价值的抗青光眼新药。

首先,在5L四口瓶中加入210g3-乙酰基-5-氯-2-(苄基巯基)噻吩,1500g乙腈,搅拌,然后加入320g冰乙酸和200g水,控制温度在0-15℃之间。分批加入241.6g三氯异氰脲酸,约30分钟加完,保持0-15℃温度进行反应,使用TLC监控反应进程直到原料消失。
接下来,将反应混合物水浴加热至35~45℃,然后进行减压浓缩除去溶剂。加入1500g25%乙酸乙酯石油醚溶液,搅拌后过滤。将滤液减压蒸干,得到182.7g淡黄色油状物,即为3-乙酰基-5-氯-2-噻吩磺酰氯。
将上述磺酰氯用105g乙酸乙酯稀释,控温0~15℃,滴加到420g氨水中,搅拌反应至磺酰氯消失,降温至0℃左右,搅拌析晶1小时。过滤,少量水泡洗,所得固体40℃烘干,得到类白色的3-乙酰基-5-氯噻吩-2-磺酰胺162.4g,收率为91.2%。HPLC纯度大于99%。
[1]CN201410236731.6布林佐胺中间体噻吩磺酰胺的制备方法
氯化异氰盐酸盐是一种常用医药中间体,可以用于合成各种药物和生物活性化合物。它在有机合成和药物合成中具有重要的应用价值。氯化异氰盐酸盐可以发生多种反应,如水解、醇解、氨(胺)解、与有机金属试剂反应、还原反应和氢卤化等。它是最活泼的酰基化试剂之一,可以提高一些羧酸的反应活性和产率。氯化异氰盐酸盐广泛用于合成多种药物和生物活性化合物。
制备氯化异氰盐酸盐常用的方法有二氯亚砜、三氯化磷、五氯化磷和三光气等。本文以异烟酸为起始物料,通过与二氯亚砜反应制备氯化异氰盐酸盐。

图1 氯化异氰盐酸盐的合成反应式
将异烟酸、过量氯化亚砜及甲醇加入到反应瓶中,在70℃回流反应10 h。反应后反应液转变为黄色清液,常压下去掉多余的氯化亚砜,黄色清液变稠成为黄色粘稠液体。经萃取,重结晶,真空干燥12 h后,即得氯化异氰盐酸盐。
氯化异氰盐酸盐在水中溶解度很小,乙酸乙酯、石油醚、丙酮、醇等是氯化异氰盐酸盐的优良溶剂。实验选择甲醇为溶剂,可在室温、碱性条件下能很快将氯化异氰盐酸盐溶解,其中卤素以离子的形式存在。
氯化异氰盐酸盐对水是稍微有危害的,不要让未稀释或大量的产品接触地下水、水道或者污水系统,若无政府许可,勿将材料排入周围环境,常规情况下不会分解,没有危险反应。密封、阴凉、干燥保存。
[1]Chen, Fengjin; Guo, Jinbao; Qu, Zhijian; Wei, Jie Journal of Materials Chemistry, 2011 , vol. 21, # 24 p. 8574 - 8582.
2-氨基噻唑类化合物是有机药物化学中重要的一类杂环化合物,具有广泛的生物活性。噻唑类化合物可用作局麻药,具有抗惊厥、抗病毒、抗菌和杀虫等作用。本文介绍了制备8-溴-[1,2,4]噻唑并[1,5-A]吡啶-2-胺的方法。
目前制备8-溴-[1,2,4]噻唑并[1,5-A]吡啶-2-胺的方法包括:
本文以2-氨基-3-溴吡啶及异硫氰酰甲酸乙酯为起始物料,经环合吡啶环制备目标化合物8-溴-[1,2,4]噻唑并[1,5-A]吡啶-2-胺。具体的合成反应式请参见下图:

图1 8-溴-[1,2,4]噻唑并[1,5-A]吡啶-2-胺的合成反应式
以下是三种制备方法的具体步骤:
方法一:
向三口烧瓶中加入2-氨基-3-溴吡啶及 DMF 的混合溶液及乙醇 50 mL,在搅拌条件下,缓慢加入异硫氰酰甲酸乙酯及无水醋酸钠,搅拌至溶解,升温至 20 ℃,反应 7 h,反应结束后抽滤,用少量乙醇洗涤滤饼,得到产物8-溴-[1,2,4]噻唑并[1,5-A]吡啶-2-胺。
方法二:
将异硫氰酰甲酸乙酯和2-氨基-3-溴吡啶混合,搅拌下在195 w微波辐射反应40 s后接着130 w反应5 分钟。反应完毕加热水200mL,趁热过滤,滤液用碳酸钠水溶液处理,得黄色固体,冷却减压过滤,滤饼用盐酸水溶液及蒸馏水洗涤两次,真空干燥后得目标化合物8-溴-[1,2,4]噻唑并[1,5-A]吡啶-2-胺。
方法三:
将0.05 mol2-氨基-3-溴吡啶、100 mL乙酸乙酯和100 mL氯仿混合,回流搅拌反应3 h。过滤,向滤液中加入异硫氰酰甲酸乙酯,继续回流反应3 h。冷却析晶,抽滤,干燥,得化合物8-溴-[1,2,4]噻唑并[1,5-A]吡啶-2-胺。
[1] Dorsey, Bruce D. Journal of Medicinal Chemistry, 2012 , vol. 55, # 11 p. 5243 - 5254
2-氰基-5-氟溴苄是一种有机化合物,常被用作有机合成的起始物或中间体,在药物合成、农药合成等领域具有一定的应用。

图一 2-氰基-5-氟溴苄
合成的具体步骤为:将1.35 g 2-甲基-4-氟苯腈(10mmol)溶于20 mL四氯化碳中,加入0.25g对甲苯磺酸(0.015 mmol)和2.15g N-溴琥珀酰亚胺(NBS)(12mmol)。加热4小时后反应完成,然后冷却至室温,过滤,加入20mL饱和氯化铵溶液,得到层。有机层依次用水和饱和氯化钠水溶液(20 mL*3)洗涤澄清,用无水硫酸钠干燥,过滤,减压蒸去溶剂,所得粗品经柱层析纯化(石油醚:乙酸乙酯=3:1),得2-溴甲基-4-氟苯腈(收率86%)。将2-溴甲基-4-氟苯腈(1.0mmol)和对甲苯胺(1.2mmol)溶于50mL四氢呋喃中,搅拌加热至60°C回流,分份加入0.2g乙醇钠(3.0mmol),再回流8小时。经TLC监测确认反应完成后,将反应物冷却至室温,浓缩,加入20mL乙酸乙酯,用水和饱和氯化钠溶液(20mL*3)依次洗涤澄清,用无水硫酸钠干燥,过滤,减压蒸发除去溶剂。所得粗产物经柱层析纯化(石油醚:乙酸乙酯=10:1),得到中间化合物2-氰基-5-氟溴苄(收率95%)[1]。

图二 2-氰基-5-氟溴苄的合成1
第二种合成方法分为两步,第一步是1-溴-4-氟-甲苯在N,N-二甲基甲酰胺回流24h,接着,第二步,与N-溴代琥珀酰亚胺、2,2'-偶氮二(异丁腈)在四氯化碳中反应2h,全程为惰性氛围[2]。

图三 2-氰基-5-氟溴苄的合成2
[1]Xinbei J,Jiali T,Yixuan W, et al. 2-((4-Arylpiperazin-1-yl)methyl)benzonitrile Derivatives as Orally Available Inhibitors of HCV With a Novel Mechanism of Action.[J]. Journal of medicinal chemistry,2020,63(11).
[2]Zhiyuan Z,B M W,Jun F, et al. Design and synthesis of pyrimidinone and pyrimidinedione inhibitors of dipeptidyl peptidase IV.[J]. Journal of medicinal chemistry,2011,54(2).
肌氨酸乙酯盐酸盐(Ethyl sarcosinate hydrochloride),分子式C5H12ClNO2,对水体有危害。外观为白色针状结晶或粉末。

图一 肌氨酸乙酯盐酸盐
称取5?氟?2?硝基苯甲酸(1.0g,5.4mmol,CAS No.320?98?9;安耐吉化学)、1?乙 基?(3?二甲基氨基丙基)碳酰二亚胺盐酸盐(1.2g,6.5mmol;EDCI,CAS No.:25952?53?8,安 耐吉化学)、1?羟基苯并三唑(0.87g,6.5mmol;CAS No:2592?95?2,安耐吉化学)置于反应瓶 (100mL),加入二氯甲烷(20mL)搅拌溶解,室温活化30min;另分别称取肌氨酸甲酯盐酸盐 (0.75g,5.4mmol,CAS No.13515?93?0,安耐吉化学)、三乙胺(1.0g,10.8mmol,国药集团)溶 于二氯甲烷(10mL)后,依次加入到反应瓶中,室温反应12h。以水/二氯甲烷(v:v=1:1,50ml×2)淬灭反应液,合并有机相,以无水硫酸 钠干燥后减压浓缩得棕色黄色油状物a;将a经硅胶柱层析,以二氯甲烷/乙酸乙酯(v:v=8: 1)为洗脱液,分得淡黄色油状物b;将油状物b溶于乙酸乙酯/石油醚(4mL,v:v=1:3,)混合 溶液,超声处理30min,有大量后固体析出,抽滤,得淡黄色固体约1.1g,收率为85.4%。称取7?氟?3,4?二氢?4?甲基?1H?[1,4]苯并二氮卓?2,5?二酮(2.0g,9.6mmol)、五 氯化磷(2.4g,11.5mmol)置于反应瓶(50mL),加入N,N?二甲基甲酰胺(0.2mL)和四氢呋喃 (20mL),70℃回流5h。反应液旋转蒸发浓缩近干,得糖浆状物,称重2.15g,收率为95%,称取碳酸铯(4.7g,14mmol)置于反应瓶(50mL),加入四氢呋喃(20mL)搅拌使溶解, 再加入异氰基乙酸乙酯(1.3g,11.5mmol;CAS No 2999?46?4)。冰水浴使体系温度降至0℃。 将步骤(3)所得2.15g糖浆状物溶于四氢呋喃(10mL),滴加入反应瓶,30分钟加入完毕,然后 室温反应4h。减压浓缩得棕色油状物,将此油状物以乙腈溶解,经0.24um滤膜过滤处理后高效液相法分析,收率为30.5%[1]。
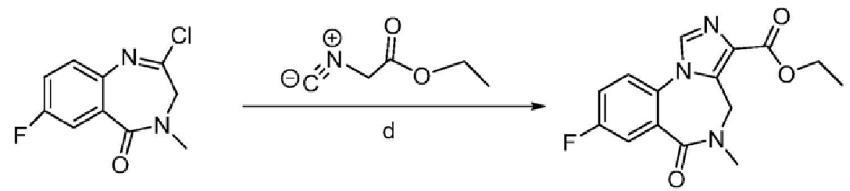
图二 肌氨酸乙酯盐酸盐制备氟马西尼
[1]何新华,张学敏,周涛等. 一种氟马西尼的制备方法[P]. 浙江省:CN112979658B,2022-05-31.
一、郭晓川研究了以异腈基乙酸甲酯和1-萘甲酰氯为原料合成了5-(萘基-1)嗯唑-4-羧酸甲酯,继续对5-(萘基-1)嗯唑-4-碳酰肼直接肼解得到5-(萘基-1)嗯唑-4-碳酰肼,然后引入不同的醛类,合成了三种性能优秀的荧光探针。这些探针在合成、选择性、灵敏性以及功能性等方面都具有独特的优势,在不同pH环境中都可以识别目标离子,同一个荧光探针在不同体系中表现出不同的光学现象,如荧光增强、荧光淬灭、发射波长红移等。其操作如下:第一步,异腈基乙酸甲酯(0.41g,4.0mmol)溶于5mL四氢呋喃(THF),加入三乙胺(1.23g,12.2mmol)搅拌均匀,1-萘甲酰氯(0.762g,4.0mmol)溶于5mL THF慢慢滴加进上述混合液中,室温搅拌48小时后,旋蒸除去THF,加30mL三氯甲烷溶解,用稀Na2CO3溶液洗涤,水洗、干燥、萃取出油相进行减压蒸馏除去三氯甲烷,得到5-(萘基-1)嗯唑-4-羧酸甲酯,未纯化直接用于下一步反应。第二步,上步产物溶解在20mL乙醇中,加入6mL 80%的水合肼加热回流6小时,降温后析出白色固体,反应结束后过滤得到5-(萘基-1)嗯唑-4-碳酰肼(0.6g,产率60.0%)。
二、2-咪唑啉结构存在于许多重要的活性天然产物中,并且广泛应用于生物活性二氨基酸衍生物的制备,因此,对于2-咪唑啉衍生物的制备具有重要意义。异氰基羧酸酯和亚胺不对称Mannich反应是获得2-咪唑啉化合物的重要方法。1996年,Hayashi等报道了金属催化异腈基乙酸甲酯与N-Ts芳香酰亚胺的不对称Mannich反应,以>99: 10dr的非对映选择性得到了cis构型的主产物。2010年,Lu等首次报道了有机催化的异腈基乙酸甲酯与N-Ts芳香醛亚胺的不对称Mannich反应,以最高70%ee(对映体过量值)的对映选择性得到trans-构型的2-咪唑啉。目前,有机催化该类反应获得光学活性2-咪唑啉的报道很少,2012年,Nakamura报道了手性硫脲衍生物有机催化异氰基乙酸甲磺酰酯与N-2-世啶磺酰基亚胺的不对称Mannich反应,得到了最高达96%ee对映选择性。
王黎明等人在有机催化异腈基乙酸甲酯与芳香醛亚胺的不对称Mannich反应中,介绍了一种通用型合成方法,操作如下:于5mL圆底烧瓶中依次加入异腈基乙酸甲酯(0.22mmol)、催化剂(0.02mmol)、不同取代苯甲醛亚胺(0.20mmol)、分子筛(200mg)和甲苯(0.5mL),室温搅拌反应24h,薄层色谱(TLC)监测。反应结束后,经硅胶柱层析分离,V(正己烷):V(乙酸乙酯)=12:1洗脱,得到不对称Mannich反应的油状产品3a-3k。
[1]郭晓川. 具萘噁唑羧酸衍生物的合成及性质[D]. 山东:济南大学,2022.
[2]王黎明,穆宏文,卢栋泽,等. 有机催化异氰基乙酸甲酯与芳香醛亚胺的不对称Mannich反应[J]. 应用化学,2019,36(7):758-763. DOI:10.11944/j.issn.1000-0518.2019.07.180340.
本文章旨在探讨使用2-氟-3-三氟甲基苯胺合成普克鲁胺的方法。文章将深入研究该合成路线,以期为相关化合物的高效制备提供可行的解决方案。
背景:普克鲁胺(Proxalutamide)是新一代雄激素受体(AR)拮抗剂,是基于美国上市新药恩杂鲁胺(Enzalutamide)的核心结构,采用计算机辅助设计并优化得到的新型化合物,针对转移性趋势抵抗前列腺癌(PCA)和转移性乳腺癌(MBC)显示出了较好的治疗效果,目前正在开展3期临床研究。2019年新型冠状病毒肺炎(COVID-19)发生后,科学家将其应用于新型冠状病毒肺炎的治疗,相关研究表明其效果优异且安全性良好,能有效降低新型冠状病毒肺炎患者的住院率和死亡率,目前正在巴西、中国、美国开展临床3期研究,2021年7月获得巴拉圭紧急使用授权用于新型冠状病毒肺炎住院患者的治疗。
2-氟-3-三氟甲基苯胺(1)是合成普克鲁胺的重要中间体。
应用:合成普克鲁胺。

(1)4-溴-2-氟-3-三氟甲基苯胺(12)的合成
在100 mL圆底烧瓶中将2-氟-3-三氟甲基苯胺(11)(2.00 g, 11.17 mmol)溶于DMF(14 mL)中,并在15 ℃条件下分次加入N-溴代琥珀酰亚胺(NBS, 1.99 g, 11.1 7 mmol)),保温反应时间1 h。反应混合物用乙酸乙酯(EtOAc, 50 mL)稀释,并用水(2×50 mL)和饱和NaCl溶液(50 mL)洗涤。分离出的有机相用Na2SO4干燥、浓缩得到化合物粗品。柱层析纯化分离(洗脱剂:石油醚 ∶乙酸乙酯=10 ∶1, V ∶V)得到化合物12 2.74 g, 收率95.0%。
(2)N-[4-溴-2-氟-3-(三氟甲基)苯基]乙酰胺(13)的合成
向100 mL圆底烧瓶中加入化合物12(2.45 g, 9.5 mmol))和乙酸酐(6 mL)的混合物,并在25 ℃条件下搅拌反应3 h, 减压蒸馏除去剩余乙酸酐。残留物加入冰水(10.00 g)和碳酸氢钠(pH=7)。用乙酸乙酯(3×30 mL)萃取混合物,合并有机相,Na2SO4干燥,过滤、浓缩得到化合物13 2.52 g, 收率88.0%。
(3)N-[4-氰基-2-氟-3-(三氟甲基)苯基]乙酰胺(14)的合成
在100 mL圆底烧瓶中将化合物13(2.40 g, 8 mmol)与CuCN(1.07 g, 12 mmol, 1.5 eq)混合后加至DMF(10 mL),氮气保护,145 ℃条件下回流反应12 h。反应混合物冷却至室温,倒入冰水(25 mL),过滤出不溶性固体,加入乙酸乙酯(3×10 mL)洗涤滤饼。有机层分离后,水层用乙酸乙酯(50 mL)萃取。混合提取物用饱和NaHCO3溶液(2×50 mL)和盐水(3×50 mL)洗涤,Na2SO4干燥,过滤后真空浓缩。残留物用柱层析(洗脱剂:石油醚 ∶乙酸乙酯=4 ∶1, V ∶V)纯化,得到黄色固体化合物14 1.50 g, 收率76.0%, m.p.215~217 ℃。
(4)4-氨基-3-氟-2-(三氟甲基)苯甲腈(15)的合成
向100 mL圆底烧瓶中依次加入化合物14(0.70 g, 2.84 mmol)的乙醇(5 mL)溶液和浓盐酸(12 mol/L, 5 mL)。将混合物溶液在78 ℃条件下回流反应1 h, 冷却至室温,真空浓缩,所得固体溶于乙酸乙酯(25 mL),用饱和碳酸氢钠溶液(25 mL)洗涤,无水MgSO4干燥,过滤、浓缩后得到淡灰色固体化合物15 0.54 g, 收率93.0%, m.p.160~162 ℃。
(5)3-氟-4-异硫氰酸根-2-三氟甲基苯甲腈(16)的合成
在100 mL圆底烧瓶中将化合物15(0.41 g, 2 mmol)溶于四氢呋喃(THF, 5 mL),并在20 ℃条件下缓慢加入硫光气(2 mL)水(5 mL)溶液。混合物搅拌反应1 h后浓缩。残留物在水(50 mL)和乙酸乙酯(30 mL)之间分配。水相用乙酸乙酯(2×30 mL)萃取,合并有机相,用盐水(2×50 mL)洗涤,无水MgSO4干燥,过滤、浓缩,得到黄色油状液体化合物16 0.40 g, 收率73.0%。
参考文献:
[1]刘双双,侯静,王娟等. 普克鲁胺中间体3-氟-4-异硫氰酸根-2-三氟甲基苯甲腈的合成 [J]. 合成化学, 2023, 31 (08): 624-629. DOI:10.15952/j.cnki.cjsc.1005-1511.22125
[2]杨东,刘辉,何立. 2-氟-3-三氟甲基苯胺的合成研究 [J]. 有机氟工业, 2022, (03): 17-21.
[3]戴稼盛. 烟草抑芽剂氟节胺的研究[D]. 浙江大学, 2002.
4-碘-5-甲基异恶唑是一种常用的医药合成中间体。当接触到4-碘-5-甲基异恶唑时,应采取相应的应对措施,如将患者移到新鲜空气处、脱去污染的衣着并用肥皂水和清水冲洗皮肤、分开眼睑并用流动清水或生理盐水冲洗眼睛、漱口并禁止催吐等。如果出现不适感,应立即就医。
4-碘-5-甲基异恶唑可用于制备2-(3,4-二氟苯基)-3-(3-氟苯基)-5-(5-甲基-1,2-噁唑-4-基)-5-氧代戊腈。制备方法如下:
1)在一个干燥的、充满氩气的Schlenk管中,向THF(5ml)中加入镁屑、氯化锌和氯化铝,然后通过添加DIBAL-H活化。将4-碘-5-甲基异恶唑逐滴加入无水THF(3ml)中,然后在25°C下搅拌30分钟。随后,与酰基氯进一步反应。
2)将亚硫酰氯加入4-氰基-4-(3,4-二氟苯基)-3-(3-氟苯基)丁酸中,然后在80°C下搅拌1.5小时。在减压下移除过量的亚硫酰氯。将反应混合物溶于二氯甲烷中,然后逐滴加入上述粗溶液,随后在25°C下搅拌2小时。在减压下移除溶剂,用乙酸乙酯洗涤剩余物,然后用硅胶进行色谱分析,得到2-(3,4-二氟苯基)-3-(3-氟苯基)-5-(5-甲基-1,2-噁唑-4-基)-5-氧代戊腈的非对映异构体混合物。
[1]CN201280039621.X2,3-二苯基戊腈衍生物、其制备方法及其作为除草剂和植物生长调节剂的用途