1-烯丙基环丙磺酰氯是一种有机中间体,可用于酰化反应,常用于制备磺酰胺产物。有文献报道1-烯丙基环丙磺酰氯可用于制备MEK抑制剂如1-烯丙基-N-(2-(2-氟-4-碘-苯基氨基)-1,5-二甲基-6-氧代-1,6-二氢吡啶-3-基)环丙烷磺酰胺。

将环丙烷磺酰氯溶于过量的n-BuOH并将反应混合物冷却至0℃,随后滴加吡啶。将该混合物加热并搅拌36小时。减压除去溶剂,并将所得固体溶于氯仿。用水、盐水清洗有机相,干燥后浓缩获得产物。
在低温下,向1-丁基环丙烷磺酸酯的THF溶液中缓慢添加丁基锂。搅拌后,添加烯丙基碘化物的THF。反应混合物在低温下搅拌,并在室温下继续搅拌。减压蒸发挥发物,并使用二氯甲烷萃取残留物。用水清洗萃取物,干燥后除去溶剂。通过硅胶柱层析纯化残留物,获得无色油状产物。
将含1-烯丙基环丙烷-1-磺酸丁酯和硫氰酸钾的二甲醚和水混合物加热回流过夜。用乙酸乙酯萃取混合物,并减压蒸发水相,得到粗产物。
将1-烯丙基环丙烷-1-磺酸钾溶液、亚硫酰氯和DMF溶液加热回流。减压蒸发挥发物,并缓慢添加水。用乙酸乙酯萃取混合物,用MgSO4干燥,过滤并减压浓缩。通过硅胶层析纯化残留物,获得产物。
[1] [中国发明] CN200910146822.X 6-芳氨基吡啶酮磺酰胺和6-芳氨基吡嗪酮磺酰胺MEK抑制剂
N-甲基磺酰胺是一种广泛应用于合成天然产物、精细化学品、医药品和关键性中间体的化合物。它在瑞舒伐他汀钙等高血脂症药物的合成中扮演着重要角色。瑞舒伐他汀钙是一种选择性HMG-CoA还原酶抑制剂,已在多个国家和地区上市。那么,如何制备N-甲基磺酰胺呢?

一种制备N-甲基磺酰胺的方法是将环丙烷磺酰胺、铱催化剂、氢氧化钾、甲醇和水加入反应容器中,在适当温度下反应一段时间后,通过柱层析得到纯净的目标化合物。
另一种制备N-甲基磺酰胺的方法是将1,2-二氯乙烷和甲基磺酰氯在适当条件下反应,经过一系列步骤得到成品。
一种瑞苏伐他汀钙的制备方法是通过多步反应将起始原料与N-甲基甲磺酰胺缩合,经过一系列步骤得到瑞苏伐他汀钙。该方法具有收率稳定、试剂价格便宜、易于操作等优点。
一种Naratriptan的制备方法是以5-卤代吲哚为起始原料,经过氰化、还原、与N-甲基甲磺酰胺缩合、加氢还原、与N-甲基哌啶酮缩合、再加氢还原等反应得到目标化合物。该方法克服了现有技术中存在的原料制备困难及操作成本过高的缺陷。
[1] 中国发明CN201810966947.6一种在水中合成N-甲基磺酰胺的方法
[2] CN201010146333.7一种制备瑞苏伐他汀钙的方法
[3] CN200410093115.6制备N-甲基-3-(1-甲基-4-哌啶基)-1,4-吲哚-5-乙硫胺的改进法
[4] 王强.N-甲基甲磺酰胺的合成研究[J].广州化工,2013,41(20):80-81+161.
环丙基甲酰氯是一种无色或浅黄色液体,具有较强的吸湿性。它可用作有机合成与医药及农药中间体,常用于基础化学研究和药物分子的合成,例如农药分子植物生长调节剂抗倒酯的合成中间体。
为了避免环丙基甲酰氯的水解,需要在处理和储存时避免接触水分,并将其保存在干燥的环境中。此外,环丙基甲酰氯在光照条件下相对不稳定,容易发生分解反应。因此,在进行光化学反应时,需要使用具有足够紫外光抵抗能力的器皿,如石英玻璃反应器,并在进行反应前避免暴露于强光下。

图1 环丙基甲酰氯的合成路线
环丙基甲酰氯的合成方法是将二氯化硫(3.0当量)加入环丙烷羧酸(1.5当量)在干燥的二氯甲烷(0.5M)中的溶液中。然后将所得的反应混合物加热至回流并在回流状态下持续搅拌反应6小时。在减压下浓缩该混合物,以除去剩余的二氯化硫,即可获得产品。
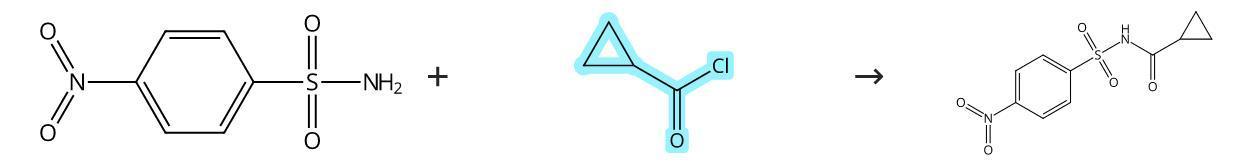
图2 环丙基甲酰氯的应用
环丙基甲酰氯的应用之一是在室温下与4-硝基苯磺酰胺、三乙胺和N,N-二甲基吡啶-4-胺反应,得到N-(4-硝基苯磺酰基)环丙烷甲酰胺。该产物可通过硅胶柱色谱法进行分离纯化。
[1] Angewandte Chemie, International Edition (2022), 61(30), e202205619
[2] International Journal of Molecular Sciences (2023), 24(3), 1981
(S)-2-苄基-N,N-二甲基氮杂环丙烷基-1-磺酰胺是一种用于制备司来吉兰的中间体。司来吉兰是一种高效、高选择性、不可逆的单胺氧化酶B(MAO-B)抑制剂,它可以增强多巴胺的传递信号,阻断脑多巴胺的分解,从而延缓或减少脑黑质中多巴胺细胞的死亡。在临床上,司来吉兰的盐酸盐被用于治疗帕金森病、阿兹海默症和抑郁症。
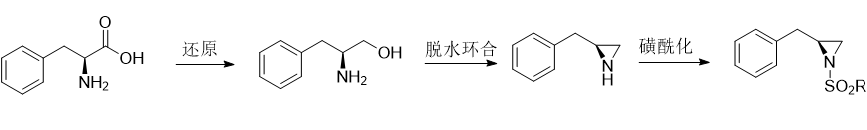
1) 在室温和搅拌条件下,将L-苯丙氨酸悬浮于1,4-二氧六环中,然后分10批次加入硼氢化钠,继续搅拌半小时;
2) 在低于20℃的控温条件下,缓慢滴加浓硫酸,继续搅拌20小时;
3) 在室温下缓慢滴加甲醇,减压蒸除溶剂后,加入氢氧化钠溶液,回流3小时;
4) 冷至室温,加入甲苯,搅拌30分钟,然后静置分层;
5) 分离有机相,得到氨基醇的甲苯溶液,用于下一步反应。
1) 在室温条件下,将氨基醇甲苯溶液中加入硫酸,搅拌30分钟;
2) 回流分水后,加入氢氧化钠溶液;
3) 继续搅拌回流20小时,静置分层;
4) 用食盐水和氢氧化钠溶液洗涤有机层;
5) 分离有机相,得到环乙亚胺的甲苯溶液,用于下一步反应。
1) 在室温和搅拌条件下,将环乙亚胺甲苯溶液中加入三乙胺;
2) 缓慢滴加二甲氨基磺酰氯,继续搅拌6小时;
3) 除盐后,用盐酸、碳酸氢钠和无水硫酸钠洗涤滤液,减压浓缩得到油状物;
4) 将油状物与异丙醇和正己烷混合,搅拌后干燥;
5) 分离固体,得到化合物(S)-2-苄基-N,N-二甲基氮杂环丙烷基-1-磺酰胺。
1H-NMR(CDCl3,400MHz)δ1.58(d,J=4.4Hz,1H),2.13(d,J=4.4Hz,1H),2.66(s,6H),2.69(dd,J=14.0,6.8Hz,1H),2.80-2.90(m,1H),2.95(dd,J=14.0,7.2Hz,1H),7.20-7.28(m,3H),7.30-7.42(m,2H);m/z241(M+H);99.95ee%。
[1] [中国发明] CN201811569604.2 盐酸司来吉兰的制备方法
伯胺是一类具有广泛生理和药理活性的化合物,也是合成中间体。本文介绍了一种制备伯胺盐酸盐的方法。

在25mL克氏管中加入环丙乙炔、cat.[Au]、AgOTf、水和甲醇,进行闭管反应。随后加入甲酸胺和cat.[Rh],在油浴中加热反应。最后通过萃取、回流处理和洗涤过滤得到纯净的目标化合物。

通过两个步骤制备伯胺盐酸盐。首先将环丙烷甲醛和2-甲基-2-丙烷亚磺酰胺在溶剂中反应,然后通过纯化得到中间体。接着将中间体与环丙基溴化镁反应,经过处理和纯化得到最终产物。
[1] [中国发明] CN201710689683.X 一种合成伯胺盐酸盐的方法
[2] From PCT Int. Appl., 2009075830, 18 Jun 2009
3-氯-2-羟基丙烷磺酸钠(CHPS-Na)分子结构中既含有活性较强卤原子和羟基,又含有亲水性的磺酸盐基团,其中卤素原子容易发生取代、消去反应,是合成高聚物工业中重要的功能单体,也可用作有机化工中间体,是比较重要的多功能性物质。
3-氯-2-羟基丙烷磺酸钠是合成高聚物工业中重要的功能单体,也可用作有机化工中间体,用于制备表面活性剂,改性淀粉,钻井液降失水材料,精神类药物原料药等多种产品。3-氯-2-羟基丙烷磺酸钠是一种含羟基和磺酸钠基的氯代烷,它与酰胺发生烷基化反应可以制得含磺酸基的两性表面活性剂,研究结果表明含磺基的两性表面活性剂是一种耐温耐盐的,活性很高的表面活性剂。在碱性条件下,3-氯-2-羟基丙烷磺酸钠可与淀粉发生醚化反应而制得含磺酸基的淀粉衍生物2-羟基-3-磺酸钠基丙基淀粉醚,这种含磺酸基的淀粉衍生物是一种性能优异的钻井液降失水材料。
现有的3-氯-2-羟基丙烷磺酸钠大多通过亚硫酸氢钠、水和环氧氯丙烷在碱性催化剂的作用下反应而成,其反应时间长,反应产物收率较低且纯度也不高,而产品的纯度往往影响下游产品的制备及性能。同时反应过程中还会产生大量的反应废液,浪费资源、污染环境。

图1 3-氯-2-羟基丙烷磺酸钠的合成反应式
一种3-氯-2-羟基丙烷磺酸钠的制备方法[1],其特征在于:将蒸馏水、四丁基溴化铵(TBAB)和亚硫酸氢钠混合后加热至一定温度,然后滴加环氧氯丙烷(ECH),待环氧氯丙烷滴加完毕,在该温度下保温一定时间,反应结束后,冰水浴冷却至10℃以下,结晶,真空抽滤,分离出固体物,回收溶剂。固体物用乙醇洗涤两次,干燥,得到白色粉末状固体(粗品);将上述粗产品用蒸馏水进行重结晶,得到白色晶体3-氯-2-羟基丙烷磺酸钠,将反应母液或重结晶母液回收;其中,四丁基溴化铵的质量是环氧氯丙烷质量的3%-8%,亚硫酸氢钠和环氧氯丙烷摩尔比为1.05-1.30,蒸馏水和亚硫酸氢钠的摩尔比为9-11,滴加时间为0.75-2.5h,反应时间为0.75-2.5h,反应温度为80-90℃.
[1]CN105585513A
甲基磺酸酐是一种外观呈灰白色固体粉末的化合物,具有腐蚀性和湿气敏感性,需要在阴凉干燥处储存。它可以在乙醚中重结晶,溶于多种有机溶剂。
甲基磺酸酐是一种常用的甲磺酰化试剂,可以与醇反应生成甲磺酸酯。与甲磺酰氯相比,使用甲基磺酸酐可以避免生成氯代副产物。然而,在不饱和醇的反应中,甲基磺酸酐的效果可能不理想,或者会生成其他产物。

甲基磺酸酐还可以与胺反应生成甲磺酰胺,这是一种常用的胺基保护方法。甲磺酰胺在酸性和碱性条件下均可稳定存在。使用LiAlH4可以将甲磺酰胺脱保护,重新得到游离的胺。

在路易斯酸的催化下,甲基磺酸酐可以与苯或取代苯发生Friedel-Crafts磺酰化反应。与甲磺酰氯相比,甲基磺酸酐可以使取代苯化合物同样得到良好的产率。

除了上述常见的反应,甲基磺酸酐还可以与二甲基亚砜联用对醇进行氧化反应。使用甲基磺酸酐和二甲基亚砜生成的组合试剂可以将伯醇氧化成相应的醛,或者将仲醇氧化成相应的酮。

2007年,Taylor等人报道了甲基磺酸酐参与的苄醇环丙烷化反应,该反应条件简单,产率都在85%以上。

在有机合成领域中,寻找高效的合成路径对于获得西司他丁钠至关重要,本文将总结其合成方法。
简述:西司他丁钠(cilastatin sodium),化学名为 (Z)-7-[(2R)-2-氨基-2-羧基乙硫基]-2-[(S)-2,2- 二甲基环丙甲酰胺基]-2-庚烯酸钠,是默克公司研发的脱氢肽酶抑制剂,本身不具备抗菌作用,但可以防止脱氢肽酶水解碳青霉烯类抗菌药,是后者的增效剂,临床常用注射用亚胺培南-1复方制剂,抗菌谱广、抗菌作用强,用于治疗下呼吸道感染、尿路感染、妇科感染、败血症,以及金黄色葡萄球菌引起的心内膜炎、骨和关节感染及皮肤结构感染等多种厌氧和需氧菌引起的感染。
合成:
1. 路线一
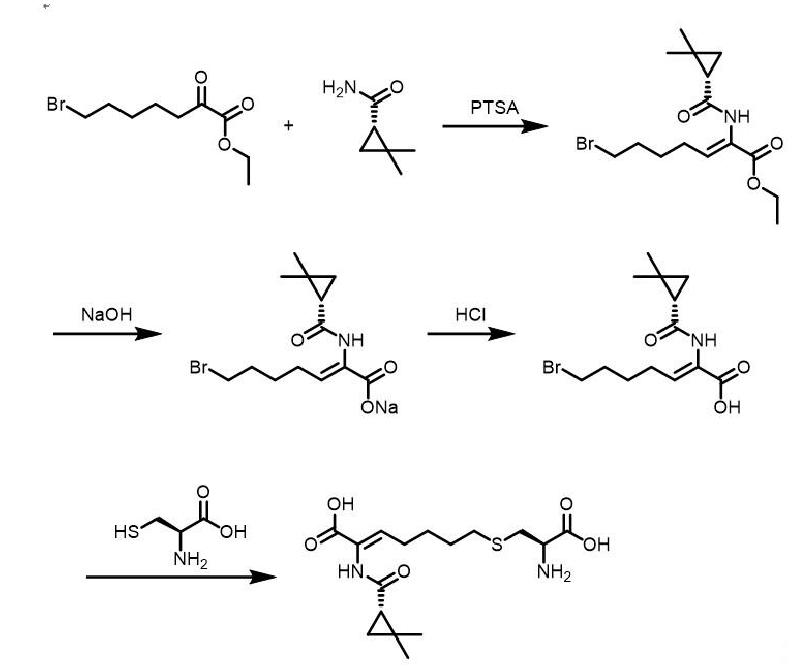
Graham D.W、徐晓莉等人报道了制备西司他丁钠的方法,在催化剂对甲苯磺 酸(PTSA)存在下,在回流甲苯中通过共沸除水,7-氯-2-氧代庚酸乙酯与(S)-(+)-2,2-二甲基环丙烷甲酰胺反应,之后与L-半胱氨酸盐酸盐在碱性钠水溶液中缩合,得到西司他丁酸化合物,收率为19.7 %。用盐酸溶液调节pH=3.0,将E异构体异构化为Z异构体,利用离子交换色谱和结晶分离相关产物。
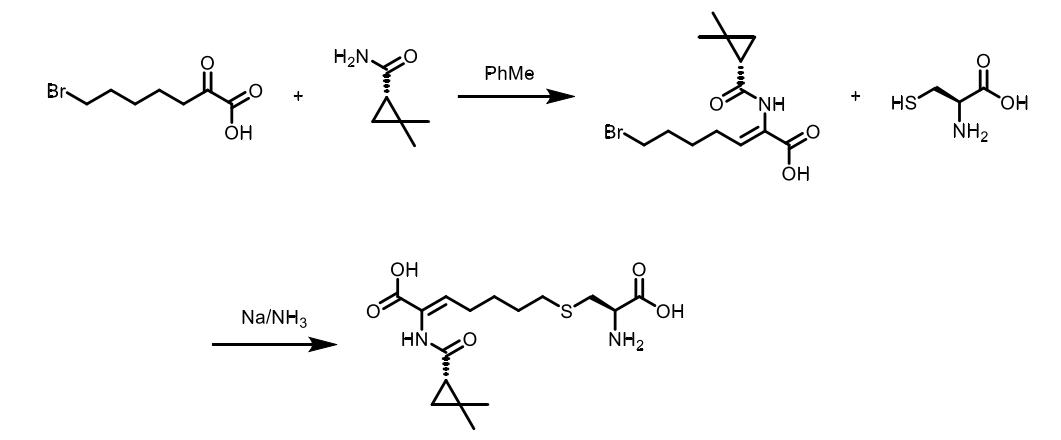
2. 路线二
石晓华等人报道了(Z)-7-氯-((S)-2,2-二甲基环丙烷甲酰胺基)-2-庚烯酸和L-半胱胺酸盐酸盐反应得到西司他丁,收率为18.3 %。该合成方法工艺相对简单、条件比较温和、且成本较低,更适合工业化生产。
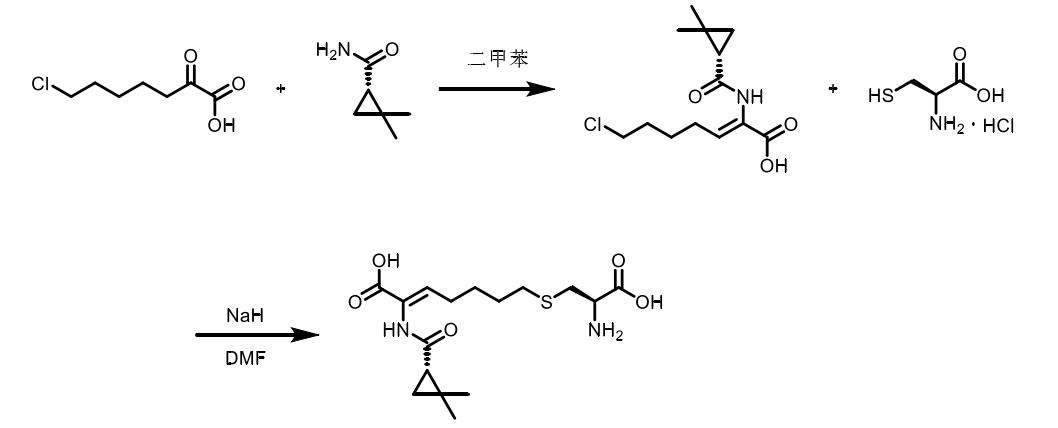
3. 路线三
Kumar Y.、陈扬、郎方等人描述了在碱性条件下,L-半胱氨酸盐酸盐一水化 合物与(Z)-7-氯-((S)-2,2-二甲基环丙烷甲酰胺基)-2-庚烯酸在室温下进行反应,使用盐酸调节pH=0.5-1.5,在90-95 ℃温度下,西司他丁酸的E-异构体发生异构化。该方法使用非离子树脂纯化西司他丁酸并进一步结晶的方法,得到西司他丁钠,总收率为32.2 %。
4. 路线四
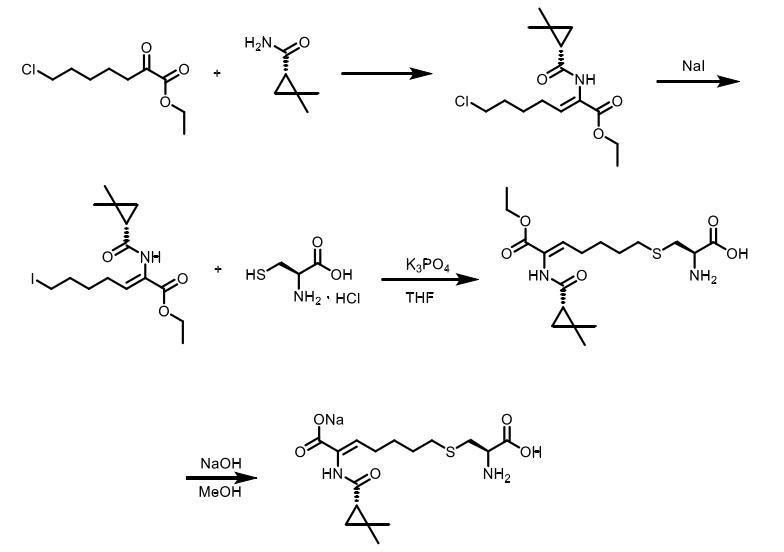
欧阳罗等人报道了(Z)-7-氯-((S)-2,2-二甲基环丙烷甲酰胺基)-2-庚烯酸乙酯和L-半胱胺酸盐酸盐80摄氏度反应,以四氢呋喃作溶剂、磷酸三钾作碱,得到西司他丁钠,收率为74.1 %。该方法使用磷酸三钾在温和的条件下合成硫醚化合物,操作简单,不需要使用强碱或无水反应体系。
5. 路线五
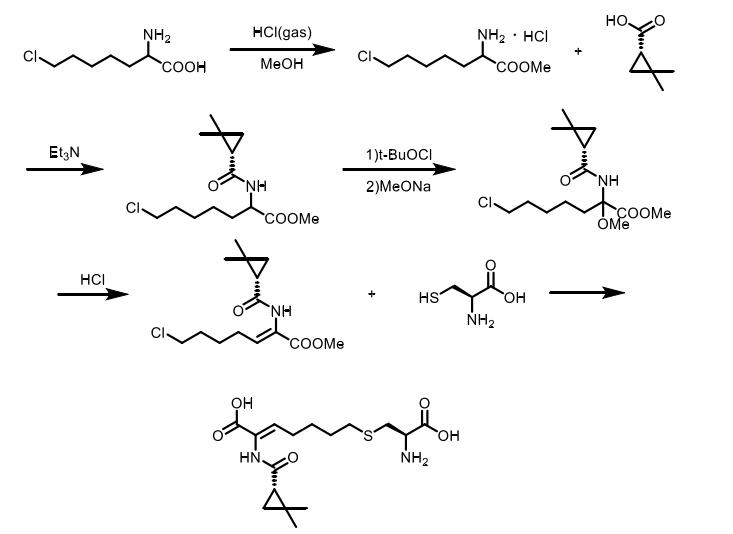
根据默克公司开发的原始路线,西司他丁合成中的中间体是7-卤-2-氧代庚酸,它与二甲基环丙烷甲酰胺缩合,卤素原子进一步被L-半胱氨酸部分取代。外消旋二甲基环丙烷羧酸是西司他丁的起始原料,该化合物是抗生素泰能药物制剂的一部分。该方法需要使用1,3-丙烷二硫醇和5-氯-1-戊基溴化镁等物质合成酮酸,但具有5个以上碳原子的脂肪族α-酮羧酸是不稳定的。此外,酸与酰胺的缩合以低收率(30-35 %) 制得N-酰化脱氢氨基酸。
参考文献:
[1]王英杰. 西司他丁钠及其关键中间体的合成工艺研究[D]. 湖北大学, 2023. DOI:10.27130/d.cnki.ghubu.2023.000313.
[2]李承明,郭珩,杨丽娜等. 西司他丁钠有关物质的合成 [J]. 中国医药工业杂志, 2021, 52 (06): 786-789. DOI:10.16522/j.cnki.cjph.2021.06.007.
【英文名称】Methanesulfonic Anhydride
【分子式】C2H6O5S2
【分子量】174.22
【CAS登录号】7143-01-3
【缩写和别名】Ms2O
【物理性质】甲磺酸酐是一种灰白色固体粉末,具有较高的熔点和沸点。它可以在乙醚中重结晶,并且可以溶于多种有机溶剂。
【制备和商品】甲磺酸酐可以在国际大型试剂公司购买。
【注意事项】甲磺酸酐具有腐蚀性,对湿气敏感,应储存在阴凉干燥处。
甲磺酸酐是一种常用的甲磺酰化试剂。它可以与醇在吡啶、2,4,6-三甲基吡啶或三乙胺等碱的存在下反应,生成相应的甲磺酸酯。与甲磺酰氯相比,甲磺酸酐的优势在于避免了氯代副产物的生成。然而,在不饱和醇的反应中,甲磺酸酐可能无法得到理想的结果,或者会生成其他产物。
该试剂还可以与胺反应生成甲磺酰胺,从而实现胺基的保护。甲磺酰胺在酸性和碱性条件下均稳定存在。使用LiAlH4可以将甲磺酰胺脱保护,重新得到游离的胺。当分子中同时存在羟基和胺基时,可以选择适当的条件使甲磺酸酐优先与胺基反应,而不影响羟基。
该试剂还可以与苯或取代苯发生Friedel-Crafts磺酰化反应。与甲磺酰氯不同,甲磺酸酐可以使取代苯化合物得到良好的产率。在体系中加入硫酸可以得到二芳基砜,从而提高反应的产率。
除了上述常见的反应,甲磺酸酐还可以与二甲基亚砜联用对醇进行氧化反应。使用甲磺酸酐与二甲基亚砜生成的组合试剂,可以将伯醇氧化成相应的醛或酮。
2007年,Taylor等人报道了甲磺酸酐参与的苄醇的环丙烷化反应。该反应条件简单,产率都在85%以上。
参考文献
1. Hu,G.; VaseUa, A. Heh. Chim. Acta 2004,87,2405.
2. Kuroda, C.; Okada, M.; Shinozaki, S.; Suzuki, H. Tetrahedron 2006, 62,726.
3. Rahaim Jr, R. J.; Maleczka Jr., R. E. Synthesis 2006, 3316.
4. Kim, I. H.; Tsai, H.-J.; Nishi, K.; Kasagami, T.; Morisseau, C.; Hammock, B. D. J. Med. Chem. 2007,50,5217.
5. Olah, G. A.; Kobayashi, S.; Nishimura, J. J. Am. Chem. Soc. 1973, 95,564.
6. Smith, K.; Ewart, G. M.; El-Hiti, G. A.; Randles, K. R. Org. Biomol. Chem. 2004,2,3150.
7. Tyobeka, T. E.; Hancock, R. A.; Weigel, H. Chem. Commun. 1980,114.
8. Albright, J, D.J. Org. Chem. 1974,39,1977.
9. Melancon, B. J.; Perl, N. R.; Taylor, R. E. Org. Lett. 2007, 9, 1425.
高哌嗪为白色至微黄色结晶,Cas号:505-66-8,分子式:C5H12N2分子量:100.16,熔点:42-45℃,闪点:64℃;沸点:167℃。

高哌嗪是重要的医药中间体,因为其结构特征,导致其应用广泛,目前主要用来合成赛克利嗪、卡马西平、喹诺酮和氯环嗪等药物。另外还有以高哌嗪为原料修饰的喹啉及异喹啉衍生物、喹诺酮衍生物、噻唑烷羟酸酰胺衍生物等药物,和用于合成哒嗪胺、含硝酰基的苄胺衍生物、水溶性唑类等的药物,对治疗心血管疾病、间质性浆细胞肺炎特别是对AIDS患者的间质性浆细胞肺炎、哮喘、中枢神经系统病症包括抑郁症和焦虑症等表现出良好的疗效。
一种高哌嗪的制备方法,其特征在于:包括以下步骤:
(1)第一步:取乙二胺和正丁醇与对甲苯磺酰氯进行反应,再加入50%氢氧化钠,搅拌,加热回流,再加入溴氯丙烷和50%氢氧化钠溶液,发生反应1-3小时,离心,得到N,N’-二对甲苯磺酰基高哌嗪;
(2)第二步:依次将苯酚、氢溴酸和N,N’-二对甲苯磺酰基高哌嗪投入反应罐内进行反应,减压浓缩,除去剩余的苯酚和氢溴酸,加入乙醇,离心,得到高哌嗪氢溴酸盐;
(3)第三步:将高哌嗪氢溴酸盐和50%氢氧化钠溶液投入反应罐中,室温搅拌,向反应罐中加入甲苯,回流,离心,收集滤液,减压蒸馏,收集90℃-110℃左右的馏分,得到高哌嗪。
本发明的高哌嗪的合成方法成本低,原材料易获得,收率高,污染较少,利于工业化。
CN104744382A