生物素-八聚乙二醇-氨基是一种常用的医药合成中间体。当吸入生物素-八聚乙二醇-氨基时,应将患者移到新鲜空气处。如果皮肤接触,应立即脱去污染的衣着,并用肥皂水和清水彻底冲洗皮肤。如有不适感,应就医。如果眼睛接触,应分开眼睑,用流动清水或生理盐水冲洗,并立即就医。如果误食,应立即漱口,禁止催吐,并立即就医。
生物素-八聚乙二醇-氨基具有广泛的应用,以下是一些应用举例:
1)合成马来酰亚胺丙酰基-PEG7-生物素:
在室温、N2下,将生物素-八聚乙二醇-氨基(1)(100mg,0.168mmol)加入无水二氯甲烷(7mL)中的搅拌溶液中,然后加入马来酰亚胺丙酸NHS酯(2)(49.2mg,0.186mmol,1.1当量)。搅拌1小时后,TLC分析表明反应完成,加入1NHCl(2mL)。分离有机溶液,用盐水洗涤并经Na2SO4干燥。通过硅胶快速柱色谱法纯化获得粗产物,用分级梯度的MeOH/二氯甲烷(v/v=1:30、1:20和1:10)洗脱,得到马来酰亚胺丙酰基-PEG7-生物素(3)(65mg,0.087mmol,52%产率)。1HNMR(CDCl3)d7.01(brs,1H),6.96(brs,1H),6.70(s,2H),5.86(s,1H),5.06(s,1H),4.51(m,1H),4.33(m,1H),3.84(t,J=7.2Hz,2H),3.62-3.66(m,24H),3.53(m,4H),3.40(m,4H),3.15(m,1H),2.88-2.96(m,1H),2.73(d,J=12.6Hz,1H),2.52(t,J=7.2Hz,2H),2.24(t,J=7.0Hz,2H),1.66(m,4H),1.45(m,2H)。
2)合成2-氟-5-马来酰亚胺苯基-PEG7-生物素:
在环境温度、N2下,将生物素-PEG7-NH2(1)(0.1g,0.168mmol,1当量)和2-氟-5-马来酰亚胺苯酚NHS酯(6)(0.084g,0.252mmol,1.5当量)混合物在二氯甲烷(1mL)中搅拌过夜。去除溶剂后,通过LH20柱尺寸排阻色谱法(SEC)纯化,用MeOH/二氯甲烷(v/v1:1)洗脱,得到2-氟-5-马来酰亚胺苯基-PEG7-生物素(7)(28mg,0.034mmol,20.5%产率)。HPLC显示,其中大约有10%的水解形态。此外,还获得了额外的期望产物和水解形态,混合物中3:2比率为90mg。
[1] CN201580053082.9 轭合多肽的方法
(+)生物素-N-琥珀酰亚胺基酯是一种重要的化工原料和医药中间体,被广泛应用于临床医学、生物学研究、化妆品和摄影技术等领域。在动植物组织中,它通常以酰胺键的形式与蛋白质分子中的赖氨酸残基的ε-氨基共价结合。此外,它还可以作为有效的电辐射防护剂,被广泛应用于军事和和平事业。因此,(+)生物素-N-琥珀酰亚胺基酯的合成越来越受到重视。
将d-生物素和N-羟基琥珀酰亚胺溶解在热DMF中,加入N,N’-二环己基碳二亚胺并在室温下搅拌过夜,形成白色沉淀物。过滤反应混合物,蒸发滤液,并用乙醚处理滤液。最后,用乙醚洗涤白色沉淀物,得到(+)生物素-N-琥珀酰亚胺基酯。
将生物素加入DMF中,加热溶解后加入N-羟基琥珀酰亚胺和DCC,室温下搅拌过夜。过滤白色尿素,蒸发DMF并加入Et2O,搅拌反应混合物。最后,用异丙醇使固体再结晶,得到(+)生物素-N-琥珀酰亚胺基酯。
以上是两种合成(+)生物素-N-琥珀酰亚胺基酯的方法,根据实际需要选择适合的方法进行合成。

图2 (+)生物素-N-琥珀酰亚胺基酯的合成路线
[1]程玉婷,彭阳峰,赵红亮. (+)生物素-N-琥珀酰亚胺基酯的合成研究[J].化学世界,2009,50(10):607-610.DOI:10.19500/j.cnki.0367-6358.2009.10.009.
[2]Li, Xuelian; et al. Investigating Molecular Interactions in Biosensors Based on Fluorescence Resonance Energy Transfer. Journal of Physical Chemistry C (2010), 114(14), 6255-6264.
N-芴甲氧羰基-N'生物素-L-赖氨酸是一种常用的氨基酸保护试剂,在多肽合成领域经常使用。本文介绍了两种制备方法。

将N-芴甲氧羰基-N'叔丁氧羰基-L-赖氨酸溶解于二氯甲烷中,加入质量百分浓度为15%的三氟醋酸溶液,剧烈搅拌并冷却,通过薄层色谱检测反应完全,减压蒸馏去除溶剂和三氟醋酸,再次溶解于二氯甲烷,再次减压蒸馏,用石油醚洗涤,将剩余固体溶于二甲基甲酰胺中,加入N-甲基吗啉和N-羟基琥珀酰亚胺生物素,反应3小时,通过薄层色谱显示反应完全,向反应中加入柠檬酸溶液,固体析出,洗涤并烘干,得到纯度为99.1%、收率为90%的产品。
将N-芴甲氧羰基-N'叔丁氧羰基-赖氨酸溶解于乙醇或乙醚中,通入氯化氢气体,剧烈搅拌并冷却,通过薄层色谱检测反应完全,过滤掉溶剂,用乙醚洗涤,将剩余固体溶于二甲基甲酰胺中,加入N,N-二异丙基乙胺和N-羟基琥珀酰亚胺生物素,反应6小时,通过薄层色谱显示反应完全,向反应中加入柠檬酸溶液,固体析出,洗涤并烘干,得到纯度为98.8%、收率为91%的产品。
这种制备方法利用吨级生产的N-芴甲氧羰基-N'叔丁氧羰基-赖氨酸,降低了初始原料的成本,并且最后使用N-羟基琥珀酰亚胺生物素,有效降低了成本。
[1] [中国发明] CN201310122131.2 一种N-芴甲氧羰基-N'-生物素-L-赖氨酸的制备方法
生物素-标记羊抗兔免疫球蛋白(H+L)是一种荧光标记二抗,通过将羊抗兔免疫球蛋白(H+L)与生物素化标记制成,实现了与第二抗体的偶联。生物素具有高亲和力,可以与许多生物素分子结合。通过将链霉亲和素与标记物(如HRP或荧光探针)结合,可以增加检测低水平表达的蛋白质的可能性。在大多数测定中,首先添加生物素标记的第二抗体,然后加入与标记物(如HRP)偶联的链霉亲和素。生物素广泛分布于动、植物组织中,可以从卵黄和肝组织中提取。随着各种生物素衍生物的问世,生物素-亲合素系统(Biotin-Avidin System,BAS)在医学各领域得到广泛应用。

近年来的研究表明,生物素-亲合素系统可以与各种标记物结合。通过亲合素-生物素-酶复合物的形成,可以追踪生物素标记的抗原或抗体,并通过酶催化底物显色来检测相应的抗体或抗原。由于抗原或抗体分子可以与多个生物素偶联,并且一个亲合素分子可以结合四个生物素分子,这种新的生物放大系统进一步提高了检测的灵敏度。BAS具有高灵敏度、高特异性和稳定性等优点,在现代生物免疫学领域得到广泛应用,并显示出明显的优越性。BAS已经应用于放射免疫、免疫荧光和免疫电镜等技术,尤其在酶免疫技术中应用更广泛。
本研究以肝癌血清标志物甲胎蛋白为检测对象,构建了一种高灵敏性的电化学免疫传感器,并对其临床结果进行了初步评价。该传感器采用了基于单抗多抗夹心体系的设计,制备简单且具有高灵敏性。通过物理吸附的方法将捕获探针抗体固定在印刷电极芯片上,获得了比共价耦联更好的抗体组装效率和抗体组装量。在靶蛋白和信号探针及多克隆抗体反应后,酶标二抗连接,利用便携式多通道电化学仪检测辣根过氧化物酶催化底物的氧化还原电流实现了检测。通过引入Poly-HRP放大技术,可以增强免疫反应电流响应的信号,提高传感器的检测灵敏度。实验结果显示,该传感器对甲胎蛋白的检测限达到56pg/ml,同时具有两个线性范围,低浓度区间为64p-1000p,高浓度区间为1n-250n。该传感器具有灵敏度高、线性范围宽等特点,对肝癌的诊断及甲胎蛋白的检测具有潜在的应用前景。
[1] A novel liquid-phase piezoelectric immunosensor for detecting Schistosoma japonicum circulating antigen[J]. Zhili Wen, Shiping Wang, Zhaoyang Wu, Guoli Shen. Parasitology International. 2011(3)
[2] Hepatocellular Carcinoma: Screening and Staging[J]. Morris Sherman. Clinics in Liver Disease. 2011(2)
[3] Quantum dot-based immunochromatography test strip for rapid, quantitative and sensitive detection of alpha fetoprotein[J]. Qiuhua Yang, Xiaoqun Gong, Tao Song, Jiumin Yang, Shengjiang Zhu, Yunhong Li, Ye Cui, Yingxin Li, Bingbo Zhang, Jin Chang. Biosensors and Bioelectronics. 2011(1)
[4] A DNA Nanostructure-based Biomolecular Probe Carrier Platform for Electrochemical Biosensing[J]. Hao Pei, Na Lu, Yanli Wen, Shiping Song, Yan Liu, Hao Yan, Chunhai Fan. Adv. Mater.. 2010(42)
[5] 李胜昔. 电化学免疫传感器在肿瘤标志物检测中的应用研究[D]. 复旦大学, 2012.
D-生物素(d-Biotin,I),又名维生素H或辅酶R,是一种可溶性B族维生素。

过去的合成方法存在一些问题,但现在有一种改进的方法。这种方法使用无机酸和有机溶剂,通过脱苄/关环反应将化合物转化为D-生物素。
这种方法的总收率高达85~90%,并且不需要分离化合物III,可以直接与环化试剂进行关环反应,然后再进行酸化。所得产品的质量符合美国药典23版标准。
在这种方法中,无机酸可以是盐酸、氢溴酸等,有机溶剂一般是芳香烃类。关环反应可以使用双光气或三光气作为环化试剂,碱可以使用常见的氢氧化钠或氢氧化钾。在适当的溶剂中稍加温度即可进行关环反应。
本文介绍了如何使用3-氟-4-氨基苯甲酸来合成蓝萼甲素生物素标记物。
简述:3-氟-4-氨基苯甲酸,英文名称:4-Amino-3-fluorobenzoic Acid,CAS:455-87-8,分子式:C7H6FNO2,密度:1.43 g/cm3。3-氟-4-氨基苯甲酸可用于合成蓝萼甲素生物素标记物。
蓝萼甲素是唇形科香茶菜属植物蓝萼香茶菜提取出来的二萜化合物,是蓝萼香茶菜中的主要活性成分。近年来,对此种二萜类化合物抑制肿瘤,抗病毒抑菌,对心血管系统保护及抗癌活性研究,已经成为当代天然药物化学的研究热点之一。而生物素-亲和素系统是一种具有高亲和力、灵敏度高、特异性强和稳定性好的信号放大标记技术,由于该标记技术具有优秀的性质,因此很快渗透到很多个学科,在细胞和抗原的定位和检测有相当重要的作用。
应用:合成蓝萼甲素生物素标记物。
李显伦的等人对生物素与6-氨基己酸、3-氨基苯甲酸、对氨基苯甲酸、4-氨基-3-甲基苯甲酸、3-氟-4-氨基苯甲酸反应得出5种不同的生物素延长链,生物素与6-氨基 己酸延长后再次与6-氨基己酸反应形成第6种生物素延长链。然后生物素以及6种不同生物素延长链与蓝萼甲素进行酯化反应。一共得出14个不同的蓝萼甲素生物素标记。并且对部分蓝萼甲素生物素标记物进行体外抗肿瘤活性测试,初步得出了抗肿瘤活性较好的蓝萼甲素生物素标记物。
方法为:生物素先与氯甲酸异丁酯在三正丁胺的作用下反应10min,再与相应的氨基苯甲酸反应,其中与对氨 基苯甲酸反应生成的化合物21,与间氨基苯甲酸反应生成的化合物22,与4-氨基-3- 甲基苯甲酸反应生成的化合物23,与3-氟-4-氨基苯甲酸反应生成的化合物24,反应路线如下图。
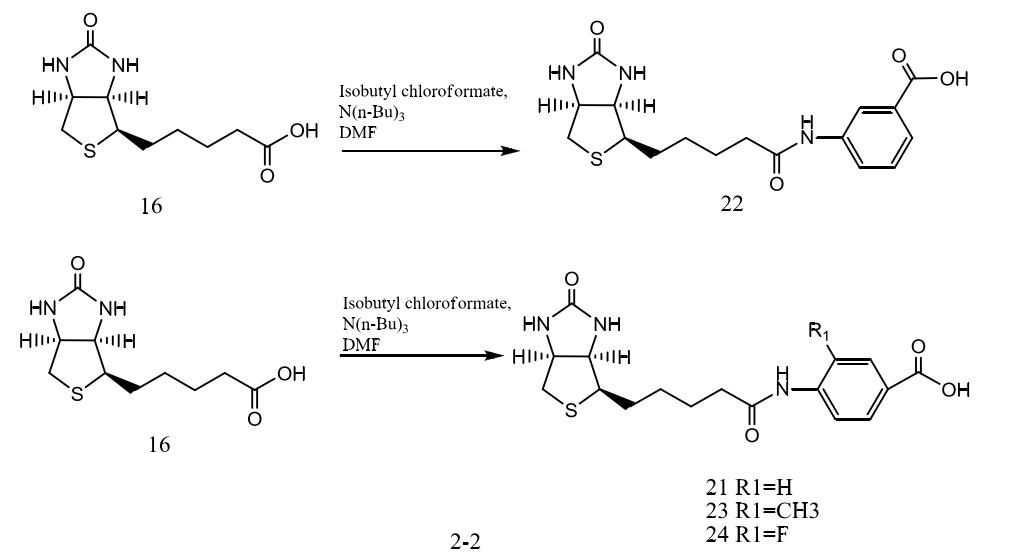
4-氨基-3-氟苯甲酸生物素基甲素的制备具体步骤如下:
(1)N-(+)-Biotinyl-4-amino-3-fluorobenzoic acid的制备(化合物24)
在100ml的圆底烧瓶加入500mg生物素,并加入0.64ml三正丁胺以及40ml DMF, 搅拌溶解后加入0.32ml氯甲酸异丁酯,在室温下反应10min后,将混合物缓慢地在5℃环境下加入到40ml含548mg 4-氨基-3-氟苯甲酸的DMF溶液中,在5℃下搅拌2小时后将溶剂旋干,将粗沉淀物溶于36ml温热的50%乙醇水溶液中,并将混合物以2.0 当量的盐酸调节pH=2.0,在0℃下放置12h后将沉淀过滤并用水洗涤后在真空下干燥。得到白色固体465mg。产率62.4%。
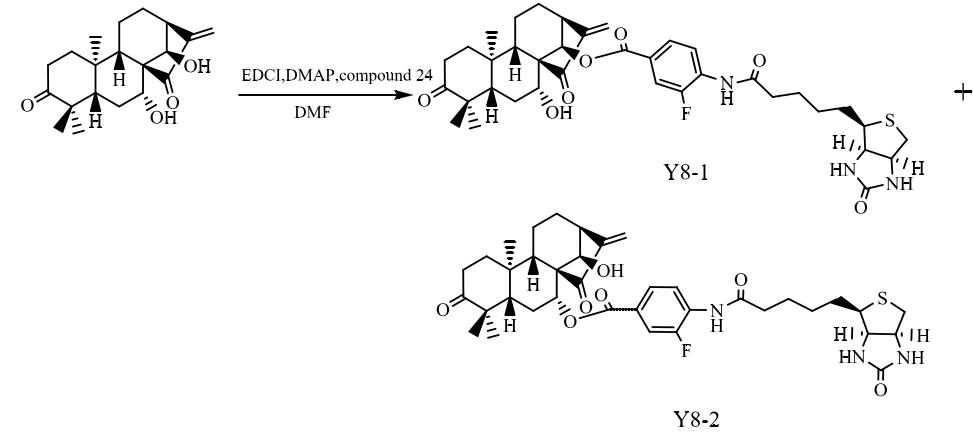
(2)4-氨基-3-氟苯甲酸生物素基甲素的制备
在50ml的圆底烧瓶中如入332mg蓝萼甲素、458mg化合物24、383mg EDCI、 122mg DMAP以及20ml DMF溶液,在常温下反应24h后旋干,过硅胶柱层析,用氯仿-甲醇(201)洗脱,得到4-氨基-3-氟苯甲酸生物素基甲素混合物190mg,然后以反相制备液相分离,用67%甲醇:33%水洗脱,得到7-(4-氨基-3-氟苯甲酸)生物素 基甲素(Y8-2)64mg,14-(4-氨基-3-氟苯甲酸)生物素基甲素(Y8-1)96mg。产率分别为 9.2%和13.8%。
参考文献:
[1]李显伦.蓝萼甲素生物素标记物合成[D].苏州大学,2016.
生物素标记肿瘤坏死因子抗体是一种多克隆抗体,能够特异性结合肿瘤坏死因子,并广泛应用于多种免疫学实验,如Western Blot、IHC-P、IF、ELISA、Co-IP等。
检测原理是利用双抗体夹心法测定标本中肿瘤坏死因子水平。首先,将纯化的肿瘤坏死因子抗体包被在微孔板上,形成固相抗体。然后,依次加入肿瘤坏死因子和HRP标记的肿瘤坏死因子抗体,形成抗体-抗原-酶标抗体复合物。经过洗涤后,加入底物TMB进行显色反应。最终,通过酶标仪测定吸光度(OD值)并利用标准曲线计算样品中肿瘤坏死因子浓度。

抗体生物素-亲和素系统是一种高亲合力的结合系统,可以与各种标记物结合,并具有多级放大效应。这使得生物素标记肿瘤坏死因子抗体在微量抗原、抗体定性、定量检测及定位观察研究中更加灵敏和可靠。
α肿瘤坏死因子(TNFα)是一种由巨噬细胞和单核细胞产生的促炎细胞因子,参与正常炎症反应和免疫反应。在许多病理状态下,TNFα的产生会增加,如败血症、恶性肿瘤、心脏衰竭和慢性炎性疾病。重症类风湿关节炎患者的血液和关节中也可发现增多的肿瘤坏死因子。
本研究通过制备大鼠非致死性机械创伤模型,研究了创伤后大鼠血清肾上腺素(EPI)和肿瘤坏死因子α(TNF-α)的变化,并探讨了它们与肺损伤的关系,以及可能的机制和临床意义。
实验使用8周龄健康雄性Wistar大鼠,将其随机分为伪创伤组、创伤组、正常对照组、盐酸肾上腺素组和肿瘤坏死因子-α组。其中,伪创伤组和创伤组制备非致死性机械性创伤模型;盐酸肾上腺素组和肿瘤坏死因子-α组通过腹腔注射制备药物肺损伤模型;正常对照组注射生理盐水作为对照。在造模成功后6小时,采集大鼠腹主动脉血液,观察肺组织病理变化,检测肺组织中细胞凋亡指数,并测定血清中肾上腺素和TNF-α的含量变化。
结果显示,创伤组的血清肾上腺素含量(1.7306±0.1394 ng/ml)明显高于伪创伤组(0.1712±0.0193 ng/ml),差异具有统计学意义(p<0.01)。
[1]ATTENUATION OF REPERFUSION LUNG INJURY AND APOPTOSIS BY A2A ADENOSINE RECEPTOR ACTIVATION IS ASSOCIATED WITH MODULATION OF Bcl-2 AND Bax EXPRESSION AND ACTIVATION OF EXTRACELLULAR SIGNAL-REGULATED KINASES[J].Julia Rivo,Evelyne Zeira,Eithan Galun,Sharon Einav,Joel Linden,Idit Matot.Shock.2007(3)
[2]The key role of apoptosis in the pathogenesis and treatment of pulmonary hypertension[J].Emin Gurbanov,Xiao Shiliang.European Journal of Cardio-Thoracic Surgery.2006(3)
[3]Systemic Inflammation and Disseminated Intravascular Coagulation in Early Stage of ALI and ARDS:Role of Neutrophil and Endothelial Activation[J].Satoshi Gando,Takashi Kameue,Naoyuki Matsuda,Atsushi Sawamura,Mineji Hayakawa,Hirokatsu Kato.Inflammation.2004(4)
[4]Lung Inflammatory Responses and Hyperinflation Induced by an Intratracheal Exposure to Lipopolysaccharide in Rats[J].Anne-Helene Jansson,Christina Eriksson,Xiangdong Wang.Lung.2004(3)
[5]贾国平.非致死性机械创伤大鼠血清肾上腺素、肿瘤坏死因子-α的变化及其意义[D].山西医科大学,2011.