苄基三甲基氢氧化铵是是一种重要的有机化合物,其合成方法和应用在化学领域中引起了广泛的关注,该文章将苄基三甲基氢氧化铵的合成方法及其应用,对于推动化学领域的发展具有重要意义。
简介: 苄基三甲基氢氧化铵是一种化学物质。外观与性状:透明略黄色溶液。密度:1.059 g/mL at 25 °C。熔点:-98oC。沸点:65°C。闪点:60 °F。折射率:n20/D 1.43。主要用于有机试剂,医药中间体、相转移催化剂。
储存方法:储存于阴凉、通风的库房。远离火种、热源、防静电。库温不宜超过30℃。应与氧化剂、酸性物质分开存放,切忌混储。密封保存。不宜大量储存或久存。采用防爆型照明、通风设施。禁止使用易产生火花的机械设备和工具。储区应备有泄漏应急处理设备和合适的收容材料。
1. 合成:通常以苄基三甲基卤代铵为原料与氧化银在溶剂中反应制备和以苄基三甲基卤代铵为原料与氢氧化钾在溶剂中反应制备。
赵文洲公开了一种连续电解制备高纯度苄基三甲基氢氧化铵的方法。该方法使用浓度为30%~50%的苄基三甲基氯化铵水溶液作为原料,将其输入阳极室。同时,将浓度为5%~30%的苄基三甲基氢氧化铵水溶液加入中间室和阴极室。然后打开所有的循环泵,连接阳极极板和阴极极板进行连续电解。通过阳离子膜的选择和连续循环过滤去除杂质,可以得到纯度为5%~30%的高纯度苄基三甲基氢氧化铵。在该产品中,各金属离子的浓度均小于20 ppb,各阴离子的浓度均小于1 ppm。该方法具有较高的产品纯度,并且产品转化率在98%以上。
2. 应用:
2.1 作为离子液制备纳米材料
利用离子液体前驱体苄基三甲基氢氧化铵(BTMAH)的辅助作用,成功制备了具有片状结构的氧化锌纳米颗粒。在80℃下,通过离子液体苄基三甲基氢氧化铵的作用,最终得到了与其他离子液体不同的形貌。氧化锌纳米颗粒呈现片状结构的形成是由于离子液体BTMAH中的阳离子在某个极性表面上吸附,从而降低了表面能量并形成了片状结构。同时,对氧化锌纳米颗粒进行了气敏性能测试,结果显示该元件在240℃的工作温度下表现出良好的性能。它对乙醇气体具有高度灵敏度,在低浓度条件下仍能保持较高的感知能力。此外,该元件还具备快速响应恢复和良好的稳定性等优点,对气敏传感领域的进展具有重要意义。
2.2 相转移催化合成N,N-二乙基苯胺
N,N-二乙基苯胺是一种广泛应用于染料、药物和彩色显影剂制备的中间体。田庆伟在常压下采用相转移催化方法,利用苄基三甲基氢氧化铵作为催化剂,使用苯胺和溴乙烷进行反应,在碱性条件下成功地合成了高产率的N,N-二乙基苯胺。研究还探究了反应体系中各因素对产率的影响,并得出了最佳工艺条件:在45 mL 45% 氢氧化钠溶液中,苯胺与溴乙烷的摩尔比为1:1.50,苄基三甲基氢氧化铵用量为0.60 g,在85℃下常压反应6小时,可获得90.8%的产品产率。
参考文献:
[1].李锐. 离子液体辅助合成金属氧化物纳米材料及其气敏性能的研究[D].山东大学,2013.
[2].田庆伟.苄基三甲基氢氧化铵相转移催化合成N,N-二乙基苯胺的研究[J].精细石油化工,2000(06):32-34.
[3].赵文洲. 三室两膜连续电解制备高纯苄基三甲基氢氧化铵的方法[P]. 北京:CN104630818A, 2015-05-20.
苄基三甲基氢氧化铵 (Triton B)作为相转移催化剂和强碱在有机合成中被广泛使用。Triton B 作为碱能够促进2-噁唑烷酮的水解开环反应。该反应需要在 -40°C 下进行,以避免破坏环上N-原子的保护基。产物具有 1,1-二氨基-2-羟基的骨架结构,经过进一步的氧化后生成α-氨基取代的甘氨酸。
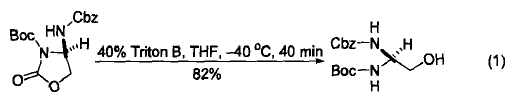
在Triton B的催化作用下,单取代的环氧乙烷能够被二巯基乙烷选择性地亲核进攻而发生开环。该反应一般发生在未被取代的碳原子上,生成相应的β,β-二羟基二甲基二硫醚。
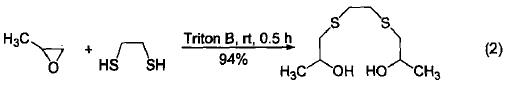
Triton B 能够催化酮和醛与炔烃在DMSO 溶剂中的炔基化反应。脂肪族羰基化合物为底物时,反应产率较高(43%?96%)。而当芳香族羰基化合物参与反应时,产率相对较低(26%?38%)。环己酮和苯乙炔为底物的炔基化反应产率为95%。
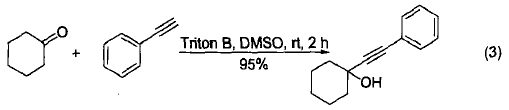
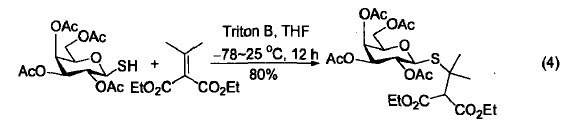
苄基三甲基氢氧化铵是共轭加成反应中的有效催化剂。在Triton B的作用下,1-巯基-D-吡喃半乳糖中的巯基可以与亚异丙基丙二酸二乙酯发生共轭加成生成硫代半乳糖苷。经进一步氧化则得到半乳糖基亚砜,该产物是糖基化反应的重要前体。在Triton B的催化作用下,苯酚也能与丙烯腈发生1,2-共轭加成。
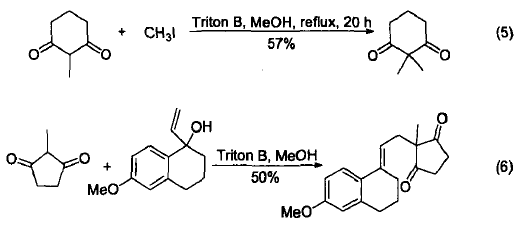
Triton B能够催化1,3-二酮的烷基化反应。在Triton B的作用下,2-甲基-1,3-环己二酮能与碘甲烷发生亲核取代反应生成2,2-二甲基-1,3-环己二酮。2-甲基-1,3-环戊二酮在 Triton B 的作用下可以生成碳负离子,然后与烯丙基醇结构单元中的叔羟基发生 Sn2 取代反应。该反应能够实现 1,3-二酮的 C-烷基化,已经用于类固醇化合物的合成。
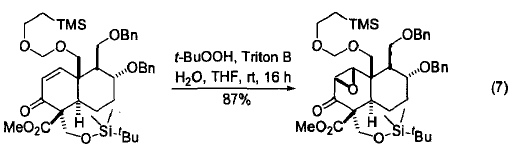
Triton B与叔丁基过氧化氢共同作用能够实现α,β-不饱和酮的环氧化反应,该反应已经在印楝素全合成中得到应用。
1. Sypniewski, M.; Penke, B.; Simon, L. Rivier, J. J. Org. Chem. 2000, 65,6595.
2. Younes, M. R-;Chaabouni, M. M.; Baklouti,A, Tetrahedron Lett. 2001,42,3167.
3. Ishikawa, T.; Mizuta, T.; Hagiwara, IC; Aikawa, T.; Kudo, T.; Saito, S. J. Org. Chem. 2003,68, 3702.
4. A versa, M. C.;Barattucci, A.; Bilardo, M. C.; Bonaccorsi, P.; Giannetto, P.; Rollin, P.; Tatibouet, A.J. Org. Chem. 2005, 70, 7389.
5. Aucagne, V.; Aversa, M. C.; Barattucci, A.; Bonaccorsi, P.; Giannetto, P.; Rollin, P.; Tatiboua, A. J.Org. Chem. 2002, 57, 6925.
6. Aversa, M. C.; Barattucci, A.;Bonaccorsi, P. Tetrahedron Lett. 2008, 64, 7659.
7. Yamazaki, Y,; Araki, T.; Koura, M.; Shibuya, K. Synthesis 2008,1017.
8. Mori, K.; Mori, H. Org. Synth. 1989, 68, 56.
9. Ananchenko, S. N.; Torgov, I. V. Tetrahedron Lett. 1963,4, 1553.
10. Ananchenko, S. N.; Limanov, V. Ye.; Leonov, V. N.; Rzheznikov, V. N.; Torgov, I. V. Tetrahedron1962,18,1355.
11. Yang, N. C.; Finnegan, R. A. J. Am. Chem. Soc. 1958,80,5845.
12. Nicolaou, K. C.; Sasmal, P. K.; Roecker, A. J.; Sun, X.-W.; Mandal, S.; Converso, A.; Angew. Chem.,Int. Ed. 2005, 44,3443.
现货优势供应:邻苯二乙醚,氯甲醚三苯基鏻,邻苯二甲醚,醋酸叔丁酯,无水乙醇,三氯乙烯,二硫化碳,焦亚硫酸钠,亚硫酸氢钠,三氯氧磷,邻二氯苯,邻甲苯胺,3-氯丙烯,一氯丙酮,正癸酸,正丁醚,二甘醇胺,@烯基磺酸钠,十二烷基硫酸钠,十二烷基硫酸钾,十二烷基硫酸锂,月桂酸甲酯,DMF-DMA,四氯乙烯,邻二甲苯,元明粉,大苏打,三苯基乙基溴化磷,甲基丙烯酸酐,对苯乙烯磺酸钠,异癸醇,对氯甲苯,三氟化硼乙醚,2-氯丙烷,二苯硫醚,二氧化硫脲,丙烯酸叔丁酯,丙烯酸甲酯,四氢呋喃,异丙胺,1-辛烯,正十二烯,无水叔丁醇,仲丁醇,三甲胺盐酸盐,一氯丙酮,亚磷酸二乙酯,亚磷酸二甲酯,亚磷酸三甲酯,水杨酸,苯酚,氯磺酸,苯磺酰氯,苯亚磺酸钠,对硝基苯胺,3-氯丙酰氯,四丙基溴化铵,四丙基氢氧化铵,三苯基甲基溴化磷,四丁基溴化铵,四乙基溴化铵,四乙基氯化铵,丙二醇丁醚,四丁基硫酸氢氨,苄基三乙基氯化铵,3-巯基丙酸,氧氯化锆,N-乙基咔唑,氯化锌,联苯二氯苄,,丙二醇丁醚,环氧丙烷,丙酰氯,乙酰氯,甲氧基乙酸,碘化钾
合作热线:13355218884
现货优势供应:邻苯二乙醚,氯甲醚三苯基鏻,邻苯二甲醚,醋酸叔丁酯,无水乙醇,三氯乙烯,二硫化碳,焦亚硫酸钠,亚硫酸氢钠,三氯氧磷,邻二氯苯,邻甲苯胺,3-氯丙烯,一氯丙酮,正癸酸,正丁醚,二甘醇胺,@烯基磺酸钠,十二烷基硫酸钠,十二烷基硫酸钾,十二烷基硫酸锂,月桂酸甲酯,DMF-DMA,四氯乙烯,邻二甲苯,元明粉,大苏打,三苯基乙基溴化磷,甲基丙烯酸酐,对苯乙烯磺酸钠,异癸醇,对氯甲苯,三氟化硼乙醚,2-氯丙烷,二苯硫醚,二氧化硫脲,丙烯酸叔丁酯,丙烯酸甲酯,四氢呋喃,异丙胺,1-辛烯,正十二烯,无水叔丁醇,仲丁醇,三甲胺盐酸盐,一氯丙酮,亚磷酸二乙酯,亚磷酸二甲酯,亚磷酸三甲酯,水杨酸,苯酚,氯磺酸,苯磺酰氯,苯亚磺酸钠,对硝基苯胺,3-氯丙酰氯,四丙基溴化铵,四丙基氢氧化铵,三苯基甲基溴化磷,四丁基溴化铵,四乙基溴化铵,四乙基氯化铵,丙二醇丁醚,四丁基硫酸氢氨,苄基三乙基氯化铵,3-巯基丙酸,氧氯化锆,N-乙基咔唑,氯化锌,联苯二氯苄,,丙二醇丁醚,环氧丙烷,丙酰氯,乙酰氯,甲氧基乙酸,碘化钾
合作热线:13355218884
12-羟基-4,7,10-三氧杂十二酸叔丁酯是一种有机中间体,可以通过不同的反应途径合成。一种方法是通过2,2'-(乙烷-1,2-二基双(氧基))二乙醇和丙烯酸叔丁酯一步反应制备得到。另一种方法是通过三甘醇单苄醚与丙烯酸叔丁酯两步反应制备得到。

将二缩三乙二醇(5.9g,39mmol,5.0equiv)的乙腈溶液中加入丙烯酸叔丁酯(1g,7.8mmol, 1.0equiv)和苄基三甲基氢氧化铵(TritonB)(121mg,0.29mmol,1.0equiv,40%水溶液),在室温下搅拌48小时。通过KMnO4显色确定反应是否完全,然后在旋转蒸发仪上除去溶剂。通过硅胶柱层析纯化,得到目标产物12-羟基-4,7,10-三氧杂十二酸叔丁酯1.6632g,产率为77%。
将2,2'-(乙烷-1,2-二基双(氧基))二乙醇(55.0mL,410.75mmol,3.0eq.)的无水四氢呋喃(200mL)溶液中加入钠块(0.1g)。搅拌混合物直至钠块消失,然后滴加丙烯酸叔丁酯(20.0mL,137.79mmol,1.0eq.)。将混合物搅拌过夜,然后在0℃下用盐酸(20.0mL,1N)淬灭。通过旋转浓缩除去四氢呋喃,加入盐水(300mL)并用乙酸乙酯(3×100mL)萃取。将有机层用盐水(3×300mL)洗涤,经无水硫酸钠干燥,过滤并浓缩,得到无色油状物(30.20g,79.0%产率)。ESI MS m/z:C13H27O6[M+H]+计算值278.1729,实测值278.1730。
第一步:将三甘醇单苄醚12.01g溶解在150ml无水四氢呋喃中,室温下加入60%氢化钠2.00g,回流反应1小时,反应液冷却至室温,加入丙烯酸叔丁酯6.41g,室温反应过夜。减压去除溶剂,柱层析纯化后得化合物34-1 6.21g。MS(ESI):369[M+Na]+。
第二步:将6.00g化合物34-1及10%钯炭1.50g加入60ml甲醇中,室温氢化过夜。反应液用硅藻土过滤,用甲醇20ml×3洗涤滤饼,滤液与洗涤液合并,减压浓缩,得化合物12-羟基-4,7,10-三氧杂十二酸叔丁酯4.54g。MS(ESI):279[M+H]+。
[1] [中国发明] CN202011016521.8 一种PROTAC小分子化合物及其应用
[2] [中国发明] CN201880098324.X 2,3-二氨基琥珀酰基偶联物连接子
[3] [中国发明] CN201910161658.3 一类具有降解Btk活性的化合物
近年来,随着科学技术的迅猛发展及分子肿瘤学、分子生物学技术的进步, 新抗肿瘤药物不断涌现,抗癌药物的研究与开发已进入一个崭新的阶段。氨鲁米特作为一种重要的抗癌药物,其合成方法备受关注。
简介:氨鲁米特 (Aminoglutethimide)3-乙基-3-(4-氨基苯基)-2,6-哌啶二酮,它首先是以抗惊厥药的形式出现的,由瑞士诺华(Novartis)公司开发,于1955 年投入市场。60年代,人们发现它能抑制肾上腺甾体激素的合成,起到“药物肾上腺切除的作用”,因而被用来替代肾上腺切除而治疗乳腺癌。由于它与他莫昔芬的作用机制不同,且无交叉耐药性,因而常用于二、三线内分泌治疗,并且取得了一定的疗效。氨鲁米特能减少雌激素对乳腺癌的促进作用,抑制肿瘤生长。作为导眠能的氨基衍生物,具有抑制肾上腺皮质激素合成的作用,通过阻断芳香化酶而抑制雌激素的生成,并能促进雌激素的代谢和消除,从而减少雌激素对乳腺癌的促进作用,抑制肿瘤生长;用于皮质醇增多症(柯兴综合征),抑制肾上腺皮质功能;用于绝经后或卵巢切除后的晚期乳腺癌,对雌激素受体或孕激素受体阳性患者疗效较好。氨鲁米特能抑制芳香酶,使肾上腺皮质额外的雄烯二酮不能转化为estrogen,还可抑制胆固醇转化为孕烯诺龙。 口服给药,经肝细胞色素P-450酶系统代谢为无活性产物。该药具诱导肝药酶作用,可加速自身代谢及dexamethasone、 theophylline、digoxin等的代谢。可用于姑息性治疗激素受体阳性的复发性晚期乳腺癌和转移性乳腺癌。主要适用于绝经后晚期乳腺癌,对乳腺癌骨转移有效,也可用于皮质醇增多症的治疗。
合成:
1. 外消旋体氨鲁米特的合成进展
1.1 苯乙腈作为初始原料合成外消旋体氨鲁米特
1986年Hartmann, R. W. & Batzl, Ch.等人提出了关于外消旋体氨鲁米特的合成方法。选苯乙腈为初始原料,在80℃下,氨基钠作碱和碘乙烷发生亲核取代反应,生成2-乙基苯乙腈即化合物1-2;化合物1-2在碱苄基三甲基氢氧化铵的作用下与丙烯腈发生Michael加成反应,二氧六环作溶剂合成了化合物1-3;化合物2-乙基-2-苯戊二腈在醋酸和浓硫酸的作用下,120℃高温下关环制得关键中间体3-乙基-3-苯基-2,6-哌啶二酮即化合物1-4;得到的3-乙基-3-苯基-2,6-哌啶二酮在-10℃,浓硝酸和浓硫酸作用下引入硝基官能团合成化合物1-5;接着对硝基进一步氨化(Pd/C, H2),制得目标产物氨鲁米特。

1.2 苯丙酮作为初始原料合成外消旋体氨鲁米特
1986年Daly, M. J. & Jones, G. W.等人提出了3-乙基-3-(4-氨基苯基)-2,5-哌啶二酮的合成路线。合成始于苯丙酮,在氨甲酸甲酯和乙醛作用下,苯作溶剂,苯丙酮与氰基乙酸乙酯通过加成、消除反应合成化合物 1-7;制得的化合物1-7在盐酸作用下与氰化钾反应制得2-乙基-2-苯丁二腈即化合物1-8;接着2-乙基-2-苯丁腈在酸性条件下水解为化合物1-9即2-乙基-2-苯丁二酸;然后2-乙基-2-苯丁二酸在尿素提供氮的环境下高温关环得3-乙基-3-(4-氨基苯基)-2,5-哌啶二酮即化合物1-10,化合物1-10再经过经典硝化、氨化反应得目标产物3-乙基-3-(4-氨基苯基)-2,5-哌啶二酮。

2. 手性氨鲁米特的合成进展
2.1 苯丙二酸作为初始原料合成手性氨鲁米特
Fadel, A. & Garcia-Argote, S.提出由苯丙二酸为原料合成手性氨鲁米特。苯丙二酸 (2-phenylmalonic acid)通过两步反应合成酯类化合物1-13,化合物1-13在PLE ( pig liver esterase ) 的作用下进行选择性的水解得到立体选择性化合物1-14,ee值为83%,多次重结晶后ee值达到97%。具有立体选择性化合物1-14与ClCOOMe在Et3N的碱性环境下形成混合酸酐,然后NaBH4对其进行选择性的还原得到立体选择性的化合物1-15,产率达 78%,为了进一步提高产率将ClCOOMe用(COCl)2替代,可以提高NaBH4对反应的选择性将产率提高到88%。化合物1-15中的手性基团伯醇通过Swern反应变为具有立体选择性的醛基化合物1-16。化合物1-16与(EtO)2P(O)CH2CO2Et作用发生了Witting-Horner反应生成了含有烯烃基手性化合物1-17,手性化合物 1-17随后经过加氢、水解、关环后得到目标产物1-20。

2.2 对硝基氯苯作为初始原料合成手性氨鲁米特
曾经有文献报道可以通过多次重结晶来提高产品的立体选择性,但重结晶对物质立体选择性的构型不能有效控制,故Bunegr, M. J.等人在不断探索的 基础上提出了一种安全、高效、可控的合成具有立体选择性的R型氨鲁米特的 路线。

参考文献:
[1]孙贵生. 氨鲁米特及其中间体的合成研究[D].西北师范大学,2012.
[2]王翠融.国产新药—氨鲁米特[J].中国新药杂志,1993(05):31-33.