赖诺普利是一种广泛用于治疗高血压和心力衰竭的重要药物,其合成方法备受关注。本文将详细介绍合成赖诺普利的几个主要策略和步骤,为读者提供了制备这一药物的全面指南。
背景:到目前为止,赖诺普利虽是高血压病及充血性心力衰竭治疗的二线药物,但据2012年世界 销售统计,心血管系统药物销售额在400亿美元,ACEI药物占心血管系统药物销售额的 18.2%,其中,赖诺普利销售额为4.2亿美元。并且 赖诺普利具有治疗效果好,价格便宜,安全性高等特点。国内一些企业和研究机构在已有的赖诺普利合成方法上分析合成工艺上的优劣,进一步对其合成工艺进行优化研究,以求进一步降低成本,提高利润,扩大市场占有率,给人民带来福利。
合成:
1. 氨醛缩合法
1992年,文献报道了三条赖诺普利的类似合成路线,分别是路线C、路线D、路线E。以3-苯基丙醛和三氟乙酰赖氨酸为原料,经过氨醛缩合、脱水缩合活化、取代、水解 脱保护4步合成赖诺普利。结果表明,路线D反应收率最高,路线C反应收率最低。但三条反应路线中氨醛缩合反应和取代反应过程收率仍非常低,需要进一步提高转化率。氰化钠和光气的使用,增加了实验后处理的难度和成本。


2. 亲核取代法
以4-苯基丁酸乙酯衍生物为原料或中间体,通过取代、脱保护等反应合成赖诺普利,为合成 赖诺普利开辟了一条新的合成途径。
2.1 合成路线一:1989年,Iwasaki等以3-苯基丙醛为原料,经过缩合、水解、卤代、酯化、取代、脱保护反应生成赖诺普利。本法采用了生物合成法,在乙内酰脲酶的催化下,选择性地水解酰胺键,生成手性化合物,收率为99.3%,节省了物料,易于后处理。且革除还原胺化反应和氨醛缩合反应以取代反应代替。但此反应的关键是总收率低,特别是第一步反应只有45%,还需要进一步研究,以提高反应收率。

2.2 合成路线二:该方法以经保护的赖氨酸衍生物与2-三 氟甲硫酰氧基-4-苯基丁酸乙酯为中间体,通过两步取代反应、缩合反应、水解生成赖诺普利。该法的创新点在于2-三氟甲硫酰氧基-4-苯基丁酸乙酯2位上三氟甲硫酰氧基的引入,提高了取代反应的收率,收率由60%提高到 80%以上;第四步中上脯氨酸的过程也采用取代反应,收率也能达到80%以上。但此合成工艺路线中,二硫化二苯并噻唑和三苯基磷的使用,给实验带来了一定的危险性,且该步收率低,成本较高。最后一步水解反应,收率也较低,只有 50%。所以,该工艺路线的关键在于如何提高此两步的收率。

3. 迈克尔加成法
该方法是以4-苯基-4-氧代-2-丁烯酸乙酯与三氟乙酰赖氨酸为关键中间体,在碱的催化下,通过迈克尔加成反应合成赖诺普利,又为合成赖诺普利开辟了一条新的合成通道。迈克尔加成得到的产物可以不经过处理,直接进行催化加氢反应,操作简单,更符合现代环保低碳的理念。然而,该合成路线的反应第一步选择性和收率较低,提高选择性和收率难度较大。这可能是因为苯酯衍生物2位上的正电性较弱及反应过程中位阻效应较大。另外,催化氢化体系组成较复杂,必然影响Pd/C催化剂的使用寿命。

参考文献:
[1]刘斌,施介华.赖诺普利的合成研究进展[J].浙江化工,2016,47(07):10-17.
[2]吴健龙,唐敏华,方元文.赖诺普利合成新工艺研究[J].江西化工,2008(04):135-137.DOI:10.14127/j.cnki.jiangxihuagong.2008.04.017.
赖诺普利是一种第三代血管紧张素转换酶抑制剂,被广泛用于治疗高血压和心力衰竭。自1987年在美国批准上市以来,赖诺普利已成为临床应用的重要药物,每年超过6000万处方中都含有赖诺普利。除了用于高血压和心力衰竭的治疗,赖诺普利还可以提高急性心肌梗死的存活率。

赖诺普利是一种血管紧张素转换酶(ACE)抑制剂,主要用于治疗高血压和心力衰竭。赖诺普利的使用可能会导致血清转氨酶轻度升高,并且在极少数情况下可能会引发急性肝损伤。
赖诺普利与其他血管紧张素转换酶抑制剂的作用机制相似,可以抑制血管紧张素I转换为血管紧张素II。血管紧张素II是肾素-血管紧张素系统中调节血管收缩和体液容量的主要调节剂。除了抑制血管紧张素I-II转化酶外,赖诺普利还可能抑制其他转化血管紧张素II的酶,这也是血管紧张素转换酶抑制剂可能引起副作用的原因之一。
赖诺普利的商品名包括心宁卫(Prinivil)和捷赐瑞(Zestril),片剂规格有2.5、5、10、20、30和40 mg等多种。建议成人的初始剂量为每日5至10 mg,根据血压反应和耐药性逐渐调整剂量。平均维持剂量为每日20至40 mg,最大剂量为每日80 mg。对于心力衰竭和急性心肌梗塞的长期治疗,建议使用较低剂量。
常见的副作用包括头痛、眩晕、疲乏、嗜睡、恶心和咳嗽。停药的最常见原因是头痛和咳嗽。
较少见的副作用包括症状性低血压、直立性低血压、晕厥、心悸、胸痛、周围性水肿、血管神经性水肿、皮疹、皮炎、便秘、胃炎、肝细胞性或胆汁淤积性肝炎、肝硬化、焦虑、失眠、感觉异常、尿量减少或无尿、肾功能不全、急性肾衰竭、性功能障碍、关节痛、肌痛和哮喘等。
其他副作用包括血尿素氮、血肌酸酐、血清肝酶值和血钾(轻度)升高,血红蛋白和血细胞比容稍降低,以及蛋白尿(发生率为0.7%)。
如果在使用赖诺普利过程中出现任何不适,请及时咨询医师或药师。如果不适严重或无法缓解,请及时就医。
赖诺普利是一种常见的降压药,被广泛应用于临床治疗高血压等疾病。作为一种原料药,赖诺普利的采购需要特殊的注意和技巧。本文将介绍赖诺普利原料药采购的相关知识和技巧。
一、了解市场行情
在进行赖诺普利原料药采购前,首先需要了解市场行情。通过了解市场价格、供应商情况、物流等信息,可以帮助你做出更明智的决策。可以通过各种途径了解市场行情,比如参考行业报告、咨询供应商、了解竞争对手等等。
二、选择可靠的供应商
选择可靠的供应商是保证产品质量的关键。要尽量选择有资质、信誉度高的供应商,以保证所采购的赖诺普利原料药符合国家和相关规定的质量标准。可通过了解供应商的企业资质、产品生产工艺、质量管理体系等方面来评估供应商的能力和信誉度。
三、确保原料药质量
赖诺普利是一种高端的药品,原材料的质量对产品的质量影响很大。在采购赖诺普利原料药时,需要注意其质量标准。应该查看相关证件和检测报告,以确保所采购的原料符合国家、行业和公司的规定,并且能够满足所需的质量要求。
四、灵活谈判价格
在采购赖诺普利原料药时,价格也是一个重要考虑因素。可以通过与供应商进行谈判来争取更优惠的价格。了解市场价格,参考竞争对手的价格,适当压缩利润空间,找到供需双方都能接受的价格点。
五、合理库存管理
赖诺普利原料药的库存管理也非常重要。合理的库存管理可以较大程度地减少库存成本和风险。在进行库存管理时,需要掌握恰当的采购量、存储条件、保质期等信息,并建立科学的库存管理体系。
赖诺普利原料药采购需要从多个方面加以考虑。要注意市场行情、选择可靠的供应商、关注原料药质量、灵活谈判价格,以及建立合理的库存管理体系,才能保证赖诺普利产品的质量和生产效益。
准确检测药物中赖诺普利的含量对于质量控制和药物疗效评估至关重要。本文将介绍用于检测药物中赖诺普利含量的各种分析方法和技术,为读者提供了一系列可靠的定量分析方案。
背景:当前,国内外对赖诺普利在检测方法上的研究并不多,主要有高效液 相色谱法、气相色谱-质谱联用法、电化学法及液相色谱-质谱联用法等。
1. 有研究弱碱性条件 下,以玫瑰精B作探针,采用荧光分析方法来研究药物中赖诺普利含量的检测方法。
1.1 实验方法:准确移取3.00 m L pH 7.50的Tris-盐酸缓冲溶液于10 m L具塞比色管中,再加入2.00 m L 1.00× 10-4mol/LRHOB溶液和适量4.055 mg/L LNP标准溶液(或加适量样液),用水定容。15 min后,在荧光光谱仪上(设光电管负高压为400 V,激发和发射光谱通带为5 nm,λex /λem =556 nm/585 nm)扫描荧光曲线,测定585 nm处体系的荧光强度F和试剂空白的荧光强度F0,计算ΔF(ΔF=F-F0)。
1.2 实验条件优化:
(1)溶液酸度及用量:最佳酸度为pH 7.50,此时荧光增强强度ΔF相对最 大且基本稳定。当溶液酸度大于或小于pH 7.50 时,荧光增强强度均有不同程度降低。故用p H 7.50 Tris-盐酸缓冲溶液控制溶液的酸度,用量以 3.00 m L为宜。(2)RHOB溶液的浓度: 最适宜的RHOB溶液的浓度为2.00×10-5mol/L,此时体系的荧光增强强度ΔF相对最大且基本稳定,灵敏度相对最高。当RHOB溶液浓度小于或大于2.00× 10-5mol/L时,体系的荧光增强强度均有不同程度 的减弱,即灵敏度有所降低。故选用2.00 m L 1.00× 10-4mol/LRHOB溶液。
2. 有研究采用瑞利光散射(RLS)技术来研究赖诺普利的定量检测方法。
2.1 实验方法:准确移取一定量的40.55 mg·L-1赖诺普利标准溶液(或适量样液)于10 mL具塞比色管中,再加入1.00 mL pH 8.56 Tris-盐酸溶液和2.50 m L 1.00×10-4mol·L-1 亮绿溶液,用水稀至刻度。20 min后,以1 cm液池,在荧光仪上扫描上述溶液。(仪器参数:λex =λem =220 nm,测定狭缝5.0 nm),于370 nm处测定体系溶液及试剂空白溶液的 RLS强度IRLS 及I0,计算△IRLS =IRLS-I0。
2.2 实验条件优化:
(1)溶液酸度及用量:当溶液酸度大于或小于pH 8.56时,体系的△IRLS 均有不同程度的减弱,即灵敏度有所降低。继而考察了该最佳pH的用量对体系IRLS的影响,结果表明适宜用量为1.00 m L。故实验选用 1.00 m L pH 8.56 Tris-盐酸溶液来控制反应的酸度。(2)BLG溶液的浓度:最适宜的BLG溶液的浓度 为3.50×10-5mol·L -1 ,此时体系的△IRLS 相对最大且稳定,灵敏度相对最高。当BLG溶液的浓度大于或小于3.50×10-5mol·L -1 时,体系△IRLS均有不同程度降低,灵敏度有所降低。故实验用 1.00×10-4mol·L-1 BLG溶液3.50 m L。
3. 有研究用双波长叠加可见吸收光谱法来检测药物中赖诺普利的含量,具有比一般吸收光谱法更高的灵敏度(约高1个数量级)。实验步骤为:
3.1 溶液的配制
赖诺普利标准溶液:405.5 g/L 贮备液,冰箱4℃保存,临用时配成 40.55 mg/L。维多利亚蓝 B溶液:1.0X10-3mol/L。Tris 溶液:0.20 mol/L盐酸溶液:0.10 mol/L。Tris-盐酸溶液:取盐酸溶液和 Tris 溶液混合,用酸度计测定,配成 pH 3.5~8.5的系列溶液。
3.2 LNP溶液的标准曲线及相关参数
于10 mL比色管中,依次准确加入2.00mL 1.00X10-3mol/L 维多利亚蓝B溶液、150 mL pH 5.58 Tris盐酸缓冲溶液和0.20~1.80 mL 40.55 mg/L 赖诺普利标准溶液或样液,用水定容10 min 后,在紫外可见光谱仪上,用1cm 液池,以试剂空白作参比,在 420~780 nm 范围内扫描吸收光谱,用双波长叠加法测定体系溶液的吸光度.
3.3 样品的测定及回收试验
取某厂家生产的不同规格的赖诺普利片(简写为1#和2#)各5片,分别置于小烧杯中;另取某厂家生产的赖诺普利胶囊(简写为3#)5粒,将内容物置于另一小烧杯中。在各小烧杯中加适量水,搅拌,使赖诺普利溶解并过滤,滤液分别置于1000ml 容量瓶中,用水定容,即得1#~3#待测液。
取待测液1#、3#各0.50 ml,2#1.00 ml, 用双波长(DWO-VIS)法测定各样液中LNP的含 量(各平行测定5份),最后求出赖诺普利片剂及胶囊中LNP的含量。
参考文献:
[1]向杰,江虹,秦丽容.赖诺普利与维多利亚蓝B的显色反应及应用[J].化学世界,2020,61(01):38-42.DOI:10.19500/j.cnki.0367-6358.20180723.
[2]刘艳,王润莲,冉金凤等.亮绿与赖诺普利的瑞利散射光谱及应用[J].化学研究与应用,2019,31(04):722-725.
[3]何树华,冉金凤,王润莲等.玫瑰精B与赖诺普利相互作用及其荧光光谱分析与应用[J].现代化工,2019,39(02):235-237.DOI:10.16606/j.cnki.issn0253-4320.2019.02.053.
赖诺普利是一种适用于慢性疾病患者的药物,特别对于治疗高血压或充血性心力衰竭等有良好效果。不同患者在服用时需要注意用量或服用方法可能有所不同。
赖诺普利是第三代血管紧张素转化酶抑制剂,熔点为148摄氏度,建议存放在2-8摄氏度的环境中。外观上没有其他颜色。正确使用赖诺普利对于治疗高血压或抗高血压至关重要,且使用时间较长,起效迅速,每天一次即可。不同患者在服用时需要注意,建议口服,吸收率约为30%,生物利用率可达25%。服用2-4小时后会有明显效果,连续作用约2小时。为了更好地治疗高血压,建议每天一次,初始剂量为10毫克,之后可考虑增至20毫克。
在服用赖诺普利时,需要注意观察自身变化。连续或过量服用可能对肾功能产生影响,因此务必及时到医院进行肾脏检查。另外,在治疗充血性心力衰竭时,建议每天一次,初始剂量为2.5毫克,后期可逐渐调整,最大剂量不超过80毫克。
赖诺普利是一种常用的抗高血压药物,其合成方法多种多样。本文将专注于介绍使用还原胺化法合成赖诺普利的步骤和优势,为药物研究人员提供了制备这一药物的一种有效途径。
简介:赖诺普利(Lisinopril)是依那普利拉的赖氨酸衍生物,为第三代长效血管紧张素转化酶抑制剂(简称ACEI)类药物,能治疗高血压及其他心脑血管疾病。赖诺普利与其他抗高血压药物相比,它具有以下特点:一是亲水性强?对细胞亲合力大;二是药效持续时间长,降低收缩和舒张压的谷峰比高,降压作用比较平稳;三是唯一不经过肝脏代谢和生物转化即有活性的治疗高血压的药物,副作用小,于肝功能不全的高血压患者。目前,赖诺普利已成为治疗高血压的首选药物之一。
还原胺化法合成:1985年,文献报道以4-苯基-2-氧代丁酸或4-苯基-2-氧代丁酸乙酯为原料,通过还原胺化的方法合成赖诺普利。之后,相继出现了此路 线的改进合成方法,在提高收率,保护环境,降低成本上做了较多的工作。
1. 合成路线一
1985年,Wu等以N2-苄氧羰基-N6-叔丁氧羰基-L-赖氨酸(3)和脯氨酸苯酯盐酸盐(4)为原料,在DCC和三乙胺的作用下,缩合生成5,收率为79%,然后在10%Pd/C催化下氢化,得到中间体6,收率为78%。接着,中间体6与4-苯基-2- 氧代丁酸(7)在催化剂NaBH3CN作用下还原胺化,再经酸解得到赖诺普利(1)和其非对映异构 体(2)(S∶R比值为50∶50),收率为87%,赖诺普利 (1)的收率为26.8%。在该工艺路线中,由于3和4具有较大的空间位阻,阻碍了缩合反应的进行,从而影响了反应收率。氢化反应过程中,中间体5上的三个保护基团易脱去,生成具有两个伯氨基的副产物,增加了后续反应的反应竞争性。另外,还原胺化试剂为NaBH3CN的还原副产物HCN和NaCN均有剧毒,废渣与废液都必须经过严格的处理之后才能排放,环保成本高,选择性和收率都非常低,并且酸解过程采用 Dowex50(H+)离子交换技术,洗脱时需大量的2% 吡啶水溶液,操作相对复杂。该合成方法不符合低碳环保的要求,不适用于大规模的工业生产。

2. 合成路线二
2012年,江西迪瑞合成化工有限公司对上述方法进行了改进,提出了两种方案。 该工艺的特点是:(1)路线A和路线B中,用NaBH(OAc)3分别取代NaBH3CN和Raney Ni和 Pd/C,避免了NaBH3CN产生的HCN和NaCN毒性副产物,对环境友好,还原效率下降了2/3,但价格相应的也下降了2/3。并且使用NaBH(OAc)3 在常压下反应,相比Raney Ni和Pd/C,提高了收率和安全性,更节省了设备成本。(2)路线B中,采用双(三氯甲基)碳酸酯(BTC)取代COCl2合成中间体11,降低了合成过程中的控制难度,方便了运输和储存。路线A:中间体11收率为71.2%, 赖诺普利(1)收率为98%;路线B:中间体13收率 为75.6%,中间体11收率为85.7%。相比合成路线 一,路线A和路线B收率明显提高,选择性更好。

3. 合成路线三
1988年,Blacklock等以三氟乙酰赖氨酸为原料,与光气发生缩合反应,得到中间体8,8与脯氨酸盐取代反应,酸解得到中间体9。然后,在 Raney Ni的催化下,原料4-苯基-2-氧代丁酸乙酯(10)与9加氢还原胺化,生成中间体11和其非对映异构体(12),碱作用下水解得到赖诺普利与其非对映体异构物。该合成路线中, 中间体8和9收率分别为95%和94%,中间体 11收率为87.5%(11与12的S:R比值为95:5), 赖诺普利(1)的收率为76.6%。该法相对合成路线 一,产物的选择性和收率更高,废渣和废液处理容易,环保成本更低,适合大规模工业化生产。但该合成路线中第三步反应的收率还有提高的空间,Raney Ni成本较高,必须进行回收多次重复利用,达到低碳绿色环保的效果。

参考文献:
[1]刘斌,施介华.赖诺普利的合成研究进展[J].浙江化工,2016,47(07):10-17.
[2]吴健龙,唐敏华,方元文.赖诺普利合成新工艺研究[J].江西化工,2008(04):135-137.DOI:10.14127/j.cnki.jiangxihuagong.2008.04.017.
赖诺普利是一种血管紧张素转化酶抑制剂,主要用于高血压和充血性心力衰竭的治疗。赖诺普利D5可以用于相关的药理学研究。
赖诺普利D5是一种稳定同位素标记物。稳定同位素标记物可以作为一种非常优良的内标物,应用于药物代谢、生物分析以及临床研究等领域。
氘标记化合物的合成应尽可能选择简单容易的步骤引入带有氘原子的中间体,或选用廉价易得的氘代化合物作为原料,且引入的氘原子在反应中必须具有较高的稳定性,不易发生氘原子与氢原子的交换,以保证最终产物的同位素丰度。

南京工业大学王崴等人选择相对便宜的氘代苯(60)为原料,与马来酸酐经过傅克酰基化、酯化后得到化合物(62)。另一边,以赖氨酸(6)为原料,与三氟乙酸乙酯反应得到6位氨基被保护的化合物(7),与苄醇酯化后得到羧基被保护的化合物(40)。化合物(62)和化合物(40)发生迈克尔加成反应,经过柱色谱分离异构得化合物(63),钯碳氢化脱去苄基、还原苯甲酰基后与L-脯氨酸甲酯盐酸盐在羰基二咪唑(CDI)作用下缩合为化合物(65),碱水解后经强酸树脂游离得到赖诺普利D5(66),合成总收率为11%。
[1]王崴,陈礼勤. 氘标记赖诺普利的合成[C]. 中国化学会.中国化学会第27届学术年会第06分会场摘要集.中国化学会:中国化学会,2010:156.
引言:
N2-(1-乙氧羰基-3-苯丙基)-N6-三氟乙酰基-L-赖氨酸作为一种重要的有机化合物,在药物化学、生物化学等领域具有广泛的应用前景。然而,其合成路线较为复杂,涉及多个反应步骤。本文旨在探讨该化合物的高效合成方法,为相关研究提供参考。
简介:
N2-(1-乙氧羰基-3-苯丙基)-N6-三氟乙酰基-L-赖氨酸(LA2)是合成赖诺普利的关键中间体。
赖诺普利,是依那普利的赖氨酸衍生物,属于第三代长效血管紧张素转化酶(ACEI)抑制剂。主要通过抑制肾素一血管紧张素一醛固酮系统降低血压,同时赖诺普利亦对低肾素性高血压有降压作用。药效持续时间长.降低收缩和舒张压的谷峰比高,降压作用比较平稳,而且它口服吸收后不需经肝脏转化,对肝脏无损害作用,故对伴有肝脏疾病或肝功能有损害者就较其它药物优越。目前,赖诺普利已成为治疗高血压的首选药物之一。
合成:
宁衡等人以 3-苯甲酰丙烯酸乙酯(BZ)和三氟乙酰赖氨酸(LA1)为原料,在三氟甲磺酸三正丁胺盐催化作用下,经迈克尔加成反应、氢化还原反应合成赖诺普利关键中间体 N2-(1-乙氧羰基-3-苯丙基)-N6-三氟乙酰基-L-赖氨酸(LA2),总收率为 38.8%。LA2 加成物立体选择性可达到 84:16。该方法具有操作简单,收率高,是一条适合工业化生产的合成路线。具体步骤如下:
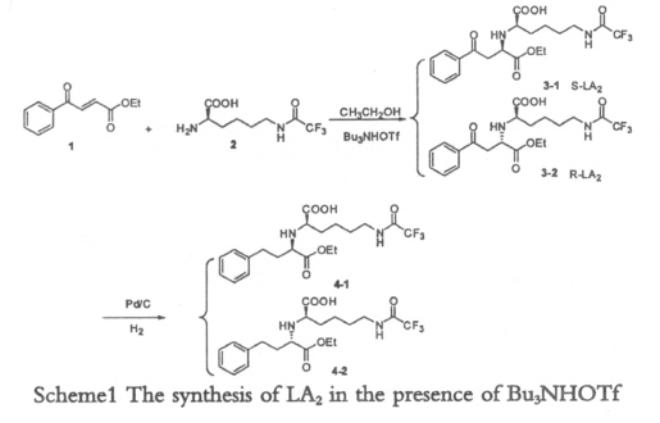
(1)加成反应过程
在一个配备机械搅拌器、温度计和恒压滴液漏斗的1000mL四口烧瓶中,加入41.7克(三氟乙酰赖氨酸,0.172摩尔)和38.6克(3-苯甲酰丙烯酸乙酯,0.189摩尔),并加入400毫升无水乙醇。将反应液冷却至-7℃,在搅拌下缓慢加入5.77克(三氟甲磺酸三正丁胺盐,0.16摩尔)。保持反应温度4小时,并通过薄层色谱(TLC,溶剂系统为CH2Cl2:CH3OH=10:1)监测反应进程。反应结束后,缓慢滴加5.0毫升浓盐酸。减压浓缩回收乙醇,类白色固体以少量冷乙醇洗涤过滤,40℃真空干燥,得N2-(1-乙氧羰基-3-苯丙甲酰基)-N6-三氟乙酰基-L-赖氨酸55.9g,收率为67%,LA2加成物S-构型与R-构型达到84:16,含量为92%。
(2)氢化反应过程
将上述的加成物55.9g与13.5g钯碳(含量为8%)混合加入到含400mL乙醇的高压氢化釜,控制温度在40℃,反应压力为0.2MPa,搅拌反应12h后结束反应,过滤回收钯碳。滤液加200mL水并使用适量的30%氢氧化钠溶液调节pH至4.5左右,保持真空条件浓缩回收乙醇。加100mL水洗后抽滤得到白色固体,50℃真空干燥,得N2-(1-乙氧羰基-3-苯丙基)-N6-三氟乙酰基-L-赖氨酸47.9g,收率58%,含量99%。
(3)HPLC条件
流动相为0.25%磷酸二氢钾溶液与乙腈(体积比6:4),色谱柱:VP-ODS5μm150×6.0mm柱温:30℃流速:1.0mL/min检测波长:210nm进样量:20μL。
参考:
[1] 苏州雅本化学股份有限公司. 一种具有高光学纯度的N2-[1-(S)-乙氧羰基-3-苯丙基]-N6-三氟乙酰基-L-赖氨酸的制备方法:CN201010294700.8[P]. 2011-02-16.
[2] 宁衡,谢媛媛,李坚军. 赖诺普利关键中间体的合成研究[J]. 浙江化工,2012,43(9):15-17,6. DOI:10.3969/j.issn.1006-4184.2012.09.004.
[3] 李剑,商永严,夏永明,等. 赖诺普利合成新工艺研究[Z]. 埃斯特维华义制药有限公司. 2011.