4-碘甲苯又被称为对碘甲苯、4-碘代甲苯、4-碘化甲苯,化学式为C7H7I。外观是一种无色或淡黄色的结晶固体,常温下不溶于水,但能溶于醇、醚、二硫化碳、苯等有机溶剂。它对皮肤、眼睛和粘膜有弱刺激性,高温下可燃。它主要用作生物制药和农药的中间体。此外,它还可以通过乌尔曼反应生成二甲基联苯的衍生物。

图一 4-碘甲苯
在压力管中,向选定的4-甲基苯硼酸(0.25 mmol)和硝酸钠(4.3 g,0.063 mmol)在无水乙腈(2 mL)中的溶液中加入PVP-I 2(1:1)(108 mg,0.3 mmol)。将反应混合物在80℃下剧烈搅拌所需时间。完成后,用二氯甲烷稀释反应混合物,通过硅藻土过滤,用更多二氯甲烷洗涤。滤液用饱和Na2S2O4溶液、饱和NaCl溶涤,并用无水Na2SO4干燥。通过1H NMR和13C NMR证实,在减压下除去溶剂得到纯的产物4-碘甲苯。将4-甲基苯硼酸(0.5 mmol)和K2CO3(1 mmol,138.0mg)加入到装有无磁性搅拌棒的20 mL Schlenk管中。将管子抽真空两次,并用氮气回填。在室温下,在氮气流下向管中加入MeCN(2 mL)和I2(0.75 mmol,191 mg),密封管并将其放入80°C的预热油浴中8-12小时。将所得溶液冷却至室温,加入H2O(10 mL)。用EtOAc(3×5mL)提取水层。对于产品2s和2t,在提取前将HCl(1M)加入水溶液中,直至pH值为2。将合并的有机相用无水Na2SO4干燥,过滤并通过旋转蒸发浓缩。通过硅胶柱色谱法纯化残留物,得到所需产物4-碘甲苯[1,2].
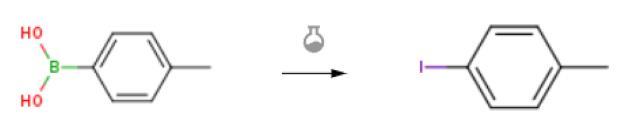
图二 4-碘甲苯的合成
在装有搅拌器、温度计和滴液漏斗的3L反应容器中,加入500 ml质量分数为70%的磷酸溶液、1.2 mol对甲苯胺,溶解C后将溶液温度降至6°,加入1.2 mol亚硫酸钾溶液于300 ml水中,将反应温度控制在18°C。加入后,反应持续15分钟,缓慢加入1.15 mol碘酸钠溶液于230 ml水中,溶液温度控制在35°C,搅拌速度控制在130 rpm,直至反应溶液中的气泡生成速率缓慢,然后将溶液温度调节至85°C,保持将温度降至无气泡产生,将溶液温度降至30°C,上层液体,剩余油中加入0.3mol亚硝酸钾,水层无色,加入50%质量分数的碳酸钠溶液300ml,溶液pH值为8-9,蒸汽蒸馏,直至无油物质,将溶液温度降至8°C,橙黄色晶体,过滤,2,2,2-三氟乙基甲醚洗涤,无水氯化钙脱水,4-碘甲苯243.29 G,收率93%[3].
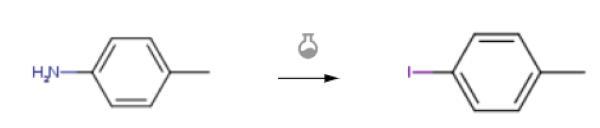
图三 4-碘甲苯的合成2
[1] Fu F , Gurung L , Czaun M ,et al.ipso-Bromination/iodination of arylboronic acids: Poly(4-vinylpyridine)-Br2/I2 complexes as safe and efficient reagents[J].Tetrahedron Letters, 2019, 60(38):151020.
[2]Niu L ,Zhang H ,Yang H , et al.Metal-Free Iodination of Arylboronic Acids and the Synthesis of Biaryl Derivatives[J].Synlett,2014,25(07):995-1000.
[3]彭响亮.一种甲氨蝶呤药物中间体对碘甲苯的合成方法[P].四川:CN201510982795.5,2016-04-20.
1,3-二甲基-5-碘苯是一种重要的有机化合物,具有广泛的应用前景,尤其在医药和化工领域具有重要意义。其独特的结构和化学性质赋予其多种潜在应用。
简述:1,3-二甲基-5-碘苯,英文名称:1-Iodo-3,5-dimethylbenzene,CAS:22445-41-6 分子式:C8H9I,外观与性状:透明淡黄色液体。
1,3-二甲基-5-碘苯(5-碘-间二甲苯)是芳基卤化物。在n-BuOH或DMF(溶剂)中,在NaI或KI存在下,通过铜催化卤素交换反应得到5-溴-间二甲苯。在CuFe2O4纳米粉作为可回收催化剂存在下,与苯酚反应生成1,3-二甲基-5-苯氧基苯。
1. 应用:
1,3-二甲基-5-碘苯适用于合成N-(3,5-芴基)-N-乙基苯胺,一种芳香胺。它可用于以下研究:
(1)酮的α-芳基化。
(2)铜催化的咪唑N-芳基化反应。。
(3)1,3-二甲基-5-碘苯的氰化形成3,5-二甲基苯并二氮杂卓。
(4)纳米CuFe2O4催化的苯酚与C-O交叉偶联合成1,3-二甲基-5-苯氧基苯。
(5)CuBr催化的1,3-二甲基-5-碘苯的胺化形成N-丙基-3,5-二甲基苯并二胺。
(6)1,3-二甲基-5-碘苯与硫醇之间的C-S键形成。
(7)作为合成联苯-3,3',5,5'-四羧酸的起始原料。
(8)N-溴丁二酰亚胺对1,3-二甲基-5-碘苯的自由基溴化形成1,3-双(溴甲基)-5-碘苯。
总的来说,1-碘-3,5-二甲苯是合成各种其他化学物质的重要组成部分。
2. 研究举例:
Xiaojie Wang等人以单齿N-杂环卡宾为辅助配体,制备了七个单体双(苯胺基)铁(II)配合物[(IPr2Me2)2Fe(NHAr)2](IPr2Me2 = 2,5-二异丙基-3,4-二甲基咪唑-1-亚基) ;Ar = Ph、C6H4-2-Pri、Mes、C6H3-2,6-Cl2、Dipp) 和 [(IPr)Fe(NHAr)2] (IPr = 2,5-二(2,6-二异丙基苯基)咪唑-1-亚基;Ar = C6H3-2,6-Cl2, Dipp), 是通过 [Fe(Mes)2]2 与相应的 N-杂环卡宾和苯胺的一锅反应制备的。这些高自旋二酰氨基配合物已通过 1H NMR、溶液磁化率、紫外-可见光、红外、X 射线衍射、循环伏安法以及元素分析进行了充分表征。N-杂环卡宾配体对亚铁中心的强亲和力以及NHC配体施加的空间保护是以单体方式稳定这些双(苯胺基)铁配合物的关键因素。反应性研究表明,四配位配合物[(IPr2Me2)2Fe(NHMes)2]可以与1当量的1-碘-3,5-二甲苯或1-溴-3,5-二甲苯在C6D6和THF-d8中反应,生成分别提供1-C6D5-3,5-Me2C6H3和5-D-1,3-Me2C6H3。在类似条件下,三配位化合物[(IPr)Fe(NHDipp)2]对这些卤化物呈惰性。
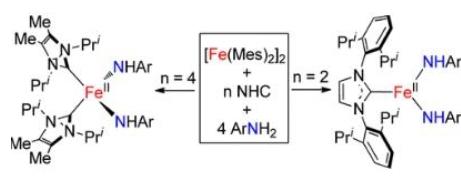
参考:
[1]Coles S J, Holmes R, Hursthouse M B, et al. Biphenyl-3, 3′, 5, 5′-tetracarboxylic acid[J]. Acta Crystallographica Section E: Structure Reports Online, 2002, 58(6): o626-o628.
[2]Wang X, Mo Z, Xiao J, et al. Monomeric Bis (anilido) iron (II) Complexes with N-Heterocyclic Carbene Ligation: Synthesis, Characterization, and Redox Reactivity toward Aryl Halides[J]. Inorganic Chemistry, 2013, 52(1): 59-65.
[3]https://www.scientificlabs.ie/product/halogenated-compounds/392510-25ML
4,4′-二甲基三苯胺是一种重要的三苯胺类衍生物,其合成与应用在有机化学领域具有广泛的研究价值。本文旨在探讨4,4′-二甲基三苯胺的有效合成方法以及其在化学合成中的应用。
简介:在三苯胺中,氮原子带有部分正电荷,因此具有一定的吸电子作用;三个苯环与中心氮原子通过C-C键相连,苯环周围可以连接不同型态的支链,因而三苯胺是优秀的接链母核。对于诸多的三苯胺衍生物来讲,其在空间光贮存、光纤应用、荧光材料等方面表现出优越的应用前景。通过对三苯胺上苯环支链进行官能团修饰,例如,卤代、烷基化、氧化、酰化等来制备三苯胺类衍生物,使其具备更突出的性能,尤其是制备一些光电子材料。
4,4′-二甲基三苯胺(4)是制备空穴传输材料的中间体。近年来,随着电子信息技术的飞速发展,有机光电材料在静电复印、激光打印和电子成像领域的应用越来越广泛。国内尚未实现此类材料的产业化,主要依赖进口。然而,文献中的方法大多采用碘苯或对溴碘苯法来合成4,这存在成本高、催化剂用量大以及后处理复杂等缺点。因此,改进制备空穴传输材料的中间体4的方法具有重要意义。
合成:
崔建兰等人以叔丁醇钾(t-BuOK, 3)为缚酸剂,在微波辐射下,4,4′-二甲基二苯胺(1)和溴苯(2)在二甲基亚砜(DMSO)中反应合成了4, 由正交实验确定最佳工艺条件为: 1 3 mmol, n(1) ∶n(2) ∶n(3)=1 ∶2 ∶2,微波功率100 W,于175 ℃反应60 min,收率67.8%。
具体步骤为:在专用压力反应管中加入1 590 mg(3 mmol)和3 670 mg(6 mmol)的DMSO(4 mL)溶液,滴加2 940 mg(5 mmol)的DMSO(4 mL)溶液,滴毕, 密封后放入微波反应仪中,用Discover专用软件设定反应条件(微波功率100 W,反应温度175 ℃,反应时间60 min)后开始反应。冷却后倒入水-甲苯中搅拌, 分液,有机相减压蒸馏,残余物用石油醚重结晶,干燥得白色晶体4 0.57 g,收率69.5%, m.p.112 ℃~113 ℃。
应用:
合成合成4,4'—二甲酸三苯胺。赵仑等人以4,4'—二甲基三苯胺为原料,在碱性条件下用高锰酸钾氧化,并加入相转移催化剂,最终合成4,4'—二甲酸三苯胺。通过对反应条件的研究,发现利用相转移催化合成4,4'—二甲酸三苯胺的最佳反应条件为:高锰酸钾用量7g,叔丁醇30ml,苄基三乙基氯化铵用量为0.50g,反应时间5.5h,此时产品产率最高达59.4%。
具体步骤为:称取4,4'—二甲基三苯胺3g(0.011mol),相转移催化剂苄基三乙基氯化铵0.5g,加入到三颈瓶中,再加入30ml叔丁醇和50ml水,通过滴加1%的氢氧化钠控制溶液PH在9~10之间,连接回流装置。在90℃加热回流反应,称取7g高锰酸钾(0.044mol),在5.5h内分批加入到反应瓶中。直到紫色基本褪去,冷却抽虑。用10ml水冲洗滤渣,收集滤液,并向其中滴加浓盐酸至PH为2~3,有大量白色沉淀物生成。抽滤,用少量水淋洗滤渣,烘干,称重,产品产率最高达59.4%。
参考文献:
[1]赵仑;邓青辉;吴志正;崔馨桐;牛茜. 苄基三乙基氯化铵为相转移催化剂催化合成4,4'—二甲酸三苯胺 [J]. 长春师范大学学报, 2014, 33 (06): 82-84.
[2]季全国;杨锋;哈伍族. 微波辐射合成4-溴-4',4″-二甲基三苯胺 [J]. 广州化工, 2011, 39 (17): 59-60+85.
[3]崔建兰;蔡剑波;曹端林;刘璐. 微波辐射合成4,4′-二甲基三苯胺 [J]. 合成化学, 2008, 16 (06): 696-697+704.
6-碘-4(H)-喹唑啉酮作为合成拉帕替尼的重要中间体,具有广泛的应用潜力。
简述:6-碘-4(H)-喹唑啉酮,英文名称:6-Iodo-4-quinazolinol,CAS:16064-08-7,分子式:C8H5IN2O,密度:2.11 g/cm3,折射率:1.779。6-碘喹唑啉-4-酮是合成拉帕替尼的重要中间体。
应用:
1. 合成拉帕替尼二对甲苯磺酸盐一水合物
拉帕替尼二对甲苯磺酸盐一水合物(lapatinib ditosylate monohydrate),商品名为Tykerb,化学名为N-[3-氯-4-[(3-氟苯基)甲氧基]苯基]-6-[5- [[[2-(甲磺酰基)乙基]胺基]甲基]呋喃-2-基]-4- 喹唑啉胺二(4-甲基苯磺酸)盐一水合物,是一种新型的分子靶向抗肿瘤药,由葛兰素史克公司于 2007年在美国率先上市,用于联合用药。
以6-碘喹唑啉-4-酮(3)为起始原料,依次经氯化反应(收率88%)、与5-甲酰基呋喃-2-硼酸的Suzuki偶联反应(收率96%)、与2-(甲砜基)乙胺的还原胺化(收率 94%)、与一水合对甲苯磺酸成盐(收率87%)和四氢呋喃-水(8∶2)结晶(收率70%)等5步操作制备目标产物拉帕替尼二对甲苯磺酸盐一水合物,总收率 48%。合成路线如下:
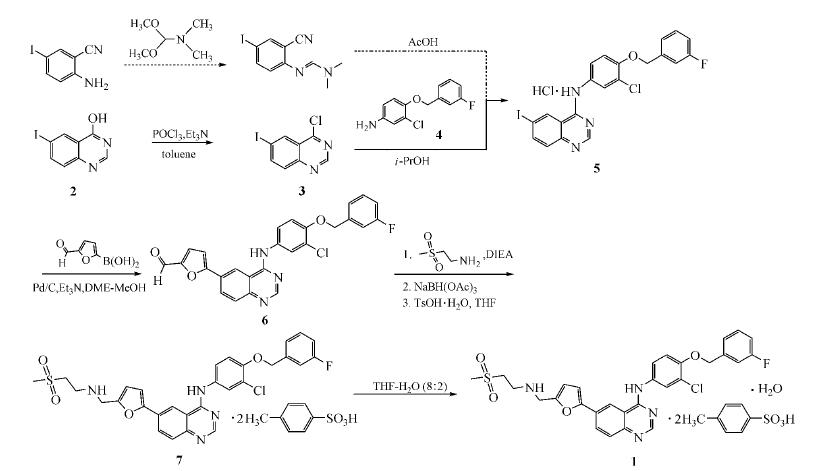
其中,4-氯-6-碘喹唑啉(3)以6-碘-4(H)-喹唑啉酮为原料合成,具体实验步骤如下:向50 mL三颈瓶中投入6-碘喹唑啉-4-酮(2)(5.44 g,20 mmol)、氧氯化磷(3.68 g,24 mmol)和无水甲苯 (16 mL),在氮气保护下,滴加三乙胺(2.43 g,24 mmol),滴完后升至77℃保温搅拌2.5 h。将所得反应物冷至2℃搅拌1 h后,抽滤。滤饼用丙酮洗涤后,再在1 mol/L氢氧化钠水溶液(26 mL)中室温搅拌洗涤30 min。抽滤,依次用水和丙酮洗涤,真空干燥得灰褐色结晶性固体(3,5.11 g,88%):mp 176.0~177.5℃。
2. 合成具有潜在的抗肿瘤活性的喹唑啉类衍生物
金正盛等人以6-碘喹唑啉-4-酮为原料,经氯代、胺化、Suzuki偶联、Wittig-horner等反应合成了7个新型的4-取代苯胺喹唑啉衍生物(5a~5g)。具体实验步骤如下:
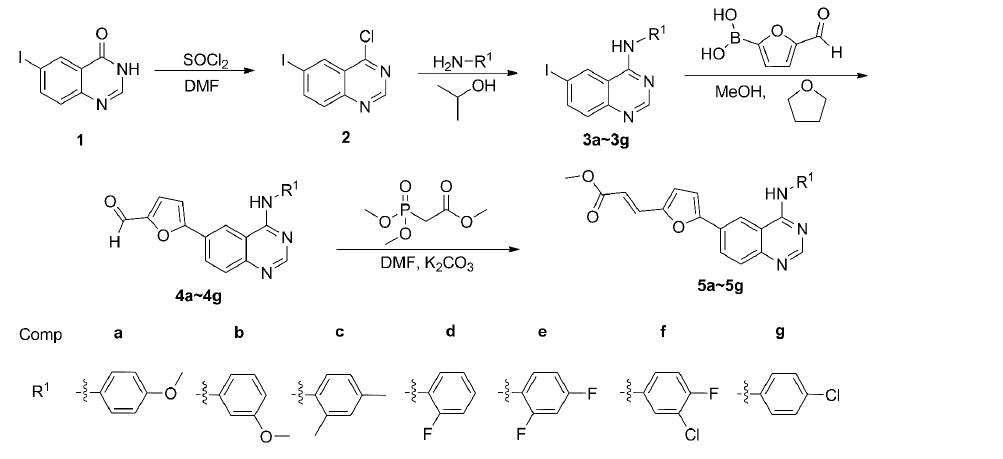
3a~3g的合成(以3a为例):将10.50 g(1.84 mmol),二氯亚砜6 mL和 N,N-二甲基甲酰胺0.25 mL加入圆底烧瓶中,搅拌下回流反应1 h。减压蒸除溶剂得中间体2,加入异丙醇10 m L和对甲氧基苯胺0.25 g(2.03 mmol),搅拌下回流反应约3 h。冷却至室温,抽滤,滤饼真空干燥后用甲醇溶解,用氨水调至pH 10,析出固体,抽滤,干燥得淡黄色固体6-碘-N-(4-甲氧苯基)喹唑啉-4-胺(3a)0.45 g,产率64.9 %。
参考文献:
[1]金正盛,蔡志强,方舒慧等. 新型4-取代苯胺喹唑啉衍生物的合成与抗肿瘤活性研究 [J]. 合成化学, 2018, 26 (06): 389-393+399. DOI:10.15952/j.cnki.cjsc.1005-1511.2018.06.17301.
[2]张庆文,周后元,尤启冬. 拉帕替尼合成工艺研究 [J]. 中国药科大学学报, 2010, 41 (04): 317-320.
3-(三氟甲氧基)碘苯是一种有机中间体,可通过重氮化反应从3-(三氟甲氧基)苯胺制备而得。

制备3-(三氟甲氧基)碘苯的方法如下:将NaNO2(7.4g,115.62mmol)的H2O溶液 (80ml)加入3-(三氟甲氧基)苯胺(17.7g,100.00mmol)中,然后在-5℃下逐滴加入H2SO4(25g,250.00mmol)。将所得溶液在-5℃维持15分钟。接着将KI (20g,120.48mmol)的H2O溶液(60ml)逐滴加入该溶液中,最后在室温下搅拌过夜并使用EtOAc(2×100mL)进行萃取。合并的有机层使用Na2SO3/H2O(2×50mL)洗涤,经过Na2SO4干燥和真空浓缩,最终得到4.0g(14%)的3-(三氟甲氧基)碘苯。
3-(三氟甲氧基)碘苯可用于制备钠离子通道抑制剂,该抑制剂对电压依赖性钠离子通道起到抑制作用。电压依赖性钠离子通道广泛分布于各类兴奋性细胞膜上,是电信号扩大和传导的主要介质。钠离子通道的异常可能导致神经疼痛、癫痫等疾病。因此,开发新型的钠离子通道抑制剂具有重要的临床意义。

3-(三氟甲氧基)碘苯可用于制备PPAR调节剂,该调节剂可以通过与PPAR应答元件结合来调节靶基因的表达。PPAR是一类重要的核受体,参与调节脂质代谢和脂肪形成的信号级联反应。因此,研究和开发PPAR调节剂对于治疗与脂质代谢相关的疾病具有潜在的临床应用价值。

[1] PCT Int. Appl., 2006055187, 26 May 2006
[2] PCT Int. Appl., 2019226687, 28 Nov 2019
[3] PCT Int. Appl., 2006055187, 26 May 2006
氟磺酰基二氟乙酸甲酯是一种有机中间体,可通过一步反应从四氟乙烷-β-磺内酯和甲醇制备而得。已有文献报道其可用于合成中间体5-氯-2-氟-4-(三氟甲基)苯胺盐酸盐和3-氯-6-三氟甲基哒嗪。


为了制备氟磺酰基二氟乙酸甲酯,首先在烤箱中干燥1000 mL的三颈圆底烧瓶,并加入磁力搅拌棒、恒压漏斗和出气口。将气体出口连接到一个空的500 ml备用阱,然后连接到位于1000 mL烧杯正上方的倒置玻璃漏斗出口,该烧杯中含有120 g NaOH溶解在600 ml水中。向烧瓶中加入无水甲醇(160 g)。在搅拌下通过加料漏斗向混合物中滴加四氟乙烷-β-磺内酯(440g)。用冰浴冷却混合物3小时。添加完成后,将反应混合物逐步加热至室温。将混合物在室温下搅拌过夜。用氮气吹气1小时以完全除去残留在系统中的HF后,用水(2×400 mL)和盐水(2×400 mL)洗涤所得的反应混合物,以除去残留的甲醇。收集有机相。用无水硫酸钠干燥有机相。过滤后,通过蒸馏纯化粗产物。
CN201710634979.1公开了一种新的合成方法,用于制备芳香含三氟甲基中间体5-氯-2-氟-4-(三氟甲基)苯胺盐酸盐。该方法包括以下步骤:1) 在无水乙醇溶液中,将5-氯-2-氟苯胺和碘单质进行碘代反应;2) 使用二氯甲烷作为溶剂,对得到的芳香碘代物进行乙酰化反应;3) 在80℃条件下,对乙酰基保护的芳香碘代物和氟磺酰基二氟乙酸甲酯进行三氟甲基化反应;4) 最后,使用6mol/L的盐酸在乙醇中进行脱乙酰化反应,得到目标产物。该方法具有新颖的路线设计,产品纯度高,操作简便安全。反应在溶剂中平稳进行,过程易于控制,粗品杂质少,易于提纯,提高了产品的质量和收率。总收率为66%,产品纯度可达98.5%,具有较高的研究开发应用价值。
CN201010619304.8提供了一种制备3-氯-6-三氟甲基哒嗪的方法。该方法包括以下步骤:将3-氯-6-碘哒嗪(2)与氟磺酰基二氟乙酸甲酯在催化剂的参与下,在90-110℃下进行三氟甲基化反应20-36小时,然后使用乙酸乙酯进行萃取并重结晶,最终制备得到3-氯-6-三氟甲基哒嗪(1)。与现有技术相比,该方法具有以下优点:1) 一步反应制备3-氯-6-三氟甲基哒嗪,反应收率高;2) 使用的催化剂为碘化铜和[1,1′-双(二苯基膦)二茂铁]二氯化钯二氯甲烷络合物,这些催化剂廉价易得,节约生产成本。
[1] Zhao G , Wu H , Xiao Z , et al. Trifluoromethylation of haloarenes with a new trifluoro-methylating reagent Cu(O2CCF2SO2F)2[J]. RSC Advances, 2016, 6.
[2] CN201710634979.1一种芳香含三氟甲基中间体5-氯-2-氟-4-(三氟甲基)苯胺盐酸盐的合成新方法
[3] CN201010619304.8一种制备3-氯-6-三氟甲基哒嗪的方法
中性红是一种多功能的组织学复染色染色剂,可用于溶酶体、高尔基体和尼斯尔氏粒的染色,并且还可以作为酸碱指示剂。
此外,中性红还是一种活体染剂,随着细胞逐渐死亡,细胞对中性红的吸收能力也会减弱。

中性红是一种弱碱性pH指示剂,其变色范围在pH6.4~8.0之间(由红变黄)。在中性或微碱性环境中,植物的活细胞能够大量吸收中性红并向液泡中排泌。由于液泡通常呈酸性反应,进入液泡的中性红会解离出大量阳离子,呈现樱桃红色。在这种情况下,原生质和细胞壁一般不会着色。而死细胞由于原生质变性凝固,细胞液无法维持在液泡内,因此,中性红染色后不会产生液泡着色现象。相反,中性红的阳离子会与带有一定负电荷的原生质及细胞核结合,使原生质与细胞核染色。
中性红是通过N,N-二甲基对亚硝基苯胺盐酸盐与甲苯-2,4-二胺反应制取而成。
具体制备方法如下:将二甲基苯胺加入5℃的盐酸水溶液中,搅拌溶解后,再加入亚硝酸钠水溶液进行反应,反应温度控制在5~10℃。搅拌反应1小时后,过滤并用少量水洗涤得到对亚硝基二甲基苯胺盐酸盐。将硫酸亚铁溶解于90℃的热水中,然后加入2,4-二氨基甲苯,充分搅拌溶解后,慢慢加入制得的对亚硝基二甲基苯胺盐酸盐,进行搅拌反应。1小时后,补加适量盐酸,过滤。将滤液通入氯化氢气体,静置,待结晶完全后过滤、干燥,即可得到中性红成品。
1.中性红可用作酸碱指示剂,其变色范围为pH值6.8(红)~8.0(橙黄)。此外,它还可以作为氧化还原指示剂以及活体和细胞的染色剂。
2.中性红还可用于萃取光度法测定碘、汞等物质。同时也被广泛应用于生物染色。
三氟甲硫基苯胺是一种常用的农药制造中间体,具有杀虫剂和杀螨剂等作用。
制备三氟甲硫基苯胺的方法有多种,其中一种方法是在对4-氨基苯硫酚与三氟碘甲烷反应时,加入氨并进行UV照射。然而,这种方法需要复杂的UV照射装置和制造设备,不适合工业生产。

三氟甲硫基苯胺的结构
将三氟甲硫基苯胺、氢溴酸和水加入容器中,滴加亚硝酸钠水溶液。在另一个容器中加入氢溴酸和铜粉,形成铜盐溶液,然后将铜盐溶液加入前一个容器中,经反应后提取三氟甲硫基溴苯。
A.制备三氟甲硫基硝基苯
在装有回流冷凝管、温度计和磁力搅拌装置的250ml三颈瓶中,加入对溴硝基苯、乙腈和甲硫醇钠,升温至回流并搅拌反应,直至反应结束。蒸馏回收乙腈,然后将残余液倒入水中,过滤收集固体,洗涤干燥,得到三氟甲硫基硝基苯。
B.制备三氯甲硫基硝基苯
在装有回流冷凝管、温度计和磁力搅拌装置的500ml三颈瓶中,加入对甲硫基硝基苯、四氯化碳和催化剂偶氮二异丁腈,升温至60℃并通入氯气,反应结束后蒸馏回收四氯化碳,然后将残余液倒入水中,过滤收集固体,洗涤干燥,得到三氯甲硫基硝基苯。
C.制备三氟甲硫基硝基苯
在高压反应釜中,加入三氯甲硫基硝基苯和1,2-二氯乙烷,通入无水氟化氢并加热反应,反应结束后蒸馏回收1,2-二氯乙烷,然后减压蒸馏,收集馏分,得到三氟甲硫基硝基苯。
D.制备三氟甲硫基苯胺
在高压反应釜中,加入三氟甲硫基硝基苯、甲醇和雷尼镍,通入氢气并加热反应,反应结束后过滤除去催化剂,减压除去溶剂,减压蒸馏,收集馏分,得到三氟甲硫基苯胺。
[1] 凌青云, & 蒋仲良. 一种制备4-三氟甲硫基苯胺的方法.
[2] 徐佳斌, 陈品红, 叶金星, & 刘国生. (2015). 钯催化的芳基c—h键三氟甲硫基化反应. 化学学报, 73(12), 1294-1297.
[3] 吕昌武, 辜志峰, 柳一, 高靓, & 刘晋彪. (2017). 无金属催化芳基亚磺酸钠的三氟甲硫基化反应. 合成化学(10).
本文介绍了两种方法,用于合成对-正丁基苯胺。这两种方法在有机合成领域具有潜在的应用价值,并为相关研究提供了新的思路。
背景:对-正丁基苯胺是制备染料、农药、医药、光电材料及液晶显示材料的重要中间体。传统对-正丁基苯胺合成工艺主要以苯胺和正丁醇为原料,采用单质碘或氯化锌作催化剂进行烷基化反应。
具体合成:
1. 方法一:
(1)碘的乙醇溶液的制备
取碘化钾25g(加碘化钾是为了生成I3-以增加碘的溶解度),加水10mL溶解后,加碘25g及乙醇500mL,搅拌使溶解。
(2)对-正丁基苯胺的合成
用100mL量筒分别量取苯胺和正丁醇(物质的量比为1∶0.8)、用分析天平称取适量的碘化钾,将碘化钾装入高压釜,拧紧螺母, 加热,升温至220℃反应4h,再升温至280℃反应16 h,期间搅拌转速为30r·min-1。反应完成后,产物冷却至室温,即得。收率达到25.63%。
2. 方法二:
以溴化-1-J基-3-甲基咪唑离子液体和1-丁基-3-甲基-1H咪唑四氟硼酸盐室温离子液体作催化剂,由正丁醇和苯胺反应合成对-正丁基苯胺,在室温下2种离子液体可以催化合成对-正丁基苯胺,作为一种绿色催化剂,离子液体在烷基化中有较大研究空间。具体步骤如下:
(1)1-丁基-3-甲基溴代咪唑离子液体的制备
溴代正丁烷和N-甲基咪唑加入圆底烧瓶,加热套加热,冷却水回流,在85℃左右剧烈回流一次,瓶内液体由无色变为金色,并分层,继续加热回流2h,此时回流温度为110℃,瓶中分层液体上层白色浑浊为溴代正丁烷,下层为金色透明液,上层倒出(可回收),下层粘稠状金色液用乙酸乙酯洗涤3-4次,真空旋转蒸发,温度为75°,时间为8h。收得金色产物,即为1-丁基-3-甲基溴代咪唑离子液体。
(2)1-丁基-3-甲基-1H咪唑氯化物的制备
在三口烧瓶中加入N-甲基咪唑,乙腈,氯代正丁烷,加上温度计,通入氮气进行保护,加入搅拌和冷凝器,油浴加热,回流温度控制在75~80℃, 48 h后冷却至室温,75℃减压蒸馏,将剩下度淡黄色油状物溶解于干乙腈,用滴管缓慢滴加干乙酸乙酯,同时进行搅拌,此时会在三口烧瓶的搅拌处出现1-丁基-3-甲基-1H咪唑氯化物的晶核,程针状,并伴随剧烈放热,完全溶解于乙腈后,将液体在-18℃下冷冻24 h,出现白色片状结晶,真空抽虑,白色结晶真空干燥30℃,6 h后,得白色粉末装固体,即为1-丁基-3-甲级-1H咪唑氯化物。
(3)1-丁基-3-甲基-1H咪唑四氟硼酸盐室温离子液体的制备
将1-丁基-3-甲基-1H咪唑氯化物和六氟磷酸钾及70 m L蒸馏水加入圆底烧瓶中,室温搅拌,反应液分层,上层为有机相,有机相用水洗涤3次, 真空干燥后,再加入100 m L二氯甲烷和无水硫酸镁,静置一小时,然后30℃减压蒸馏2 h,得到浅黄色黏稠液体,即为1-丁基-3-甲级-1H咪唑四氟硼酸盐室温离子液体。
(4)催化合成对-正丁基苯胺
分别以1-丁基-3-甲基溴代咪唑离子液体及1-丁基-3-甲基-1H咪唑四氟硼酸盐室温离子液体作催化剂,催化合成对-正丁基苯胺。
参考文献:
[1]马琳. 碘催化合成对-正丁基苯胺的正交实验研究 [J]. 化学与生物工程, 2014, 31 (06): 31-33.
[2]马琳. 对-正丁基苯胺合成过程中绿色催化剂的初选 [J]. 化学与生物工程, 2014, 31 (01): 33-35.
[3]马琳. 离子液体催化合成对-正丁基苯胺的研究 [J]. 煤炭技术, 2011, 30 (04): 185-187.
[(4-(N,N-二甲氨基)苯基]二叔丁基膦是一种重要的有机膦类配体,广泛应用于合成天然产物、药物、功能材料、液晶分子以及生物活性化合物等领域。本文将介绍两种制备[4-(N,N-二甲氨基)苯基]二叔丁基膦的方法。
1. 在氩气保护下,向干燥反应器中加入1L甲苯。
2. 依次加入N,N-二甲基苯胺、4-二甲氨基吡啶、乙酸亚铜以及二叔丁基氯化膦。
3. 升温至120°C反应8小时。
4. 反应结束后加入1L水淬灭反应。
5. 萃取有机层,用无水硫酸镁干燥,过滤。
6. 减压蒸馏得到黄色固体。
7. 将黄色固体溶于1L正己烷中冷冻重结晶得到白色固体。
8. 得到[4-(N,N-二甲氨基)苯基]二叔丁基膦。
1. 取干燥的10L四口反应瓶,经干燥氮气充分置换。
2. 加入已除去表面氧化层的镁屑和无水四氢呋喃。
3. 滴加N,N-二甲基对氯苯胺的无水四氢呋喃溶液。
4. 加入碘粒,搅拌升温至50℃。
5. 待格氏反应引发后,停止加热。
6. 继续滴加N,N-二甲基对氯苯胺的无水四氢呋喃溶液,保持反应体系温度在60℃。
7. 反应1小时后,检测原料N,N-二甲基对氯苯胺的剩余量。
8. 反应体系降温至-30℃,加入催化剂氯化亚铜粉末。
9. 滴加二叔丁基氯化磷,控制反应温度在-30℃以下。
10. 升温至50℃反应3小时。
11. 得到[4-(N,N-二甲氨基)苯基]二叔丁基膦。
[1] 一种合成[4-(N,N-二甲氨基)苯基]二烷基膦的方法
[2] 一种二氯二叔丁基-4-二甲基氨基苯基膦钯的制备方法