 1
1
对苯二甲酸是苯二甲酸异构体中的一个,两个羧基处于苯环的对位,化学式为p-C6H4(COOH)2。对苯二甲酸是生产聚酯,尤其是聚对苯二甲酸乙二酯(PET)的原料。

对苯二甲酸呈白色细颗粒粉状物体,不溶于水、氯仿、醚、醋酸中,仅微溶于醇中。加热时升华而不熔化。
纯对苯二甲酸(PTA)是以上游芳烃联合装置生产的对二甲苯(PX)为原料,以醋酸为溶剂,在催化剂的作用下与空气中的氧气进行氧化反应,生成粗对苯二甲酸(CTA)。CTA进行加氢精制,去除杂质,再经结晶,分离,干燥,制得纯对苯二酸(PTA)产品。
精对苯二甲酸是用于生产聚酯切片、长短绦纶纤维等化纤产品和化工产品的原料。
一种从粗对苯二甲酸的液体分散体中纯化粗对苯二甲酸的方法,该粗对苯二甲酸的液体还含有选自未反应原料、溶剂、副反应产物和/或其他不希望物质的杂质,该方法包括:
过滤所述分散体,形成粗对苯二甲酸滤饼;
在140℃-190℃的高温下将该滤饼溶入选择性的无水、无毒、无腐蚀性和基本上不与对苯二甲酸反应的结晶溶剂中,形成溶液;
在所述的结晶溶剂中通过降低所述溶液的温度从该溶液中结晶纯对苯二甲酸;和从所述溶液中分离出结晶的纯对苯二甲酸;
其中在没有任何氧化步骤存在下生产所述的纯对苯二甲酸,并且其中4-羧基苯甲醛的含量不大于25ppm。
根据本发明,上述选择性结晶溶剂无水,无腐蚀性,基本上不与对苯二酸反应。优选该选择性结晶溶剂为N-甲基吡咯烷酮。该方法和设备以经济上具有吸引力的速度和只需较低基本投资及简易工艺的不苛刻的实施条件来制备用于生产聚酯树脂和其他产品所需纯度的纯对苯二酸。
CN1080253C
显示全部对苯二甲酸是苯二甲酸异构体中的一个,两个羧基处于苯环的对位,化学式为p-C6H4(COOH)2。对苯二甲酸是生产聚酯,尤其是聚对苯二甲酸乙二酯(PET)的原料。

对苯二甲酸呈白色细颗粒粉状物体,不溶于水、氯仿、醚、醋酸中,仅微溶于醇中。加热时升华而不熔化。
纯对苯二甲酸(PTA)是以上游芳烃联合装置生产的对二甲苯(PX)为原料,以醋酸为溶剂,在催化剂的作用下与空气中的氧气进行氧化反应,生成粗对苯二甲酸(CTA)。CTA进行加氢精制,去除杂质,再经结晶,分离,干燥,制得纯对苯二酸(PTA)产品。
精对苯二甲酸是用于生产聚酯切片、长短绦纶纤维等化纤产品和化工产品的原料。
一种从粗对苯二甲酸的液体分散体中纯化粗对苯二甲酸的方法,该粗对苯二甲酸的液体还含有选自未反应原料、溶剂、副反应产物和/或其他不希望物质的杂质,该方法包括:
过滤所述分散体,形成粗对苯二甲酸滤饼;
在140℃-190℃的高温下将该滤饼溶入选择性的无水、无毒、无腐蚀性和基本上不与对苯二甲酸反应的结晶溶剂中,形成溶液;
在所述的结晶溶剂中通过降低所述溶液的温度从该溶液中结晶纯对苯二甲酸;和从所述溶液中分离出结晶的纯对苯二甲酸;
其中在没有任何氧化步骤存在下生产所述的纯对苯二甲酸,并且其中4-羧基苯甲醛的含量不大于25ppm。
根据本发明,上述选择性结晶溶剂无水,无腐蚀性,基本上不与对苯二酸反应。优选该选择性结晶溶剂为N-甲基吡咯烷酮。该方法和设备以经济上具有吸引力的速度和只需较低基本投资及简易工艺的不苛刻的实施条件来制备用于生产聚酯树脂和其他产品所需纯度的纯对苯二酸。
CN1080253C
 1
1
盐酸万古霉素被广泛认为是一种“猛药”,在治疗多种疾病中发挥着重要作用。然而,如果使用不当可能会带来治疗效果下降和用药风险增加的问题。
盐酸万古霉素是第一个问世的糖肽类抗生素,作用于细菌的细胞壁。除了抗菌作用外,它还可以改变细胞膜的通透性、选择性的抑制RNA的合成。
虽然去甲万古霉素与万古霉素相似,但抗菌谱和作用略有不同。盐酸万古霉素主要用于革兰阳性球菌感染的治疗,尤其是耐甲氧西林金黄色葡萄球菌感染。
盐酸万古霉素可用于治疗MRSA、PNSP等耐药革兰阳性球菌引起的呼吸系统感染。
耐药葡萄球菌和肠球菌是医院内血流感染的常见病原菌,盐酸万古霉素是治疗的首选药物。
盐酸万古霉素也可用于感染性心内膜炎的治疗。
对于中枢神经系统感染,特别是MRSA感染,盐酸万古霉素是首选药物。
盐酸万古霉素也适用于治疗化脓性骨髓炎和成人化脓性关节炎。
链球菌和金黄色葡萄球菌引起的皮肤及软组织感染也可考虑使用盐酸万古霉素。
在外科手术预防中,盐酸万古霉素可以有效预防手术部位感染。
需要注意的是,盐酸万古霉素的治疗窗窄,药物监测可以提高治疗有效率并降低肾毒性的风险。在使用过程中应该引起重视,做好相关患者的药物监测。 显示全部
盐酸万古霉素被广泛认为是一种“猛药”,在治疗多种疾病中发挥着重要作用。然而,如果使用不当可能会带来治疗效果下降和用药风险增加的问题。

盐酸万古霉素是第一个问世的糖肽类抗生素,作用于细菌的细胞壁。除了抗菌作用外,它还可以改变细胞膜的通透性、选择性的抑制RNA的合成。
虽然去甲万古霉素与万古霉素相似,但抗菌谱和作用略有不同。盐酸万古霉素主要用于革兰阳性球菌感染的治疗,尤其是耐甲氧西林金黄色葡萄球菌感染。
盐酸万古霉素可用于治疗MRSA、PNSP等耐药革兰阳性球菌引起的呼吸系统感染。
耐药葡萄球菌和肠球菌是医院内血流感染的常见病原菌,盐酸万古霉素是治疗的首选药物。
盐酸万古霉素也可用于感染性心内膜炎的治疗。
对于中枢神经系统感染,特别是MRSA感染,盐酸万古霉素是首选药物。
盐酸万古霉素也适用于治疗化脓性骨髓炎和成人化脓性关节炎。
链球菌和金黄色葡萄球菌引起的皮肤及软组织感染也可考虑使用盐酸万古霉素。
在外科手术预防中,盐酸万古霉素可以有效预防手术部位感染。
需要注意的是,盐酸万古霉素的治疗窗窄,药物监测可以提高治疗有效率并降低肾毒性的风险。在使用过程中应该引起重视,做好相关患者的药物监测。
 1
1
1-戊烯-3-醇,英文名为1-Penten-3-ol,是一种烯丙醇类化合物,常温常压下为透明无色液体,具有特殊的果香味,常用于食品加工生产中。
1-戊烯-3-醇的分子结构包含末端的双键单元和一个活性醇羟基结构,赋予了它较高的化学反应活性,在有机合成和香料制备中具有重要地位。
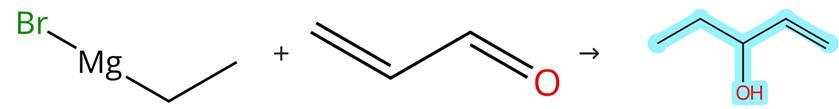
在一个干燥的反应烧瓶中将丙烯醛和溴乙基镁缓慢反应,经过一系列步骤得到目标产物分子。
1-戊烯-3-醇在食品香料、香精、有机合成等领域发挥着重要作用,是一种允许使用的食品用香料。
[1] Shakhmaev, R. N.; et al Russian Journal of General Chemistry (2009), 79(6), 1171-1174.
显示全部1-戊烯-3-醇,英文名为1-Penten-3-ol,是一种烯丙醇类化合物,常温常压下为透明无色液体,具有特殊的果香味,常用于食品加工生产中。
1-戊烯-3-醇的分子结构包含末端的双键单元和一个活性醇羟基结构,赋予了它较高的化学反应活性,在有机合成和香料制备中具有重要地位。

在一个干燥的反应烧瓶中将丙烯醛和溴乙基镁缓慢反应,经过一系列步骤得到目标产物分子。
1-戊烯-3-醇在食品香料、香精、有机合成等领域发挥着重要作用,是一种允许使用的食品用香料。
[1] Shakhmaev, R. N.; et al Russian Journal of General Chemistry (2009), 79(6), 1171-1174.
 1
1
水合铝酸碳酸镁,又被称为水滑石(LDHs),是一种层状离子化合物,其特征是由带正电荷的主体层板和层间阴离子通过非共价键的相互作用组装而成化合物,属于一类具有层状结构的无机材料。阴离子层位于氧化物层之间的空隙,通过电荷平衡与金属离子层相互吸引,使层状结构稳定。水分子与金属离子层和阴离子层之间形成氢键,存在于晶格间隙中。LDHs的化学通式一般表示为其中x的取值范围为0.2~0.33。M2+代表二价金属阳离子,包括Mg2+,Ni2+,Co2+,Zn2+,Cu2+等,M3+代表三价金属阳离子,包括Al3+,Cr3+,Fe3+,Sc3+等,An?是用来平衡非框架电荷的阴离子,包括Cl?,OH?,等无机和有机离子以及络合离子,层间无机阴离子不同,LDHs的层间距不同。由于其独特的层状结构,水滑石具有可控的主体层板的化学组成、层间客体阴离子种类和数量以及插层组装体的粒径尺寸和分布方面的特性。因此,水滑石种类繁多,在吸附、医药、催化、电化学、阻燃、光化学等领域具有广阔的应用前景。

水合铝酸碳酸镁
水合铝酸碳酸镁中,二价金属氧化物具有较强碱性,三价金属氧化物具有较弱酸性,层间的阴离子为弱酸根离子,导致水滑石整体分子成弱碱性,具有良好的吸酸效果。此外,水滑石的双层结构也导致水滑石具有优良的吸附效果和阴离子交换性能。水滑石应用在PVC等材料改性时,可以有效吸附其释放的游离酸,避免游离酸对于材料的进一步催化作用;水滑石类稳定剂还可以与游离酸发生层间阴离子置换反应,使其热稳定性大大提升。
现有技术,如CN202010475473.2,采用使用氢氧化镁作为镁源、氢氧化铝作为铝源,以二氧化碳作为碳酸根源,经过一段时间反应制备得到水合铝酸碳酸镁。但是其存在如下技术问题:1.以二氧化碳气体作为碳酸根源,容易导致水滑石的分层结构存在缺陷,影响水滑石的吸附效果和阴离子交换性能;2.镁源、碳酸根源来源单一,在实际使用生产线精确配比进行生产后,难以快速改变水滑石中镁和铝的比例;因此生产出来的产品其镁铝比例单一,酸碱性能固定,难以根据适用制品的不同,调整水滑石的性能。
张志勇[1]以氯化镁作为主要镁源,氢氧化铝作为铝源,二氧化碳作为主要碳酸根源;同时引入碳酸镁作为辅助镁源和辅助碳酸根源,反应后制得水合铝酸碳酸镁。
S1.将100g六水氯化镁、30g氢氧化铝、50g碳酸镁、2g氢氧化钠加入500mL水中,在98℃的条件下,高压反应1h;S2.在所述S1步骤反应完毕后,通入二氧化碳气体,调节反应液PH值至9?10,在110℃条件下继续高压2MPa反应11h;S3.对产物过滤、洗涤、烘干后得到水合铝酸碳酸镁。制得产品的镁铝比为2.05。
该方法使用碳酸镁作为辅助碳酸根源,相较于传统的使用二氧化碳气体作为碳酸根源的技术方案,可以形成优良的双层结构,碳酸根最大程度的稳定与层间,使产品具有良好的吸附性和阴离子交换性能,吸附酸性气体的性能优异。2.使用碳酸镁作为辅助镁源,可以单独通过调整碳酸镁的用量得到不同镁铝比的水滑石,从而达到调整水滑石酸碱性能的目的,以便使水滑石适用不同PVC、PP、PE制品。3.制作的水合铝酸碳酸镁纯度高,粒径分布均匀,具有良好的吸酸性能;此外,制作的产品热稳定性能强、抗老化性能好。4.制备工艺简单,并可以根据产品的参数要求进行快速调整,具有良好的市场应用效果。
[1]张志勇. 一种高纯镁铝水滑石的合成方法[P]. 山东省:CN116495761B,2023-09-12.
显示全部水合铝酸碳酸镁,又被称为水滑石(LDHs),是一种层状离子化合物,其特征是由带正电荷的主体层板和层间阴离子通过非共价键的相互作用组装而成化合物,属于一类具有层状结构的无机材料。阴离子层位于氧化物层之间的空隙,通过电荷平衡与金属离子层相互吸引,使层状结构稳定。水分子与金属离子层和阴离子层之间形成氢键,存在于晶格间隙中。LDHs的化学通式一般表示为其中x的取值范围为0.2~0.33。M2+代表二价金属阳离子,包括Mg2+,Ni2+,Co2+,Zn2+,Cu2+等,M3+代表三价金属阳离子,包括Al3+,Cr3+,Fe3+,Sc3+等,An?是用来平衡非框架电荷的阴离子,包括Cl?,OH?,等无机和有机离子以及络合离子,层间无机阴离子不同,LDHs的层间距不同。由于其独特的层状结构,水滑石具有可控的主体层板的化学组成、层间客体阴离子种类和数量以及插层组装体的粒径尺寸和分布方面的特性。因此,水滑石种类繁多,在吸附、医药、催化、电化学、阻燃、光化学等领域具有广阔的应用前景。

水合铝酸碳酸镁
水合铝酸碳酸镁中,二价金属氧化物具有较强碱性,三价金属氧化物具有较弱酸性,层间的阴离子为弱酸根离子,导致水滑石整体分子成弱碱性,具有良好的吸酸效果。此外,水滑石的双层结构也导致水滑石具有优良的吸附效果和阴离子交换性能。水滑石应用在PVC等材料改性时,可以有效吸附其释放的游离酸,避免游离酸对于材料的进一步催化作用;水滑石类稳定剂还可以与游离酸发生层间阴离子置换反应,使其热稳定性大大提升。
现有技术,如CN202010475473.2,采用使用氢氧化镁作为镁源、氢氧化铝作为铝源,以二氧化碳作为碳酸根源,经过一段时间反应制备得到水合铝酸碳酸镁。但是其存在如下技术问题:1.以二氧化碳气体作为碳酸根源,容易导致水滑石的分层结构存在缺陷,影响水滑石的吸附效果和阴离子交换性能;2.镁源、碳酸根源来源单一,在实际使用生产线精确配比进行生产后,难以快速改变水滑石中镁和铝的比例;因此生产出来的产品其镁铝比例单一,酸碱性能固定,难以根据适用制品的不同,调整水滑石的性能。
张志勇[1]以氯化镁作为主要镁源,氢氧化铝作为铝源,二氧化碳作为主要碳酸根源;同时引入碳酸镁作为辅助镁源和辅助碳酸根源,反应后制得水合铝酸碳酸镁。
S1.将100g六水氯化镁、30g氢氧化铝、50g碳酸镁、2g氢氧化钠加入500mL水中,在98℃的条件下,高压反应1h;S2.在所述S1步骤反应完毕后,通入二氧化碳气体,调节反应液PH值至9?10,在110℃条件下继续高压2MPa反应11h;S3.对产物过滤、洗涤、烘干后得到水合铝酸碳酸镁。制得产品的镁铝比为2.05。
该方法使用碳酸镁作为辅助碳酸根源,相较于传统的使用二氧化碳气体作为碳酸根源的技术方案,可以形成优良的双层结构,碳酸根最大程度的稳定与层间,使产品具有良好的吸附性和阴离子交换性能,吸附酸性气体的性能优异。2.使用碳酸镁作为辅助镁源,可以单独通过调整碳酸镁的用量得到不同镁铝比的水滑石,从而达到调整水滑石酸碱性能的目的,以便使水滑石适用不同PVC、PP、PE制品。3.制作的水合铝酸碳酸镁纯度高,粒径分布均匀,具有良好的吸酸性能;此外,制作的产品热稳定性能强、抗老化性能好。4.制备工艺简单,并可以根据产品的参数要求进行快速调整,具有良好的市场应用效果。
[1]张志勇. 一种高纯镁铝水滑石的合成方法[P]. 山东省:CN116495761B,2023-09-12.
 1
1
乙醇酸,又称甘醇酸或羟基乙酸,是一种α-羟基酸(AHAs),常被广泛应用于日化清洗、生物降解材料生产、皮肤医学和化妆品行业中。

溶解能力:对碱土金属垢污有良好的溶解能力,尤其与钙镁等化合物反应剧烈。
清洗范围:适用于清洗钙镁盐垢、铁锈和水垢,以及奥氏体钢材质的清洗。
操作方便:由于对材质的腐蚀性低,使用安全且操作方便,适用于各种设备和材料的清洗。
聚乳酸-乙醇酸(PLGA):是一种生物降解材料,应用广泛于医用领域,如缝合补强材料、药物缓释载体等。
治疗功效:对粉刺、老年斑、疣等皮肤问题有疗效,能促进皮肤更新。
渗透性:分子小、渗透力强,能够深层滋润皮肤,改善各种皮肤问题。
护肤功效:可以保湿、滋润肌肤,促进表皮更新,改善皱纹、黑斑、暗疮等问题。
角质调理:去除堆积的角质,加速皮肤更新,改善色素、疤痕和毛孔问题。
刺激性:使用后可能出现刺痛感和红肿,需注意防晒护理。
适用人群:孕妇、肌肤敏感者和青少年应避免使用高浓度乙醇酸产品。
通过以上应用和注意事项,乙醇酸在不同领域发挥着重要的作用,同时需注意正确使用以确保安全有效。 显示全部
乙醇酸,又称甘醇酸或羟基乙酸,是一种α-羟基酸(AHAs),常被广泛应用于日化清洗、生物降解材料生产、皮肤医学和化妆品行业中。

溶解能力:对碱土金属垢污有良好的溶解能力,尤其与钙镁等化合物反应剧烈。
清洗范围:适用于清洗钙镁盐垢、铁锈和水垢,以及奥氏体钢材质的清洗。
操作方便:由于对材质的腐蚀性低,使用安全且操作方便,适用于各种设备和材料的清洗。
聚乳酸-乙醇酸(PLGA):是一种生物降解材料,应用广泛于医用领域,如缝合补强材料、药物缓释载体等。
治疗功效:对粉刺、老年斑、疣等皮肤问题有疗效,能促进皮肤更新。
渗透性:分子小、渗透力强,能够深层滋润皮肤,改善各种皮肤问题。
护肤功效:可以保湿、滋润肌肤,促进表皮更新,改善皱纹、黑斑、暗疮等问题。
角质调理:去除堆积的角质,加速皮肤更新,改善色素、疤痕和毛孔问题。
刺激性:使用后可能出现刺痛感和红肿,需注意防晒护理。
适用人群:孕妇、肌肤敏感者和青少年应避免使用高浓度乙醇酸产品。
通过以上应用和注意事项,乙醇酸在不同领域发挥着重要的作用,同时需注意正确使用以确保安全有效。
 1
1
磷酸二苯酯(Diphenyl phosphate),分子式是C12H11O4P。外观呈白色结晶粉末状,可用于医药及化工生产领域。

图一 磷酸二苯酯
磷酸二苯酯的合成方法有很多种,介绍由苯酚和磷酸为起始原料合成的两种方法,具体如下:
将85%磷酸(461.2毫克,4.0毫摩尔)、苯酚(3.76克,40毫摩尔)、三乙胺(1.21克,12毫摩尔)、1-丁基咪唑(149.0毫克,1.2毫摩尔)和DMF(5毫升)放入由50毫升三颈烧瓶组成的反应装置中,该反应装置具有沸腾溶剂和水蒸汽流过的管子和溶剂通过脱水剂回流的管子。(见图S1)将2.0克作为干燥剂的PAdeCS置于冷凝器下方。将反应在230℃下加热24小时,此后,将所得混合物通过阳离子交换树脂(洗脱剂:甲醇)以除去胺。洗脱液蒸发后,混合物在低压下蒸馏除去苯酚和DMF。通过凝胶渗透色谱GPC(洗脱剂:CHCl3)获得所需的磷酸二苯酯,71%(619.6mg,2.84 mmol)[1]。
在氮气气氛中,加入1毫摩尔植酸(在第二实施例中调节或购自Nacalai Tescu有限公司,50重量%水溶液)、60毫摩尔苯酚(购自Nacalai Tescu有限公司)、18毫摩尔三乙胺(购自Nacalai Tescu有限公司)、3毫摩尔正丁基咪唑(购自Nacalaitescu有限公司)、N,N-二甲基甲酰胺(DMF,购自Nacalaitescu有限公司)并加入搅拌器磁铁。接下来,在将脱水装置连接到上述烧瓶后,将回流管作为冷却器连接到烧瓶的上部。将反应容器浸入油浴中并在230℃下以200 rpm反应24小时。2克2.5-5毫米的PAdeCS(注册商标,由日本混凝土工业有限公司制造)用作脱水材料。反应后,通过1H NMR、13C NMR和31P NMR确认目标磷酸二苯酯的形成。反应后的混合物溶解在甲醇中,并以1毫升/分钟的流速流向阳离子交换树脂(H型)(DOWEX 50 W×2 100-200目(H)阳离子交换树脂)。将所得溶液的溶剂在减压下蒸馏掉,然后在120℃和1.6×102Pa下在kugel辊中减压蒸馏以获得作为目标产物的残余物。将其再次倒入阳离子交换树脂中并纯化。减压除去溶液后,获得白色固体,磷酸二苯酯产率为65%(3.9毫摩尔)[2].
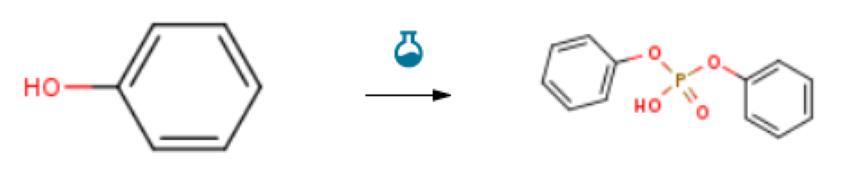
图二 磷酸二苯酯的合成
[1]Chi C T ,Kazuya A ,Takeshi S , et al.Synthesis of diaryl phosphates using orthophosphoric acid as a phosphorus source[J].Tetrahedron Letters,2022,96.
[2]YUKI N ,KAZUHIKO S ,YUMIKO N .ORGANIC SILICON COMPOUND CONTAINING PHOSPHORYL COMPOUND AND METHOD FOR PRODUCING THE SAME[P].JP2022071356,2022-05-16. 显示全部
磷酸二苯酯(Diphenyl phosphate),分子式是C12H11O4P。外观呈白色结晶粉末状,可用于医药及化工生产领域。

图一 磷酸二苯酯
磷酸二苯酯的合成方法有很多种,介绍由苯酚和磷酸为起始原料合成的两种方法,具体如下:
将85%磷酸(461.2毫克,4.0毫摩尔)、苯酚(3.76克,40毫摩尔)、三乙胺(1.21克,12毫摩尔)、1-丁基咪唑(149.0毫克,1.2毫摩尔)和DMF(5毫升)放入由50毫升三颈烧瓶组成的反应装置中,该反应装置具有沸腾溶剂和水蒸汽流过的管子和溶剂通过脱水剂回流的管子。(见图S1)将2.0克作为干燥剂的PAdeCS置于冷凝器下方。将反应在230℃下加热24小时,此后,将所得混合物通过阳离子交换树脂(洗脱剂:甲醇)以除去胺。洗脱液蒸发后,混合物在低压下蒸馏除去苯酚和DMF。通过凝胶渗透色谱GPC(洗脱剂:CHCl3)获得所需的磷酸二苯酯,71%(619.6mg,2.84 mmol)[1]。
在氮气气氛中,加入1毫摩尔植酸(在第二实施例中调节或购自Nacalai Tescu有限公司,50重量%水溶液)、60毫摩尔苯酚(购自Nacalai Tescu有限公司)、18毫摩尔三乙胺(购自Nacalai Tescu有限公司)、3毫摩尔正丁基咪唑(购自Nacalaitescu有限公司)、N,N-二甲基甲酰胺(DMF,购自Nacalaitescu有限公司)并加入搅拌器磁铁。接下来,在将脱水装置连接到上述烧瓶后,将回流管作为冷却器连接到烧瓶的上部。将反应容器浸入油浴中并在230℃下以200 rpm反应24小时。2克2.5-5毫米的PAdeCS(注册商标,由日本混凝土工业有限公司制造)用作脱水材料。反应后,通过1H NMR、13C NMR和31P NMR确认目标磷酸二苯酯的形成。反应后的混合物溶解在甲醇中,并以1毫升/分钟的流速流向阳离子交换树脂(H型)(DOWEX 50 W×2 100-200目(H)阳离子交换树脂)。将所得溶液的溶剂在减压下蒸馏掉,然后在120℃和1.6×102Pa下在kugel辊中减压蒸馏以获得作为目标产物的残余物。将其再次倒入阳离子交换树脂中并纯化。减压除去溶液后,获得白色固体,磷酸二苯酯产率为65%(3.9毫摩尔)[2].

图二 磷酸二苯酯的合成
[1]Chi C T ,Kazuya A ,Takeshi S , et al.Synthesis of diaryl phosphates using orthophosphoric acid as a phosphorus source[J].Tetrahedron Letters,2022,96.
[2]YUKI N ,KAZUHIKO S ,YUMIKO N .ORGANIC SILICON COMPOUND CONTAINING PHOSPHORYL COMPOUND AND METHOD FOR PRODUCING THE SAME[P].JP2022071356,2022-05-16.
 1
1
含氟药物2,3,5,6-四氟吡啶中间体应用十分广泛,主要用于合成农药、医药和染料等,其快速发展促进了下游含氟精细化学品的开发,如目前我国已经能够大量生产的2,3,5,6-四氟吡啶及其类似物,成为世界主要生产国和供应国[1]。

图12,3,5,6-四氟吡啶的合成路线
在装有橡胶隔膜的12x75mm硼硅酸盐试管中加入1.0mLIr(ppy)3在CH3CN中的储备溶液。向混合物中加入五氟吡啶(16.9mg)和N,N-二异丙基乙胺(28.4mg)。在0°C下对反应进行脱气,以避免N,N-二异丙基乙胺和挥发性起始材料通过氩气鼓泡5-10分钟蒸发,然后通过移除出口针在正氩气压力下放置。将试管放入光浴中。将管子的下部浸入保持在45°C(或65°C)的水浴中。通过19FNMR和GC-MS监测反应。用0.3mLCDCl3稀释0.3mL反应混合物。在原料完全消耗后,通过旋转蒸发器去除CH3CN。用去离子水(2mL)处理残留物。用EtOAc(5x1mL)提取残留物。用无水MgSO4干燥合并的有机化合物2,3,5,6-四氟吡啶。合成路线如图1所示[2]。

图22,3,5,6-四氟吡啶的合成路线
将8.85g(10.0mmol)有机锌化合物XXII、1.02g(11.0mmol)丙酰氯(Ic)和0.01g(0.10mmol)CuCl的混合物在55-60°c下在氩气下加热2小时。将混合物冷却至室温,用10ml水处理,并进行蒸汽蒸馏。将有机相分离并用MgSO4干燥。我们分离1.70g含有(GLC)83%的酮XXIV和2,3,5,6-四氟吡啶的混合物。2,3,5,6-四氟吡啶的收益率68%;其红外光谱数据,cm-1:2982、2946、2888、1842、1730、1642、1465、1409、1269、956、859。紫外光谱:λmax275nm(logε3.46)。合成路线如图2所示。
2,3,5,6-四氟吡啶是重要的精细化工中间体,由于其分子结构中活性位点较多,可广泛应用于医药、农药、染料、生物工程、聚酯化合物等的合成。我国从20世纪80年代开始研究开发2,3,5,6-四氟吡啶,除农药领域有所应用外,医药等其他领域均处于起步阶段,且生产规模较小,产能低。随着精细化工产业的日益发展,2,3,5,6-四氟吡啶作为新型产品,应用范围不断扩大,需求量逐年增长[1]。
[1] 马振萍. 四氟吡啶及其类似物的合成研究[D]. 浙江大学, 2007.
[2] Arevalo, Alma; et al. On the Catalytic Hydrodefluorination of Fluoroaromatics Using Nickel Complexes: The True Role of the Phosphine. Journal of the American Chemical Society (2014), 136(12), 4634-4639. 显示全部
含氟药物2,3,5,6-四氟吡啶中间体应用十分广泛,主要用于合成农药、医药和染料等,其快速发展促进了下游含氟精细化学品的开发,如目前我国已经能够大量生产的2,3,5,6-四氟吡啶及其类似物,成为世界主要生产国和供应国[1]。

图12,3,5,6-四氟吡啶的合成路线
在装有橡胶隔膜的12x75mm硼硅酸盐试管中加入1.0mLIr(ppy)3在CH3CN中的储备溶液。向混合物中加入五氟吡啶(16.9mg)和N,N-二异丙基乙胺(28.4mg)。在0°C下对反应进行脱气,以避免N,N-二异丙基乙胺和挥发性起始材料通过氩气鼓泡5-10分钟蒸发,然后通过移除出口针在正氩气压力下放置。将试管放入光浴中。将管子的下部浸入保持在45°C(或65°C)的水浴中。通过19FNMR和GC-MS监测反应。用0.3mLCDCl3稀释0.3mL反应混合物。在原料完全消耗后,通过旋转蒸发器去除CH3CN。用去离子水(2mL)处理残留物。用EtOAc(5x1mL)提取残留物。用无水MgSO4干燥合并的有机化合物2,3,5,6-四氟吡啶。合成路线如图1所示[2]。

图22,3,5,6-四氟吡啶的合成路线
将8.85g(10.0mmol)有机锌化合物XXII、1.02g(11.0mmol)丙酰氯(Ic)和0.01g(0.10mmol)CuCl的混合物在55-60°c下在氩气下加热2小时。将混合物冷却至室温,用10ml水处理,并进行蒸汽蒸馏。将有机相分离并用MgSO4干燥。我们分离1.70g含有(GLC)83%的酮XXIV和2,3,5,6-四氟吡啶的混合物。2,3,5,6-四氟吡啶的收益率68%;其红外光谱数据,cm-1:2982、2946、2888、1842、1730、1642、1465、1409、1269、956、859。紫外光谱:λmax275nm(logε3.46)。合成路线如图2所示。
2,3,5,6-四氟吡啶是重要的精细化工中间体,由于其分子结构中活性位点较多,可广泛应用于医药、农药、染料、生物工程、聚酯化合物等的合成。我国从20世纪80年代开始研究开发2,3,5,6-四氟吡啶,除农药领域有所应用外,医药等其他领域均处于起步阶段,且生产规模较小,产能低。随着精细化工产业的日益发展,2,3,5,6-四氟吡啶作为新型产品,应用范围不断扩大,需求量逐年增长[1]。
[1] 马振萍. 四氟吡啶及其类似物的合成研究[D]. 浙江大学, 2007.
[2] Arevalo, Alma; et al. On the Catalytic Hydrodefluorination of Fluoroaromatics Using Nickel Complexes: The True Role of the Phosphine. Journal of the American Chemical Society (2014), 136(12), 4634-4639.
 1
1
L-盐酸组氨酸是一种白色结晶状物质,易溶于水,呈酸性。作为食品添加剂,它是人体必需的氨基酸之一,也被称为“第一必需氨基酸”。除了用于消化溃疡的辅助治疗外,它还可以用于治疗贫血、心脏疾病等。L-盐酸组氨酸一水物是一种无色结晶固体,常用作营养补充剂,有助于提高免疫功能和抵抗力,同时也可用于治疗疲劳、肝炎等疾病。

L-盐酸组氨酸一水物
L-盐酸组氨酸一水物可以通过多种方法合成,其中最常见的是微生物发酵法。除了发酵法外,还可以使用化学合成法和酶法。化学合成法成本较高且环境污染大,而酶法具有较高的选择性,但受到酶来源和稳定性的限制。
目前L-盐酸组氨酸的生产方法较为复杂,多数需要经过离子交换柱除杂等步骤。新的生产方法提供了一种简单、低成本的生产方式,通过发酵后处理得到产品,避免了大量废水排放。
朱文佳等人提出了一种操作简单、成本低的L-盐酸组氨酸一水物的生产方法,通过发酵、浓缩结晶等步骤得到高收率的产品。
[1]朱文佳,李嫦,黎燕媚等.一种L-盐酸组氨酸的生产方法[P].广东省:CN115851844A,2023-03-28. 显示全部
L-盐酸组氨酸是一种白色结晶状物质,易溶于水,呈酸性。作为食品添加剂,它是人体必需的氨基酸之一,也被称为“第一必需氨基酸”。除了用于消化溃疡的辅助治疗外,它还可以用于治疗贫血、心脏疾病等。L-盐酸组氨酸一水物是一种无色结晶固体,常用作营养补充剂,有助于提高免疫功能和抵抗力,同时也可用于治疗疲劳、肝炎等疾病。

L-盐酸组氨酸一水物
L-盐酸组氨酸一水物可以通过多种方法合成,其中最常见的是微生物发酵法。除了发酵法外,还可以使用化学合成法和酶法。化学合成法成本较高且环境污染大,而酶法具有较高的选择性,但受到酶来源和稳定性的限制。
目前L-盐酸组氨酸的生产方法较为复杂,多数需要经过离子交换柱除杂等步骤。新的生产方法提供了一种简单、低成本的生产方式,通过发酵后处理得到产品,避免了大量废水排放。
朱文佳等人提出了一种操作简单、成本低的L-盐酸组氨酸一水物的生产方法,通过发酵、浓缩结晶等步骤得到高收率的产品。
[1]朱文佳,李嫦,黎燕媚等.一种L-盐酸组氨酸的生产方法[P].广东省:CN115851844A,2023-03-28.
 1
1
3,5-双三氟甲基苯甲醛,化学式为C8H5F6O,是一种无色至浅黄色的固体,具有强烈的刺激性气味。它在常温下不溶于水,但能溶于许多有机溶剂如乙醇和乙醚。在有机合成中常用作试剂和中间体。它可用于合成许多其他有机化合物,如三氟甲基取代的苯甲醚类化合物、具有生物活性的分子和配体。

3,5-双三氟甲基苯甲醛
向1升高压釜中加入100克(0.36摩尔)用与实施例3相同的方法制备的3,5-双(三氟甲基)苯甲酰氯、350克无水甲苯、90克(1.08摩尔)无水乙酸钠和10.9克10%钯-碳。加入21.7克(0.17摩尔)喹啉和3.6克(0.11摩尔)硫后,将内容物加热回流5小时。然后加入用干二甲苯稀释至250毫升的喹啉-S。抽空高压釜后,通过引入氢气将内压调节至1 MPa。在连续供应氢气以将内压保持在1 MPa的同时,在室温下搅拌内容物1小时。将温度升至50℃并继续搅拌2小时。然后,将温度恢复至室温并继续搅拌24小时以完成反应。将内压恢复至大气压后,过滤反应产物溶液,然后用甲苯洗涤。滤液依次用5%碳酸钠水溶液和水洗涤,然后用无水硫酸钠干燥。通过过滤除去无水硫酸钠并通过蒸馏除去甲苯后,通过气相色谱分析所得产物。证实产生了65.4克(0.27摩尔)目标物3,5-双三氟甲基苯甲醛(产率:76%)。通过真空蒸馏,分离出63.0克(0.27摩尔)3,5-双三氟甲基苯甲醛[1]。
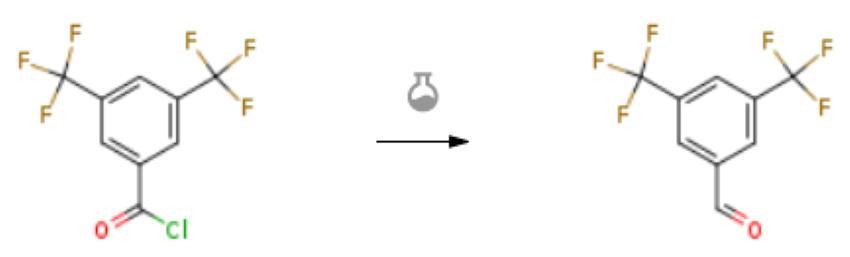
图二 3,5-双三氟甲基苯甲醛的合成
在装有搅拌叶片和温度计的反应釜中,加入4400克四氢呋喃和96克镁粉。在搅拌下加入590克3,5-双三氟甲基溴苯,并将温度控制在35-45℃反应8小时。反应结束后,将温度保持在25-35°C,并继续滴加221g N,N-二甲基甲酰胺。反应结束后,向釜中加入5000克水和400克浓盐酸,酸化后分离液体。水相用8500克乙酸乙酯萃取两次。合并有机相,加入750克5%碳酸钠溶液,搅拌20分钟,分离液体。对有机相进行常压蒸馏以除去大部分溶剂,并在减压下蒸馏以获得GC纯度为99.1%且产率为83%的3,5-双三氟甲基苯甲醛[2]。
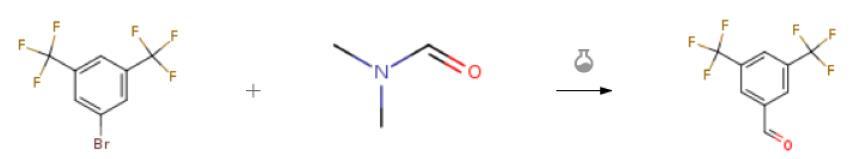
图三 3,5-双三氟甲基苯甲醛的合成2
[1]HIDAKA ,T.,FUSHIMI , et al.HOCHREINE (FLUORALKYL)BENZOLDERIVATE UND VERFAHREN ZU DEREN HERSTELLUNG[P].EP1500641,2006-05-31.
[2]张同斌,王涛,姜殿平等.一种高纯度3,5-双三氟甲基苄醇的制备工艺[P].宁夏回族自治区:CN113214045A,2021-08-06.
显示全部3,5-双三氟甲基苯甲醛,化学式为C8H5F6O,是一种无色至浅黄色的固体,具有强烈的刺激性气味。它在常温下不溶于水,但能溶于许多有机溶剂如乙醇和乙醚。在有机合成中常用作试剂和中间体。它可用于合成许多其他有机化合物,如三氟甲基取代的苯甲醚类化合物、具有生物活性的分子和配体。

3,5-双三氟甲基苯甲醛
向1升高压釜中加入100克(0.36摩尔)用与实施例3相同的方法制备的3,5-双(三氟甲基)苯甲酰氯、350克无水甲苯、90克(1.08摩尔)无水乙酸钠和10.9克10%钯-碳。加入21.7克(0.17摩尔)喹啉和3.6克(0.11摩尔)硫后,将内容物加热回流5小时。然后加入用干二甲苯稀释至250毫升的喹啉-S。抽空高压釜后,通过引入氢气将内压调节至1 MPa。在连续供应氢气以将内压保持在1 MPa的同时,在室温下搅拌内容物1小时。将温度升至50℃并继续搅拌2小时。然后,将温度恢复至室温并继续搅拌24小时以完成反应。将内压恢复至大气压后,过滤反应产物溶液,然后用甲苯洗涤。滤液依次用5%碳酸钠水溶液和水洗涤,然后用无水硫酸钠干燥。通过过滤除去无水硫酸钠并通过蒸馏除去甲苯后,通过气相色谱分析所得产物。证实产生了65.4克(0.27摩尔)目标物3,5-双三氟甲基苯甲醛(产率:76%)。通过真空蒸馏,分离出63.0克(0.27摩尔)3,5-双三氟甲基苯甲醛[1]。

图二 3,5-双三氟甲基苯甲醛的合成
在装有搅拌叶片和温度计的反应釜中,加入4400克四氢呋喃和96克镁粉。在搅拌下加入590克3,5-双三氟甲基溴苯,并将温度控制在35-45℃反应8小时。反应结束后,将温度保持在25-35°C,并继续滴加221g N,N-二甲基甲酰胺。反应结束后,向釜中加入5000克水和400克浓盐酸,酸化后分离液体。水相用8500克乙酸乙酯萃取两次。合并有机相,加入750克5%碳酸钠溶液,搅拌20分钟,分离液体。对有机相进行常压蒸馏以除去大部分溶剂,并在减压下蒸馏以获得GC纯度为99.1%且产率为83%的3,5-双三氟甲基苯甲醛[2]。

图三 3,5-双三氟甲基苯甲醛的合成2
[1]HIDAKA ,T.,FUSHIMI , et al.HOCHREINE (FLUORALKYL)BENZOLDERIVATE UND VERFAHREN ZU DEREN HERSTELLUNG[P].EP1500641,2006-05-31.
[2]张同斌,王涛,姜殿平等.一种高纯度3,5-双三氟甲基苄醇的制备工艺[P].宁夏回族自治区:CN113214045A,2021-08-06.
 1
1
心脏停搏与复灌广泛应用于心脏移植及其他需要心肺旁路循环的手术,但常常造成心肌收缩力下降,心脏机械功能受损。保存复灌心脏的功能,是众多研究的焦点,已有的方法包括:改良停搏液配方、改善底物代谢的药物、清除氧自由基、抑制白细胞对内皮细胞的黏附。近年来,一种通过使心肌细胞肌球蛋白与肌动蛋白失耦联,从而产生负性肌力作用的药物2,3-丁烷二酮一肟(butanedione monoxime,BDM)在保存停搏心肌活性方面的作用越来越受到重视。2,3-丁烷二酮一肟作为停搏液的添加成分,可减少心肌能耗,提高心脏对缺血与停搏的耐受性,改善心肌氧供需平衡;含BDM的复灌液也能发挥相似的作用。本文旨在探讨停搏后以不同浓度的2,3-丁烷二酮一肟进行初始复灌,对后继正常灌流心脏左室机械功能和氧代谢的影响,探寻保护作用最强的浓度并研究其机制。

豚鼠48只,性别不拘,体重250~350g。腹腔注射20mg氯胺酮和1000U肝素,去头处死。开胸后迅速行主动脉插管,以改良Krebs-Ringer液逆行灌流,剪开腔静脉与肺动脉,摘取心脏,旋即将心脏挂于Langendorff灌流装置上,灌流液体同上,压力为55mmHg(1mmHg=0.133kPa),温度37℃。稳定灌流30min后测量基础指标。以20ml St.Thomas Hospital 液灌流,诱导心脏停搏,随后停止灌流,将心脏浸入4℃停搏液中维持12h。复灌前,随机将心脏分为4组。对照组(CON组,12例)直接以改良Krebs-Ringer液复灌:研究组首先分别以含20mmol/L(2,3-丁烷二酮一肟20组,12例)、30mmol/L(2,3-丁烷二酮一肟30组,12例)、40mmol/L(2,3-丁烷二酮一肟40组,12例)的Krebs液进行初始复灌20min,随后均以改良Krebs-Ringer液进行复灌。所有心脏在恢复改良Krebs-Ringer液灌流前均注射利多卡因0.5mg,以恢复窦性心律。分别在改良Krebs-Ringer液灌流5、15、30、60 min后测量各项指标。灌流结束后,剪取左室游离壁组织块,戊二醛固定后行透射电镜检查。
[1]周忠泉,杨沙宁,杨学新,等. 不同浓度2,3-丁二酮单肟初始复灌对停搏心脏的保护作用[J]. 中国心血管病研究杂志,2007,5(4):299-302. DOI:10.3969/j.issn.1672-5301.2007.04.022.
显示全部心脏停搏与复灌广泛应用于心脏移植及其他需要心肺旁路循环的手术,但常常造成心肌收缩力下降,心脏机械功能受损。保存复灌心脏的功能,是众多研究的焦点,已有的方法包括:改良停搏液配方、改善底物代谢的药物、清除氧自由基、抑制白细胞对内皮细胞的黏附。近年来,一种通过使心肌细胞肌球蛋白与肌动蛋白失耦联,从而产生负性肌力作用的药物2,3-丁烷二酮一肟(butanedione monoxime,BDM)在保存停搏心肌活性方面的作用越来越受到重视。2,3-丁烷二酮一肟作为停搏液的添加成分,可减少心肌能耗,提高心脏对缺血与停搏的耐受性,改善心肌氧供需平衡;含BDM的复灌液也能发挥相似的作用。本文旨在探讨停搏后以不同浓度的2,3-丁烷二酮一肟进行初始复灌,对后继正常灌流心脏左室机械功能和氧代谢的影响,探寻保护作用最强的浓度并研究其机制。

豚鼠48只,性别不拘,体重250~350g。腹腔注射20mg氯胺酮和1000U肝素,去头处死。开胸后迅速行主动脉插管,以改良Krebs-Ringer液逆行灌流,剪开腔静脉与肺动脉,摘取心脏,旋即将心脏挂于Langendorff灌流装置上,灌流液体同上,压力为55mmHg(1mmHg=0.133kPa),温度37℃。稳定灌流30min后测量基础指标。以20ml St.Thomas Hospital 液灌流,诱导心脏停搏,随后停止灌流,将心脏浸入4℃停搏液中维持12h。复灌前,随机将心脏分为4组。对照组(CON组,12例)直接以改良Krebs-Ringer液复灌:研究组首先分别以含20mmol/L(2,3-丁烷二酮一肟20组,12例)、30mmol/L(2,3-丁烷二酮一肟30组,12例)、40mmol/L(2,3-丁烷二酮一肟40组,12例)的Krebs液进行初始复灌20min,随后均以改良Krebs-Ringer液进行复灌。所有心脏在恢复改良Krebs-Ringer液灌流前均注射利多卡因0.5mg,以恢复窦性心律。分别在改良Krebs-Ringer液灌流5、15、30、60 min后测量各项指标。灌流结束后,剪取左室游离壁组织块,戊二醛固定后行透射电镜检查。
[1]周忠泉,杨沙宁,杨学新,等. 不同浓度2,3-丁二酮单肟初始复灌对停搏心脏的保护作用[J]. 中国心血管病研究杂志,2007,5(4):299-302. DOI:10.3969/j.issn.1672-5301.2007.04.022.
 1
1
4-氨基苯乙酮是一种重要的医药中间体和原料,可用于合成克喘素和氟比布洛芬等药物。克喘素用于治疗支气管哮喘等疾病,而氟比布洛芬是一种非甾体抗炎药。目前,制备4-氨基苯乙酮的方法存在一些缺陷,如反应条件苛刻、试剂腐蚀性强等。

为了解决这些问题,可以通过Williamson醚合成法制备4-氨基苯乙酮。具体步骤包括制备2-(4-乙酰苯氧基)-2-甲基丙酰胺和N-(4-乙酰苯基)-2-羟基-2-甲基丙酰胺,最终生成4-氨基苯乙酮。
第一步是制备2-(4-乙酰苯氧基)-2-甲基丙酰胺,需要在极性非质子溶剂中进行反应。第二步是制备N-(4-乙酰苯基)-2-羟基-2-甲基丙酰胺,也需要在适当的温度下进行反应。最后一步是将前一步得到的产物进行水解反应,生成4-氨基苯乙酮。
通过这种方法,可以避免反应条件苛刻、减少副产物生成,提高产物纯度和收率,从而更有效地制备4-氨基苯乙酮。
显示全部4-氨基苯乙酮是一种重要的医药中间体和原料,可用于合成克喘素和氟比布洛芬等药物。克喘素用于治疗支气管哮喘等疾病,而氟比布洛芬是一种非甾体抗炎药。目前,制备4-氨基苯乙酮的方法存在一些缺陷,如反应条件苛刻、试剂腐蚀性强等。

为了解决这些问题,可以通过Williamson醚合成法制备4-氨基苯乙酮。具体步骤包括制备2-(4-乙酰苯氧基)-2-甲基丙酰胺和N-(4-乙酰苯基)-2-羟基-2-甲基丙酰胺,最终生成4-氨基苯乙酮。
第一步是制备2-(4-乙酰苯氧基)-2-甲基丙酰胺,需要在极性非质子溶剂中进行反应。第二步是制备N-(4-乙酰苯基)-2-羟基-2-甲基丙酰胺,也需要在适当的温度下进行反应。最后一步是将前一步得到的产物进行水解反应,生成4-氨基苯乙酮。
通过这种方法,可以避免反应条件苛刻、减少副产物生成,提高产物纯度和收率,从而更有效地制备4-氨基苯乙酮。
 1
1
香料是由人工模仿水果和天然香料气味而合成的浓缩芳香油,多用于制造食品、饮料、化妆品和卷烟等。食用香精是参照天然食品的香味,采用天然和天然等同香料、合成香料经精心调配而成具有天然风味的各种香型的香精。包括水果类水质和油质、奶类、家禽类、肉类、蔬菜类、坚果类、蜜饯类、乳化类以及酒类等各种香精,适用于饮料、饼干、糕点、冷冻食品、糖果、调味料、乳制品、罐头、酒等食品中。

丁位十一内酯
向2000mL四口烧瓶中加入6.1g氢氧化钠固体和393.9g水,机械搅拌下加热至80℃,用恒压滴液漏斗滴加342.6g(3.0mol)庚醛与277.2g环戊酮混合液,滴加两小时,保温反应一小时,取样GC检测原料残留和产物含量,待反应完毕则降温,静置分层取上层有机相即反应生成2?亚庚基环戊酮559.8g。GC检测纯度81.9%,内标法计算该步收率约80.8%。所得2?亚庚基环戊酮粗品经5%硫酸钠溶涤后,用钯炭在40?80℃下进行加氢,加氢完成后得到2?庚基环戊酮粗品,再用填料塔进行精馏,收集1mmHg取98℃?105℃馏分451.2g,GC含量98.8%。向干燥洁净的1000ml三口烧瓶加入上述精馏所得庚基环戊酮190g(1mol),加入乙酸260g,浓硫酸5.0g,缓慢加热至温度35℃,滴加现配浓度为27.5%的双氧水240g,滴加时长3小时,保温反应5小时,取样GC检测结果:庚基环戊酮残留4.2%,产物含量88.1%;整个反应过程未发现放热现象。反应结束后降温,静置分层,分出上层有机相丁位十一内酯210.8g[1]。
该方法规避了丁位内酯香料生产过程中所产生的过氧化物的危险工艺,且同时废酸水可套用,提高资源综合利用率,一锅法合成丁位十一内酯合理高效、操作简便。
[1]张政,梁立冬,王毅.一种安全、高效生产天然丁位十一内酯的方法[P].安徽省:CN116874459A,2023-10-13.
显示全部香料是由人工模仿水果和天然香料气味而合成的浓缩芳香油,多用于制造食品、饮料、化妆品和卷烟等。食用香精是参照天然食品的香味,采用天然和天然等同香料、合成香料经精心调配而成具有天然风味的各种香型的香精。包括水果类水质和油质、奶类、家禽类、肉类、蔬菜类、坚果类、蜜饯类、乳化类以及酒类等各种香精,适用于饮料、饼干、糕点、冷冻食品、糖果、调味料、乳制品、罐头、酒等食品中。

丁位十一内酯
向2000mL四口烧瓶中加入6.1g氢氧化钠固体和393.9g水,机械搅拌下加热至80℃,用恒压滴液漏斗滴加342.6g(3.0mol)庚醛与277.2g环戊酮混合液,滴加两小时,保温反应一小时,取样GC检测原料残留和产物含量,待反应完毕则降温,静置分层取上层有机相即反应生成2?亚庚基环戊酮559.8g。GC检测纯度81.9%,内标法计算该步收率约80.8%。所得2?亚庚基环戊酮粗品经5%硫酸钠溶涤后,用钯炭在40?80℃下进行加氢,加氢完成后得到2?庚基环戊酮粗品,再用填料塔进行精馏,收集1mmHg取98℃?105℃馏分451.2g,GC含量98.8%。向干燥洁净的1000ml三口烧瓶加入上述精馏所得庚基环戊酮190g(1mol),加入乙酸260g,浓硫酸5.0g,缓慢加热至温度35℃,滴加现配浓度为27.5%的双氧水240g,滴加时长3小时,保温反应5小时,取样GC检测结果:庚基环戊酮残留4.2%,产物含量88.1%;整个反应过程未发现放热现象。反应结束后降温,静置分层,分出上层有机相丁位十一内酯210.8g[1]。
该方法规避了丁位内酯香料生产过程中所产生的过氧化物的危险工艺,且同时废酸水可套用,提高资源综合利用率,一锅法合成丁位十一内酯合理高效、操作简便。
[1]张政,梁立冬,王毅.一种安全、高效生产天然丁位十一内酯的方法[P].安徽省:CN116874459A,2023-10-13.
 1
1
N-叔丁基-2-苯并噻唑次磺酰胺,英文简称为TBBS,常温常压下为浅黄色固体粉末,不溶于水但是可溶于二氯甲烷、四氯化碳和乙酸乙酯。N-叔丁基-2-苯并噻唑次磺酰胺是一种工业常用的次磺酰胺类硫化促进剂,它可用于天然橡胶、顺丁橡胶、丁苯橡胶的工业生产过程。

图1 N-叔丁基-2-苯并噻唑次磺酰胺的性状图
橡胶硫化促进剂产品种类多样,按照化学结构来划分,主要可以分为次磺酰胺类、噻唑类、秋兰姆类、胍类、二硫代甲酸盐类、硫脲类等,磺酰胺类是其中应用范围最广、需求量最大的品类,而促进剂N-叔丁基-2-苯并噻唑次磺酰胺则是磺酰胺类促进剂的主流产品类型。促进剂是橡胶生产所不可或缺的重要助剂,在全球范围内,中国是主要的促进剂生产国,全球70%左右的促进剂由中国供应,全球促进剂NS产能主要集中在中国。
N-叔丁基-2-苯并噻唑次磺酰胺属于次磺酰胺类硫化促进剂,是常见的后效性橡胶促进剂,它具有特殊气味,并且其结构中含有一个高度活泼的硫氮键,它受高热或者强光照射容易发生硫氮键的断裂,并且它对氧化剂也较为敏感。N-叔丁基-2-苯并噻唑次磺酰胺拥有一般磺酰胺类促进剂的优点,具有优良的抗焦烧性能与硫化速度,且安全性好。与促进剂NOBS相比,N-叔丁基-2-苯并噻唑次磺酰胺性能接近且无致癌性,可替代促进剂NOBS使用。N-叔丁基-2-苯并噻唑次磺酰胺性能也与促进剂CBS(促进剂CZ)接近,用途与后者相似,相较来说,其后效性更大。促进剂NS可作为多种橡胶的添加剂使用,可以广泛应用在轮胎、制鞋、胶带、胶管、电缆等制造中。
N-叔丁基-2-苯并噻唑次磺酰胺制备是以促进剂M(2-巯基苯并噻唑)为原料,与氢氧化钠水溶液在反应釜进行反应,再依次加入叔丁胺、硫酸、次氯酸钠,在一定温度条件下进行反应,再经冷却、过滤、洗涤、干燥等工艺制得。[1]
[1] 赵敏. 橡胶硫化促进剂N-叔丁基-2-苯并噻唑次磺酰胺(NS)制备方法[J].橡胶工业, 2014, 61(9): 575-575. 显示全部
N-叔丁基-2-苯并噻唑次磺酰胺,英文简称为TBBS,常温常压下为浅黄色固体粉末,不溶于水但是可溶于二氯甲烷、四氯化碳和乙酸乙酯。N-叔丁基-2-苯并噻唑次磺酰胺是一种工业常用的次磺酰胺类硫化促进剂,它可用于天然橡胶、顺丁橡胶、丁苯橡胶的工业生产过程。

图1 N-叔丁基-2-苯并噻唑次磺酰胺的性状图
橡胶硫化促进剂产品种类多样,按照化学结构来划分,主要可以分为次磺酰胺类、噻唑类、秋兰姆类、胍类、二硫代甲酸盐类、硫脲类等,磺酰胺类是其中应用范围最广、需求量最大的品类,而促进剂N-叔丁基-2-苯并噻唑次磺酰胺则是磺酰胺类促进剂的主流产品类型。促进剂是橡胶生产所不可或缺的重要助剂,在全球范围内,中国是主要的促进剂生产国,全球70%左右的促进剂由中国供应,全球促进剂NS产能主要集中在中国。
N-叔丁基-2-苯并噻唑次磺酰胺属于次磺酰胺类硫化促进剂,是常见的后效性橡胶促进剂,它具有特殊气味,并且其结构中含有一个高度活泼的硫氮键,它受高热或者强光照射容易发生硫氮键的断裂,并且它对氧化剂也较为敏感。N-叔丁基-2-苯并噻唑次磺酰胺拥有一般磺酰胺类促进剂的优点,具有优良的抗焦烧性能与硫化速度,且安全性好。与促进剂NOBS相比,N-叔丁基-2-苯并噻唑次磺酰胺性能接近且无致癌性,可替代促进剂NOBS使用。N-叔丁基-2-苯并噻唑次磺酰胺性能也与促进剂CBS(促进剂CZ)接近,用途与后者相似,相较来说,其后效性更大。促进剂NS可作为多种橡胶的添加剂使用,可以广泛应用在轮胎、制鞋、胶带、胶管、电缆等制造中。
N-叔丁基-2-苯并噻唑次磺酰胺制备是以促进剂M(2-巯基苯并噻唑)为原料,与氢氧化钠水溶液在反应釜进行反应,再依次加入叔丁胺、硫酸、次氯酸钠,在一定温度条件下进行反应,再经冷却、过滤、洗涤、干燥等工艺制得。[1]
[1] 赵敏. 橡胶硫化促进剂N-叔丁基-2-苯并噻唑次磺酰胺(NS)制备方法[J].橡胶工业, 2014, 61(9): 575-575.
 1
1
2-磺基苯甲酸酐,英文名:2-Sulfobenzoic anhydride,CAS号:81-08-3,分子量:184.169,密度:1.6±0.1 g/cm3,沸点:314.7±0.0°C at 760 mmHg,分子式:C7H4O4S,熔点:116-124°C,闪点:140.6±19.3°C,蒸汽压:0.0±0.6 mmHg at 25°C,灰白色粉末,可溶于甲苯,存放于惰性气体之中.

目前, 酰基磺酸酯类化合物的合成方法有限,主要方法是羧酸酐与磺酸进行反应或磺酸/磺酸酐与羧基酰氯/羧酸进行反应的方法,该方法中存在一定的风险弊端,例如利用甲基磺酸与甲基羧酸酐进行的反应,这种酯交换反应活性低,反应速率和转化率均较低,后续提纯过程繁琐;而利用磺酸酐与酰氯进行反应的方法只对于制备一些链状酰基磺酸酯比较适用,限制了这种方法的应用。本文为了克服上述方法的不足,以制备2-磺基苯甲酸酐为例提供一种酰基磺酸酯类化合物的新型的合成方法.
方法一:量取200ml乙腈溶剂,加入到三口烧瓶中,然后加入0.5mol的2-巯基苯甲酸;向溶液中逐渐加入0.45mol的磺酰氯,滴加时间为30min,温度控制在20℃以下。滴加完毕后,继续反应1h,然后向溶液中逐渐加入二氯甲烷洗涤剂500ml。过滤溶液,收集固体滤饼,并加入200ml二氯甲烷洗涤、过滤,如此洗涤4次,得到白色固体。将得到的固体在50℃进行真空干燥,得到的2-磺基苯甲酸酐,产率87.4%,纯度99.1%.
方法二:量取200ml乙腈溶剂,加入到三口烧瓶中,然后加入0.5mol的2-巯基苯甲酸;向溶液中逐渐加入0.45mol的氯磺酸,滴加时间为30min,温度控制在20℃以下。滴加完毕后,继续反应1h,然后向溶液中逐渐加入二氯甲烷洗涤剂500m1。过滤溶液,收集固体滤饼,并加入200ml二氯甲烷洗涤、过滤,如此洗涤4次,得到白色固体。将得到的固体在50℃进行真空干燥,得到的2-磺基苯甲酸酐,产率53.7%,纯度98.6%.
方法三:量取200ml乙睛溶剂,加入到三口烧瓶中,然后加入0.5mol的2-巯基苯甲酸;向溶液中逐渐加入0.45mol的氯磺酸和0.5mol的DCC,滴加时间为1h,温度控制在20℃以下。滴加完毕后,继续反应1h,然后向溶液中逐渐加入二氯甲烷洗涤剂500ml。过滤溶液,收集固体滤饼,利用200ml二氯甲烷和200ml超纯水反复洗涤、过滤,如此洗涤4次,得到白色固体。将得到的固体在50℃进行真空干燥,得到的2-磺基苯甲酸酐,产率78.5%,纯度98.0%.
[1]杉杉新材料(衢州)有限公司. 一种酰基磺酸酯类化合物的制备方法:CN201910641518.6[P]. 2021-01-19.
显示全部2-磺基苯甲酸酐,英文名:2-Sulfobenzoic anhydride,CAS号:81-08-3,分子量:184.169,密度:1.6±0.1 g/cm3,沸点:314.7±0.0°C at 760 mmHg,分子式:C7H4O4S,熔点:116-124°C,闪点:140.6±19.3°C,蒸汽压:0.0±0.6 mmHg at 25°C,灰白色粉末,可溶于甲苯,存放于惰性气体之中.

目前, 酰基磺酸酯类化合物的合成方法有限,主要方法是羧酸酐与磺酸进行反应或磺酸/磺酸酐与羧基酰氯/羧酸进行反应的方法,该方法中存在一定的风险弊端,例如利用甲基磺酸与甲基羧酸酐进行的反应,这种酯交换反应活性低,反应速率和转化率均较低,后续提纯过程繁琐;而利用磺酸酐与酰氯进行反应的方法只对于制备一些链状酰基磺酸酯比较适用,限制了这种方法的应用。本文为了克服上述方法的不足,以制备2-磺基苯甲酸酐为例提供一种酰基磺酸酯类化合物的新型的合成方法.
方法一:量取200ml乙腈溶剂,加入到三口烧瓶中,然后加入0.5mol的2-巯基苯甲酸;向溶液中逐渐加入0.45mol的磺酰氯,滴加时间为30min,温度控制在20℃以下。滴加完毕后,继续反应1h,然后向溶液中逐渐加入二氯甲烷洗涤剂500ml。过滤溶液,收集固体滤饼,并加入200ml二氯甲烷洗涤、过滤,如此洗涤4次,得到白色固体。将得到的固体在50℃进行真空干燥,得到的2-磺基苯甲酸酐,产率87.4%,纯度99.1%.
方法二:量取200ml乙腈溶剂,加入到三口烧瓶中,然后加入0.5mol的2-巯基苯甲酸;向溶液中逐渐加入0.45mol的氯磺酸,滴加时间为30min,温度控制在20℃以下。滴加完毕后,继续反应1h,然后向溶液中逐渐加入二氯甲烷洗涤剂500m1。过滤溶液,收集固体滤饼,并加入200ml二氯甲烷洗涤、过滤,如此洗涤4次,得到白色固体。将得到的固体在50℃进行真空干燥,得到的2-磺基苯甲酸酐,产率53.7%,纯度98.6%.
方法三:量取200ml乙睛溶剂,加入到三口烧瓶中,然后加入0.5mol的2-巯基苯甲酸;向溶液中逐渐加入0.45mol的氯磺酸和0.5mol的DCC,滴加时间为1h,温度控制在20℃以下。滴加完毕后,继续反应1h,然后向溶液中逐渐加入二氯甲烷洗涤剂500ml。过滤溶液,收集固体滤饼,利用200ml二氯甲烷和200ml超纯水反复洗涤、过滤,如此洗涤4次,得到白色固体。将得到的固体在50℃进行真空干燥,得到的2-磺基苯甲酸酐,产率78.5%,纯度98.0%.
[1]杉杉新材料(衢州)有限公司. 一种酰基磺酸酯类化合物的制备方法:CN201910641518.6[P]. 2021-01-19.
 1
1
1-(4-methylphenyl)-1-propanon,简称4-MPP,可用作化学试剂和医药中间体。

性状:浅黄色至无色透明液体
熔点为7.2℃
沸点238-239℃,78-82℃/533Pa(4mmHg)
相对密度0.993
折光率1.5280
闪点96℃
折射率:n20/D 1.528(lit.)
对甲基苯丙酮可用作生产药物脑脉宁的重要中间体;也用于电羧化反应的化学试剂。
远离明火。储存在阴凉干燥的密闭容器内。
显示全部1-(4-methylphenyl)-1-propanon,简称4-MPP,可用作化学试剂和医药中间体。

性状:浅黄色至无色透明液体
熔点为7.2℃
沸点238-239℃,78-82℃/533Pa(4mmHg)
相对密度0.993
折光率1.5280
闪点96℃
折射率:n20/D 1.528(lit.)
对甲基苯丙酮可用作生产药物脑脉宁的重要中间体;也用于电羧化反应的化学试剂。
远离明火。储存在阴凉干燥的密闭容器内。
 1
1
安息香乙醚是一种在药物合成中十分重要的中间体,其化学结构为1,2-二苯基-2-烷氧基乙酮。除了在药物领域,它还因为能吸收近紫外光的特性,在印刷、涂料等工业中被广泛应用作光敏剂。
传统方法合成安息香乙醚通常采用均相催化反应,分为两步:首先,苯甲醛在催化剂的作用下与自身进行缩合,形成安息香;其次,安息香与低碳醇在酸性催化剂的作用下反应,生成安息香乙醚。然而,传统的催化剂,如氰化物或亲核性强的有机物(如噻唑盐、硫胺素等),存在诸多问题,包括毒性高、转化率低、副产物多等,同时也难以满足催化剂再利用和产品纯化等需求。
近年来,为了克服传统方法的不足,研究人员提出了利用多相催化剂一步合成安息香乙醚的方法。然而,目前报道的多相催化剂对苯甲醛的转化率最高仅为75.6%,依然不尽人意。因此,开发高转化率、高选择性的多相催化剂,以实现安息香乙醚的绿色一步法合成,仍然是一个具有挑战性的重要课题。
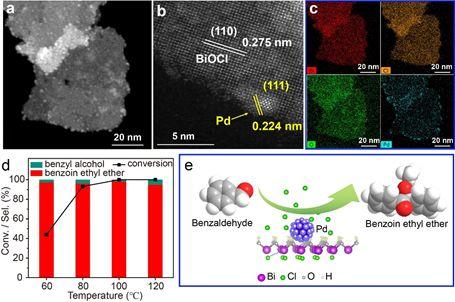
研究人员选择了BiOCl作为贵金属催化剂的载体,构建了一种新型多相催化剂,用于高效合成安息香乙醚。他们利用液相激光辐照技术制备了超薄BiOCl纳米片作为载体,并在其表面原位负载超精细Pd纳米颗粒,合成了Pd/BiOCl催化剂。
在100 ℃和1Mpa H2的反应条件下,Pd/BiOCl催化剂成功实现了对原料苯甲醛的完全转化,同时对安息香乙醚的选择性高达97.9%,并且表现出良好的循环稳定性。
研究者通过选择不含卤素离子的TiO2、C3N4和C作为载体负载Pd催化剂,发现同等条件下其对安息香乙醚的选择性表现为0%。理论计算结果显示,Fe离子在BiOCl晶格中的替代掺杂能够抑制Cl?离子的解离。
为了进一步验证载体对安息香乙醚合成的重要性,研究者构建了Pd负载Fe掺杂BiOCl催化剂,结果显示随着Fe掺杂量的增加,催化剂对安息香乙醚的选择性逐渐降低。
催化机制分析表明,BiOCl载体中易解离的Cl?离子与Pd在反应中形成了亲核试剂,从而促进了安息香乙醚的合成。这项研究提出了基于超薄BiOCl纳米片载体构建多相催化剂的新思路,为安息香乙醚的合成提供了新的途径。
相关结果发表在ChemCatChem, 2019, 11, 2676。 显示全部
安息香乙醚是一种在药物合成中十分重要的中间体,其化学结构为1,2-二苯基-2-烷氧基乙酮。除了在药物领域,它还因为能吸收近紫外光的特性,在印刷、涂料等工业中被广泛应用作光敏剂。
传统方法合成安息香乙醚通常采用均相催化反应,分为两步:首先,苯甲醛在催化剂的作用下与自身进行缩合,形成安息香;其次,安息香与低碳醇在酸性催化剂的作用下反应,生成安息香乙醚。然而,传统的催化剂,如氰化物或亲核性强的有机物(如噻唑盐、硫胺素等),存在诸多问题,包括毒性高、转化率低、副产物多等,同时也难以满足催化剂再利用和产品纯化等需求。
近年来,为了克服传统方法的不足,研究人员提出了利用多相催化剂一步合成安息香乙醚的方法。然而,目前报道的多相催化剂对苯甲醛的转化率最高仅为75.6%,依然不尽人意。因此,开发高转化率、高选择性的多相催化剂,以实现安息香乙醚的绿色一步法合成,仍然是一个具有挑战性的重要课题。

研究人员选择了BiOCl作为贵金属催化剂的载体,构建了一种新型多相催化剂,用于高效合成安息香乙醚。他们利用液相激光辐照技术制备了超薄BiOCl纳米片作为载体,并在其表面原位负载超精细Pd纳米颗粒,合成了Pd/BiOCl催化剂。
在100 ℃和1Mpa H2的反应条件下,Pd/BiOCl催化剂成功实现了对原料苯甲醛的完全转化,同时对安息香乙醚的选择性高达97.9%,并且表现出良好的循环稳定性。
研究者通过选择不含卤素离子的TiO2、C3N4和C作为载体负载Pd催化剂,发现同等条件下其对安息香乙醚的选择性表现为0%。理论计算结果显示,Fe离子在BiOCl晶格中的替代掺杂能够抑制Cl?离子的解离。
为了进一步验证载体对安息香乙醚合成的重要性,研究者构建了Pd负载Fe掺杂BiOCl催化剂,结果显示随着Fe掺杂量的增加,催化剂对安息香乙醚的选择性逐渐降低。
催化机制分析表明,BiOCl载体中易解离的Cl?离子与Pd在反应中形成了亲核试剂,从而促进了安息香乙醚的合成。这项研究提出了基于超薄BiOCl纳米片载体构建多相催化剂的新思路,为安息香乙醚的合成提供了新的途径。
相关结果发表在ChemCatChem, 2019, 11, 2676。
 1
1
核黄素磷酸钠是一种消炎类药物,适用于由核黄素缺乏引起的口角炎、唇炎、舌炎、膜炎及阴囊炎等疾病的治疗。也可用于心血管疾病、缺铁性贫血、食道系统恶性肿瘤的防治,还可大量作为食品营养强化剂.

核黄素磷酸钠为黄色至橙色结晶性粉末。微臭。味苦。有吸湿性。溶于水,在水中的溶解度比核黄素大100倍以上(1g/10ml)。不溶于乙醇、乙醚和氯仿。水溶液为浅黄绿色,发出带浅黄绿色的荧光。1%水溶液的pH值约为2.0,6.8%约为pH5.6,11.2%约为pH6.9。干燥时不受散射光的影响,但在溶液中时,光促使其迅速变质。旋光度 :+38°~+42°.
核黄素磷酸钠为维生素类药。核黄素(维生素B2)是人体重要营养素,在能量代谢中起关键作用。本药为黄素单核苷酸(FMN)和黄素腺嘌呤二核苷酸(FAD)前体药,而FMN和FAD是黄素酶家族的重要辅助因子。黄素酶催化很多生化反应,最典型的为氧化还原反应,它们是细胞呼吸的关键因子。FAD和 FMN在线粒体转动链中递氢,在此过程中产生细胞能量。缺乏时可影响机体的生物氧化,使代谢发生障碍,其病变多表现为口、眼、外生殖器部位的炎症.
CN105399772A公开一种核黄素磷酸钠的合成工艺,其特征是:该合成工艺包括如下步骤:
(1)酯化反应:在乙腈作为溶剂的反应釜中,加入吡啶作为催化剂,核黄素和三氯氧磷可以发生酯化反应生成核黄素磷酸酯以及一些其他杂质,如感光黄素。过滤,除去固体物料,将滤液打到水解釜进行下一步反应.
(2)水解反应:在水解釜中,加入酸酸化,再加入氢氧化钠中和,得核黄素磷酸钠粗品。过滤,收集滤饼,将滤饼加入结晶釜中进行纯化.
(3)结晶反应:在结晶罐中,加入盐酸调节pH在5.5左右,此时进行结晶,得核黄素磷酸钠晶体,过滤.
(4)精制:将滤饼在干燥器中进行干燥,干燥后得核黄素磷酸钠.
1.ADI 0~0.5mg/kg(FAO/WHO,1994)。2. LD50 510mg/kg(小鼠皮下注射)。3. GRAS(FDA,§182,5697,1985).
显示全部核黄素磷酸钠是一种消炎类药物,适用于由核黄素缺乏引起的口角炎、唇炎、舌炎、膜炎及阴囊炎等疾病的治疗。也可用于心血管疾病、缺铁性贫血、食道系统恶性肿瘤的防治,还可大量作为食品营养强化剂.

核黄素磷酸钠为黄色至橙色结晶性粉末。微臭。味苦。有吸湿性。溶于水,在水中的溶解度比核黄素大100倍以上(1g/10ml)。不溶于乙醇、乙醚和氯仿。水溶液为浅黄绿色,发出带浅黄绿色的荧光。1%水溶液的pH值约为2.0,6.8%约为pH5.6,11.2%约为pH6.9。干燥时不受散射光的影响,但在溶液中时,光促使其迅速变质。旋光度 :+38°~+42°.
核黄素磷酸钠为维生素类药。核黄素(维生素B2)是人体重要营养素,在能量代谢中起关键作用。本药为黄素单核苷酸(FMN)和黄素腺嘌呤二核苷酸(FAD)前体药,而FMN和FAD是黄素酶家族的重要辅助因子。黄素酶催化很多生化反应,最典型的为氧化还原反应,它们是细胞呼吸的关键因子。FAD和 FMN在线粒体转动链中递氢,在此过程中产生细胞能量。缺乏时可影响机体的生物氧化,使代谢发生障碍,其病变多表现为口、眼、外生殖器部位的炎症.
CN105399772A公开一种核黄素磷酸钠的合成工艺,其特征是:该合成工艺包括如下步骤:
(1)酯化反应:在乙腈作为溶剂的反应釜中,加入吡啶作为催化剂,核黄素和三氯氧磷可以发生酯化反应生成核黄素磷酸酯以及一些其他杂质,如感光黄素。过滤,除去固体物料,将滤液打到水解釜进行下一步反应.
(2)水解反应:在水解釜中,加入酸酸化,再加入氢氧化钠中和,得核黄素磷酸钠粗品。过滤,收集滤饼,将滤饼加入结晶釜中进行纯化.
(3)结晶反应:在结晶罐中,加入盐酸调节pH在5.5左右,此时进行结晶,得核黄素磷酸钠晶体,过滤.
(4)精制:将滤饼在干燥器中进行干燥,干燥后得核黄素磷酸钠.
1.ADI 0~0.5mg/kg(FAO/WHO,1994)。2. LD50 510mg/kg(小鼠皮下注射)。3. GRAS(FDA,§182,5697,1985).
 1
1
羧甲基纤维素是一种白色或微黄色粉末、粒状或纤维状固体,属大分子化学物质,易溶解在水中,不溶于有机溶剂,且能够吸水膨胀,在水中溶胀时可以形成透明的黏稠胶液,黏性会因为温度的上升而下降。由于其特殊性能,因此在储存运输中有着许多特殊要求。水悬浮液的pH值为6.5-8.5。

分子量:当置换度为0.2,分子量为178.14;当置换度为1.5,分子量为282.18;聚合分子量约17,000(n约100)。
外观:白色或淡黄色,无臭、无味,具吸湿性颗粒,粉粒或细纤维状。
羧甲基纤维素是天然纤维素经化学改性得到的一种具有醚结构的衍生物,由于酸式的水溶性较差,因而产品普遍制成钠盐,简称CMC。羧甲基纤维素钠溶于水,能显著改善溶液粘度,具有增稠、乳化、分散、悬浮、保护胶体等作用,生理无害,因此在食品、医药、日化、造纸、纺织等领域中得到广泛应用。
一种羧甲基纤维素的制备方法,其特征在于,在密封、氮气环境中,所述制备方法包括以下步骤:
(1)纤维素浸润:在60~300转/分的搅拌速度下,将1重量份、60~120目大小的纤维素粉缓慢加入反应釜中,使纤维素粉体处于动态悬浮状态,以液压喷雾的方式往反应釜中加入0.4~1.0重量份体积比为90~98%甲醇或乙醇或异戊醇溶液,维持20~40分钟;
(2)纤维素碱化:维持纤维素粉体处于动态悬浮状态,往反应釜中加入0.2~1.5重量份100~150目的粉末氢氧化钠或氢氧化钾,混匀15~30分钟;随后以液压喷雾的方式加入0.1~0.6重量份水进行碱化反应,控制温度在8~25℃,反应30~240min;
(3)醚化反应:维持反应物料处于动态悬浮状态,加入0.4~2.0重量份固体一氯乙酸,控制温度在46~52℃,反应60~120min;
(4)二次碱化反应:维持反应物料处于动态悬浮状态,加入0.1~1.0重量份100~150目的粉末氢氧化钠或氢氧化钾,控制温度在55~75℃,反应60~120min后,停止搅拌,降温出料,得到羧甲基纤维素钠或羧甲基纤维素钾。
毒性分级: 低毒。一般情况下正常合理的使用对人体危害不大。
CN104844715A
显示全部羧甲基纤维素是一种白色或微黄色粉末、粒状或纤维状固体,属大分子化学物质,易溶解在水中,不溶于有机溶剂,且能够吸水膨胀,在水中溶胀时可以形成透明的黏稠胶液,黏性会因为温度的上升而下降。由于其特殊性能,因此在储存运输中有着许多特殊要求。水悬浮液的pH值为6.5-8.5。

分子量:当置换度为0.2,分子量为178.14;当置换度为1.5,分子量为282.18;聚合分子量约17,000(n约100)。
外观:白色或淡黄色,无臭、无味,具吸湿性颗粒,粉粒或细纤维状。
羧甲基纤维素是天然纤维素经化学改性得到的一种具有醚结构的衍生物,由于酸式的水溶性较差,因而产品普遍制成钠盐,简称CMC。羧甲基纤维素钠溶于水,能显著改善溶液粘度,具有增稠、乳化、分散、悬浮、保护胶体等作用,生理无害,因此在食品、医药、日化、造纸、纺织等领域中得到广泛应用。
一种羧甲基纤维素的制备方法,其特征在于,在密封、氮气环境中,所述制备方法包括以下步骤:
(1)纤维素浸润:在60~300转/分的搅拌速度下,将1重量份、60~120目大小的纤维素粉缓慢加入反应釜中,使纤维素粉体处于动态悬浮状态,以液压喷雾的方式往反应釜中加入0.4~1.0重量份体积比为90~98%甲醇或乙醇或异戊醇溶液,维持20~40分钟;
(2)纤维素碱化:维持纤维素粉体处于动态悬浮状态,往反应釜中加入0.2~1.5重量份100~150目的粉末氢氧化钠或氢氧化钾,混匀15~30分钟;随后以液压喷雾的方式加入0.1~0.6重量份水进行碱化反应,控制温度在8~25℃,反应30~240min;
(3)醚化反应:维持反应物料处于动态悬浮状态,加入0.4~2.0重量份固体一氯乙酸,控制温度在46~52℃,反应60~120min;
(4)二次碱化反应:维持反应物料处于动态悬浮状态,加入0.1~1.0重量份100~150目的粉末氢氧化钠或氢氧化钾,控制温度在55~75℃,反应60~120min后,停止搅拌,降温出料,得到羧甲基纤维素钠或羧甲基纤维素钾。
毒性分级: 低毒。一般情况下正常合理的使用对人体危害不大。
CN104844715A
 1
1
苯丙酸诺龙属于男性生殖系统用药中的雄激素类或蛋白同化激素类药。
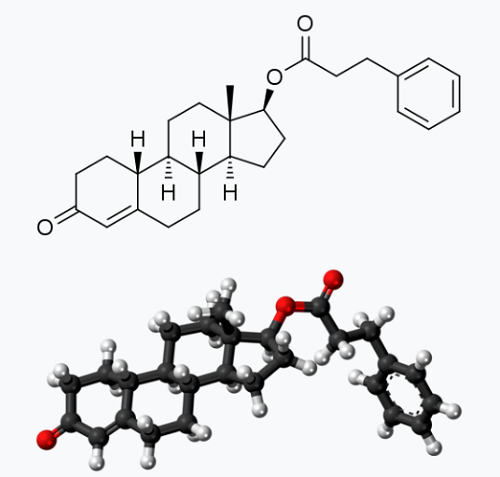
☆ 本药为蛋白同化激素,能促进氨基酸合成蛋白质,抑制氨基酸分解生成尿素,从而纠正负氮平衡;还可使钙、磷、钾、硫和肌酸蓄积,促进肌肉、骨骼生长和发育,增加体重。
☆ 苯丙酸诺龙能促进蛋白质合成,还能促进肌肉、骨胳生长和发育,增加体重。主要用于以下情况:
① 女性晚期乳腺癌的姑息治疗;
② 伴蛋白分解的消耗性疾病,如严重烧伤、慢性腹泻、大手术后。
注:医生可能因其他原因给您处方本药。
☆ 如果您存在以下情况,是不能使用苯丙酸诺龙的,请您将所有已确诊的疾病及正在接受的治疗方案告诉医生:
① 高血压。
② 前列腺癌。
☆ 请不要给儿童使用苯丙酸诺龙。
☆ 孕妇禁用。如果您已经怀孕或者计划怀孕,请告知医生以便做出更好的治疗选择。
☆ 哺乳期妇女如果用药,需停止哺乳。如果您处于哺乳期,请告知医生以便做出更好的治疗选择。
☆ 经深部肌内注射给药。
注:不按照医嘱或说明书用药可能影响疗效且会增加毒副作用。
☆ 用于蛋白大量分解的严重消耗性疾病时,需同时摄入充足的热量和蛋白质。
☆ 用药后可能出现恶心、呕吐、消化不良、腹泻、黄疸、皮疹、脸潮红、女性轻微男性化(如长胡须、粉刺增多、多毛、声音变粗、阴蒂肥大、闭经或月经紊乱)等副作用。如果出现黄疸,可能需立即停药。男性长期用药可能出现座疮、精子减少、精液减少。
注:您可能出现其他的副作用,如果您用药后感觉不适请就诊! 显示全部
苯丙酸诺龙属于男性生殖系统用药中的雄激素类或蛋白同化激素类药。

☆ 本药为蛋白同化激素,能促进氨基酸合成蛋白质,抑制氨基酸分解生成尿素,从而纠正负氮平衡;还可使钙、磷、钾、硫和肌酸蓄积,促进肌肉、骨骼生长和发育,增加体重。
☆ 苯丙酸诺龙能促进蛋白质合成,还能促进肌肉、骨胳生长和发育,增加体重。主要用于以下情况:
① 女性晚期乳腺癌的姑息治疗;
② 伴蛋白分解的消耗性疾病,如严重烧伤、慢性腹泻、大手术后。
注:医生可能因其他原因给您处方本药。
☆ 如果您存在以下情况,是不能使用苯丙酸诺龙的,请您将所有已确诊的疾病及正在接受的治疗方案告诉医生:
① 高血压。
② 前列腺癌。
☆ 请不要给儿童使用苯丙酸诺龙。
☆ 孕妇禁用。如果您已经怀孕或者计划怀孕,请告知医生以便做出更好的治疗选择。
☆ 哺乳期妇女如果用药,需停止哺乳。如果您处于哺乳期,请告知医生以便做出更好的治疗选择。
☆ 经深部肌内注射给药。
注:不按照医嘱或说明书用药可能影响疗效且会增加毒副作用。
☆ 用于蛋白大量分解的严重消耗性疾病时,需同时摄入充足的热量和蛋白质。
☆ 用药后可能出现恶心、呕吐、消化不良、腹泻、黄疸、皮疹、脸潮红、女性轻微男性化(如长胡须、粉刺增多、多毛、声音变粗、阴蒂肥大、闭经或月经紊乱)等副作用。如果出现黄疸,可能需立即停药。男性长期用药可能出现座疮、精子减少、精液减少。
注:您可能出现其他的副作用,如果您用药后感觉不适请就诊!
 1
1
2,3-二甲氧基苯甲醛是一种重要的医药中间体,主要用于黄连素的合成。

目前2,3-二甲氧基苯甲醛的生产工艺主要是由2-甲氧基-3-羟基苯甲醛与硫酸二甲酯反应而得。但是2-甲氧基-3-羟基苯甲醛价格昂贵,硫酸二甲酯毒性大,严重污染环境,制备的2,3-二甲氧基苯甲醛不适合作为医药中间体。文献报道了和碘甲烷反应制备2,3-二甲氧基苯甲醛,但成本较高,原子利用率较低。
考虑到工业生产的可行性,我们提出了以邻溴苯酚为原料经过甲酰化、溴的甲氧基化和酚羟基的醚化集成的两步法合成2,3-二甲氧基苯甲醛。其中邻溴苯酚与多聚甲醛的甲酰化反应形成3-溴-2-羟基苯甲醛已有相关文献报道(Tetrahedron Letters,2005,46:3357–3358)取代溴苯与甲醇钠反应形成取代苯甲醚也有相关报道(Tetrahedron Letters,1993,34(6):3357–3358),酚与碳酸二甲酯反应形成苯甲醚也有文献报道,但转化率较低,主要是因为用碳酸二甲酯为甲基化试剂反应条件苛刻,需要高温高压,还需要使用有毒性的相转移催化剂(Tetrahedron Letters,2002,43:2661–2663)但此方法从未用于2,3-二甲氧基苯甲醛的合成。因此开发一条环境友好的,操作方便、原料易得的2,3-二甲氧基苯甲醛的工业化生产工艺具有重要的意义。
利用邻溴苯酚的甲酰化反应制备3-溴-2-羟基苯甲醛,进一步与甲醇钠及碳酸二甲酯(DMC)反应,制备2,3-二甲氧基苯甲醛。将溴的甲氧基化及羟基的醚化两步合二为一,使用碳酸二甲酯为甲基化试剂的制备2,3-二羟基苯甲醛工艺路线未有过报道。碳酸二甲酯的使用减少反应工程的毒性,反应条件温和,提高了反应收率、操作简便。
一种2,3-二甲氧基苯甲醛的制备方法,包括以下步骤:
第一步,2-羟基-3-溴苯甲醛的制备:将邻溴苯酚、无水氯化镁、三乙胺、多聚甲醛和溶剂依次放入反应器中,在50℃~120℃反应3~9h,酸化后分出有机相,除去溶剂后减压蒸馏得到2-羟基-3-溴苯甲醛;其中物料摩尔比为邻溴苯酚:无水氯化镁:三乙胺:多聚甲醛=1:0.5~3:0.5~3:2~4,溶剂的质量为邻溴苯酚质量的10~15倍;
第二步,2,3-二甲氧基苯甲醛的制备:将2-羟基-3-溴苯甲醛、亚铜盐、DMF(N,N-二甲基甲酰胺)加入到反应器中,60℃下待固体溶解后,将甲醇钠的甲醇溶液在0.5~1h内滴加入到反应器中,在50~130℃下反应3~9h,再向反应液中加入碳酸二甲酯,回流反应12~48h,得到2,3-二甲氧基苯甲醛;其中,亚铜盐的摩尔量为2-羟基-3-溴苯甲醛摩尔量的5%~20%,甲醇钠的甲醇溶液质量浓度为5%~40%,甲醇钠的摩尔量为2-羟基-3-溴苯甲醛摩尔量的1~3倍;DMF的质量为2-羟基-3-溴苯甲醛的5~10倍,碳酸二甲酯的质量为2-羟基-3-溴苯甲醛的5~15倍。
所述的第一步中溶剂为甲苯或四氢呋喃;第一步酸化过程所用的酸为盐酸、硫酸、醋酸或硝酸;第二步中亚铜盐为氯化亚铜、溴化亚铜和碘化亚铜中的一种或多种。 显示全部
2,3-二甲氧基苯甲醛是一种重要的医药中间体,主要用于黄连素的合成。

目前2,3-二甲氧基苯甲醛的生产工艺主要是由2-甲氧基-3-羟基苯甲醛与硫酸二甲酯反应而得。但是2-甲氧基-3-羟基苯甲醛价格昂贵,硫酸二甲酯毒性大,严重污染环境,制备的2,3-二甲氧基苯甲醛不适合作为医药中间体。文献报道了和碘甲烷反应制备2,3-二甲氧基苯甲醛,但成本较高,原子利用率较低。
考虑到工业生产的可行性,我们提出了以邻溴苯酚为原料经过甲酰化、溴的甲氧基化和酚羟基的醚化集成的两步法合成2,3-二甲氧基苯甲醛。其中邻溴苯酚与多聚甲醛的甲酰化反应形成3-溴-2-羟基苯甲醛已有相关文献报道(Tetrahedron Letters,2005,46:3357–3358)取代溴苯与甲醇钠反应形成取代苯甲醚也有相关报道(Tetrahedron Letters,1993,34(6):3357–3358),酚与碳酸二甲酯反应形成苯甲醚也有文献报道,但转化率较低,主要是因为用碳酸二甲酯为甲基化试剂反应条件苛刻,需要高温高压,还需要使用有毒性的相转移催化剂(Tetrahedron Letters,2002,43:2661–2663)但此方法从未用于2,3-二甲氧基苯甲醛的合成。因此开发一条环境友好的,操作方便、原料易得的2,3-二甲氧基苯甲醛的工业化生产工艺具有重要的意义。
利用邻溴苯酚的甲酰化反应制备3-溴-2-羟基苯甲醛,进一步与甲醇钠及碳酸二甲酯(DMC)反应,制备2,3-二甲氧基苯甲醛。将溴的甲氧基化及羟基的醚化两步合二为一,使用碳酸二甲酯为甲基化试剂的制备2,3-二羟基苯甲醛工艺路线未有过报道。碳酸二甲酯的使用减少反应工程的毒性,反应条件温和,提高了反应收率、操作简便。
一种2,3-二甲氧基苯甲醛的制备方法,包括以下步骤:
第一步,2-羟基-3-溴苯甲醛的制备:将邻溴苯酚、无水氯化镁、三乙胺、多聚甲醛和溶剂依次放入反应器中,在50℃~120℃反应3~9h,酸化后分出有机相,除去溶剂后减压蒸馏得到2-羟基-3-溴苯甲醛;其中物料摩尔比为邻溴苯酚:无水氯化镁:三乙胺:多聚甲醛=1:0.5~3:0.5~3:2~4,溶剂的质量为邻溴苯酚质量的10~15倍;
第二步,2,3-二甲氧基苯甲醛的制备:将2-羟基-3-溴苯甲醛、亚铜盐、DMF(N,N-二甲基甲酰胺)加入到反应器中,60℃下待固体溶解后,将甲醇钠的甲醇溶液在0.5~1h内滴加入到反应器中,在50~130℃下反应3~9h,再向反应液中加入碳酸二甲酯,回流反应12~48h,得到2,3-二甲氧基苯甲醛;其中,亚铜盐的摩尔量为2-羟基-3-溴苯甲醛摩尔量的5%~20%,甲醇钠的甲醇溶液质量浓度为5%~40%,甲醇钠的摩尔量为2-羟基-3-溴苯甲醛摩尔量的1~3倍;DMF的质量为2-羟基-3-溴苯甲醛的5~10倍,碳酸二甲酯的质量为2-羟基-3-溴苯甲醛的5~15倍。
所述的第一步中溶剂为甲苯或四氢呋喃;第一步酸化过程所用的酸为盐酸、硫酸、醋酸或硝酸;第二步中亚铜盐为氯化亚铜、溴化亚铜和碘化亚铜中的一种或多种。
 1
1
对甲氧基苯乙酮是一种白色晶体,具有特殊的香气,溶于乙醇和乙醚,但不能用于食品添加,且具有刺激性。主要用于皂用香精,市场前景广阔。

传统的合成方法是利用芳香族化合物和羧酸衍生物在催化剂作用下进行酰化反应,常用的催化剂为ALCL3。
辽宁石油化工大学的研究人员使用杂多酸作为催化剂,成功合成对甲氧基苯乙酮,但催化剂难以回收。
采用HZSM-5分子筛取代传统催化剂合成对甲氧基苯乙酮,但再生温度高,且回收率低,成本较高。
显示全部对甲氧基苯乙酮是一种白色晶体,具有特殊的香气,溶于乙醇和乙醚,但不能用于食品添加,且具有刺激性。主要用于皂用香精,市场前景广阔。

传统的合成方法是利用芳香族化合物和羧酸衍生物在催化剂作用下进行酰化反应,常用的催化剂为ALCL3。
辽宁石油化工大学的研究人员使用杂多酸作为催化剂,成功合成对甲氧基苯乙酮,但催化剂难以回收。
采用HZSM-5分子筛取代传统催化剂合成对甲氧基苯乙酮,但再生温度高,且回收率低,成本较高。
 1
1
3-羟基-6-甲基吡啶(3-Hydroxy-6-methylpyridine)是一种有机化合物,属于吡啶类衍生物。具有米色粉末外观,含有羟基和甲基,具有一定的反应活性,可生成多种有用的衍生物。此外,还具有抗氧化性质和抗菌活性。

图一 3-羟基-6-甲基吡啶
制备方法包括以2,4-二甲氧基-1,3,5-三嗪为原料,通过去甲基化反应制备。使用L-Selectride作为还原剂,可得到84%的产率。
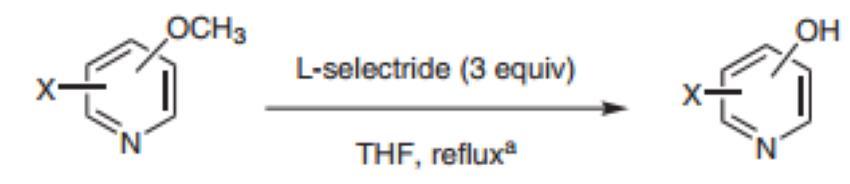
图二 3-羟基-6-甲基吡啶的合成
3-羟基-6-甲基吡啶是一种重要的合成中间体,可用于合成药物、农药、染料等精细化学品。
作为一种重要的吡啶类衍生物,3-羟基-6-甲基吡啶在化学合成、药物研发等领域具有广泛的应用前景。
[1]Igarashi K ,Kawai C ,Kurakane S .3-Hydroxy-6-Methylpyridine with Preventive Activity on Carbon Tetrachloride-Induced Liver Injury Is Produced During Roasting of Coffee Beans[J].Food science and technology research,2011,17(1):39-44. 显示全部
3-羟基-6-甲基吡啶(3-Hydroxy-6-methylpyridine)是一种有机化合物,属于吡啶类衍生物。具有米色粉末外观,含有羟基和甲基,具有一定的反应活性,可生成多种有用的衍生物。此外,还具有抗氧化性质和抗菌活性。

图一 3-羟基-6-甲基吡啶
制备方法包括以2,4-二甲氧基-1,3,5-三嗪为原料,通过去甲基化反应制备。使用L-Selectride作为还原剂,可得到84%的产率。

图二 3-羟基-6-甲基吡啶的合成
3-羟基-6-甲基吡啶是一种重要的合成中间体,可用于合成药物、农药、染料等精细化学品。
作为一种重要的吡啶类衍生物,3-羟基-6-甲基吡啶在化学合成、药物研发等领域具有广泛的应用前景。
[1]Igarashi K ,Kawai C ,Kurakane S .3-Hydroxy-6-Methylpyridine with Preventive Activity on Carbon Tetrachloride-Induced Liver Injury Is Produced During Roasting of Coffee Beans[J].Food science and technology research,2011,17(1):39-44.
 1
1
噻吩并[3,2-b]噻吩,英文名为Thieno[3,2-b]thiophene,常温常压下为白色固体粉末,在水中溶解性差但是可溶于甲醇。噻吩并[3,2-b]噻吩是一种双噻吩类化合物,其分子整体具有丰富的电子云密度,可与常见的亲电型卤化试剂发生溴化或者碘化反应。该物质可用作有机电子器件的合成原料,它在有机太阳能电池、有机场效应晶体管和有机发光二极管(OLED)的制备中有一定的应用。
噻吩并[3,2-b]噻吩具有丰富的电子云密度,因此它能进行多种芳香亲电取代反应,最为常见的是它可在亲电试剂例如NBS,NCS等作用下在呋喃环的2号位引入一个卤素原子(包括氯,溴,碘)。值得说明的是由于该物质具有较为对称的化学结构,通过控制反应条件可在噻吩环上引入一个或者两个卤原子,拓展了其反应多样性。
噻吩并[3,2-b]噻吩的制备方法可以通过串联两步反应来实现。首先将噻吩与亚硫酰氯反应生成噻吩-2-亚砜基化合物,然后通过硫化物还原和氢化处理生成噻吩[3,2-b]并二噻吩。
![噻吩并[3,2-b]噻吩的卤化反应 噻吩并[3,2-b]噻吩的卤化反应](https://imgen4.guidechem.com/img/answer/2024/10/16/1729034615011305.jpg)
图1 噻吩并[3,2-b]噻吩的卤化反应
在一个干燥的反应烧瓶中将噻吩并[3,2-b]噻吩 (5.61 g, 40 mmol)溶于干燥的DMF (80 mL)中,将其在室温下进行搅拌溶解。然后往上述反应混合物中加入N-氯琥珀酰亚胺(10.68 g, 80 mmol)。将所得的反应混合物在室温下剧烈搅拌反应大约6小时。反应结束后向上述反应混合物中加水,并用乙醚将混合物萃取三次。用水清洗有机相4次,然后在MgSO4上干燥有机相。将反应混合物进行过滤以除去干燥剂并将所得的滤液在真空下进行浓缩,所得的残余物通过硅胶(戊烷)柱层析法进行分离纯化即可得到目标产物分子。
由于其对称的化学结构和丰富的电子云密度,噻吩并[3,2-b]噻吩在材料科学领域具有潜在的应用,它可以用于合成具有特殊电子性质的半导体聚合物,可用于光伏材料、传感器等领域。
[1] Kunz, Thomas; et al Chemistry-A European Journal (2011), 17(3), 866-872.
显示全部噻吩并[3,2-b]噻吩,英文名为Thieno[3,2-b]thiophene,常温常压下为白色固体粉末,在水中溶解性差但是可溶于甲醇。噻吩并[3,2-b]噻吩是一种双噻吩类化合物,其分子整体具有丰富的电子云密度,可与常见的亲电型卤化试剂发生溴化或者碘化反应。该物质可用作有机电子器件的合成原料,它在有机太阳能电池、有机场效应晶体管和有机发光二极管(OLED)的制备中有一定的应用。
噻吩并[3,2-b]噻吩具有丰富的电子云密度,因此它能进行多种芳香亲电取代反应,最为常见的是它可在亲电试剂例如NBS,NCS等作用下在呋喃环的2号位引入一个卤素原子(包括氯,溴,碘)。值得说明的是由于该物质具有较为对称的化学结构,通过控制反应条件可在噻吩环上引入一个或者两个卤原子,拓展了其反应多样性。
噻吩并[3,2-b]噻吩的制备方法可以通过串联两步反应来实现。首先将噻吩与亚硫酰氯反应生成噻吩-2-亚砜基化合物,然后通过硫化物还原和氢化处理生成噻吩[3,2-b]并二噻吩。
![噻吩并[3,2-b]噻吩的卤化反应 噻吩并[3,2-b]噻吩的卤化反应](https://imgen4.guidechem.com/img/answer/2024/10/16/1729034615011305.jpg)
图1 噻吩并[3,2-b]噻吩的卤化反应
在一个干燥的反应烧瓶中将噻吩并[3,2-b]噻吩 (5.61 g, 40 mmol)溶于干燥的DMF (80 mL)中,将其在室温下进行搅拌溶解。然后往上述反应混合物中加入N-氯琥珀酰亚胺(10.68 g, 80 mmol)。将所得的反应混合物在室温下剧烈搅拌反应大约6小时。反应结束后向上述反应混合物中加水,并用乙醚将混合物萃取三次。用水清洗有机相4次,然后在MgSO4上干燥有机相。将反应混合物进行过滤以除去干燥剂并将所得的滤液在真空下进行浓缩,所得的残余物通过硅胶(戊烷)柱层析法进行分离纯化即可得到目标产物分子。
由于其对称的化学结构和丰富的电子云密度,噻吩并[3,2-b]噻吩在材料科学领域具有潜在的应用,它可以用于合成具有特殊电子性质的半导体聚合物,可用于光伏材料、传感器等领域。
[1] Kunz, Thomas; et al Chemistry-A European Journal (2011), 17(3), 866-872.
 1
1
2-溴-5-羟基吡啶,英文名:6-Brompyridin-3-ol,CAS号:55717-40-3,分子量:173.995,密度:1.8±0.1 g/cm3,沸点:373.0±22.0°C at 760 mmHg,分子式:C5H4BrNO,闪点:179.4±22.3°C,蒸汽压:0.0±0.9 mmHg at 25°C,淡黄色固体,室温干燥处保存。

在装配有机械搅拌器、热电偶和氮气入口的250mL三颈烧瓶中将2,5-二溴吡啶(V)(9.98g,42.1mmol)在氮气下溶解于53mL无水THF中。形成浅褐色溶液。经3min经由注射器添加i-PrMgCl在乙醚(23mL)中的2M溶液。当已经添加大约50%的格氏溶液(Grignard solution)时,形成棕色悬浮液。i-PrMgCl的添加导致达到36℃的放热。搅拌90min后,将悬浮液冷却至2℃,并且经由注射器快速地添加纯的硼酸三甲酯。反应放热至6℃,并且移除冰浴。搅拌过夜后,添加冰乙酸(3.79g),使得所有固体溶解并且形成深棕色溶液。将溶液在冰浴中冷却并且以保持反应温度不超过12℃的速度滴加5.25g30%过氧化氢(氧化剂)。将反应混合物搅拌90分钟,然后添加二乙醚(diethyl ether)(150mL)和水(100mL)。将水层分离并且用乙醚(ether)(2×100mL)萃取。将合并的有机物用100mL 10%亚硫酸氢钠溶液洗涤,然后用盐水洗涤。将萃取物干燥(MgSO4)并且旋转蒸发至棕色油状物,其静置时形成褐色固体(7.95g)。将粗产物吸附至15g Celite?上,并且使用220g二氧化硅柱和己烷/EtOAc梯度通过快速层析法纯化。使级分(fractions)蒸发以得到2-溴-5-羟基吡啶4.81g(66%收率)为米黄色固体。1HNMR(DMSO-d6,400MHz)δ:10.24(s,1H),7.94(d,J=3.0Hz,1H),7.42(d,J=8.6Hz,1H),7.17 (dd,J=3.0,8.6Hz,1H);13CNMR(DMSO-d6,101MHz)δ:153.74,138.13,129.30,128.14,126.21[1].
1、专利CN202010668194.8公开了一种金属聚合物、金属聚合物纳米胶束及其制备方法和应用,聚合物I-1的合成第一步,称取2-溴-5-羟基吡啶(10.0g,57.4mmol),对甲基苯磺酰氯(16.0g,86.1mmol),Et3N(8mL)溶于DCM(200mL)中,室温搅拌2h。反应结束,除去溶剂,硅胶柱层析(洗脱剂为二氯甲烷/甲醇=50/1)纯化得白色固体粉末(13.0g,77.0%),得到中间体化合物1[2].
2、专利CN201910711937.2公开了一种新型硝基咪唑类化合物的制备方法,在化合物8的制备中,第一步将N-Boc-4-羟基哌啶(3g,14.937mmol),2-溴-5羟基吡啶(2g,11.49mmol),三苯基膦(3.615g,13.788mmol),溶于甲苯(50ml)中,冰浴下滴加DIAD(2.788g,13.788mmol)5min , 加热至110℃回流过夜,TLC检测反应完毕,加入水(50ml),二氯甲烷(50ml),水相用二氯甲 烷(20ml×3)萃取,有机相水(25ml×1)洗,饱和食盐水(25ml×1)洗,无水硫酸钠干燥,过滤旋干,柱层析(PE/EA=50:1-30:1),得中间体化合物8-1为白色固体(2.88g,70%)[3].
[1]美国陶氏益农公司. 4-((6-(2-(2,4-二氟苯基)-1,1-二氟-2-氧代乙基)吡啶-3-基)氧基)苄腈以及制备方法:CN201680079078.4[P]. 2018-11-23.
[2]东南大学. 一种金属聚合物、金属聚合物纳米胶束及其制备方法和应用:CN202010668194.8[P]. 2020-11-17.
[3]上海阳帆医药科技有限公司. 硝基咪唑类化合物及其制备方法和用途:CN201910711937.2[P]. 2021-02-02.
显示全部2-溴-5-羟基吡啶,英文名:6-Brompyridin-3-ol,CAS号:55717-40-3,分子量:173.995,密度:1.8±0.1 g/cm3,沸点:373.0±22.0°C at 760 mmHg,分子式:C5H4BrNO,闪点:179.4±22.3°C,蒸汽压:0.0±0.9 mmHg at 25°C,淡黄色固体,室温干燥处保存。

在装配有机械搅拌器、热电偶和氮气入口的250mL三颈烧瓶中将2,5-二溴吡啶(V)(9.98g,42.1mmol)在氮气下溶解于53mL无水THF中。形成浅褐色溶液。经3min经由注射器添加i-PrMgCl在乙醚(23mL)中的2M溶液。当已经添加大约50%的格氏溶液(Grignard solution)时,形成棕色悬浮液。i-PrMgCl的添加导致达到36℃的放热。搅拌90min后,将悬浮液冷却至2℃,并且经由注射器快速地添加纯的硼酸三甲酯。反应放热至6℃,并且移除冰浴。搅拌过夜后,添加冰乙酸(3.79g),使得所有固体溶解并且形成深棕色溶液。将溶液在冰浴中冷却并且以保持反应温度不超过12℃的速度滴加5.25g30%过氧化氢(氧化剂)。将反应混合物搅拌90分钟,然后添加二乙醚(diethyl ether)(150mL)和水(100mL)。将水层分离并且用乙醚(ether)(2×100mL)萃取。将合并的有机物用100mL 10%亚硫酸氢钠溶液洗涤,然后用盐水洗涤。将萃取物干燥(MgSO4)并且旋转蒸发至棕色油状物,其静置时形成褐色固体(7.95g)。将粗产物吸附至15g Celite?上,并且使用220g二氧化硅柱和己烷/EtOAc梯度通过快速层析法纯化。使级分(fractions)蒸发以得到2-溴-5-羟基吡啶4.81g(66%收率)为米黄色固体。1HNMR(DMSO-d6,400MHz)δ:10.24(s,1H),7.94(d,J=3.0Hz,1H),7.42(d,J=8.6Hz,1H),7.17 (dd,J=3.0,8.6Hz,1H);13CNMR(DMSO-d6,101MHz)δ:153.74,138.13,129.30,128.14,126.21[1].
1、专利CN202010668194.8公开了一种金属聚合物、金属聚合物纳米胶束及其制备方法和应用,聚合物I-1的合成第一步,称取2-溴-5-羟基吡啶(10.0g,57.4mmol),对甲基苯磺酰氯(16.0g,86.1mmol),Et3N(8mL)溶于DCM(200mL)中,室温搅拌2h。反应结束,除去溶剂,硅胶柱层析(洗脱剂为二氯甲烷/甲醇=50/1)纯化得白色固体粉末(13.0g,77.0%),得到中间体化合物1[2].
2、专利CN201910711937.2公开了一种新型硝基咪唑类化合物的制备方法,在化合物8的制备中,第一步将N-Boc-4-羟基哌啶(3g,14.937mmol),2-溴-5羟基吡啶(2g,11.49mmol),三苯基膦(3.615g,13.788mmol),溶于甲苯(50ml)中,冰浴下滴加DIAD(2.788g,13.788mmol)5min , 加热至110℃回流过夜,TLC检测反应完毕,加入水(50ml),二氯甲烷(50ml),水相用二氯甲 烷(20ml×3)萃取,有机相水(25ml×1)洗,饱和食盐水(25ml×1)洗,无水硫酸钠干燥,过滤旋干,柱层析(PE/EA=50:1-30:1),得中间体化合物8-1为白色固体(2.88g,70%)[3].
[1]美国陶氏益农公司. 4-((6-(2-(2,4-二氟苯基)-1,1-二氟-2-氧代乙基)吡啶-3-基)氧基)苄腈以及制备方法:CN201680079078.4[P]. 2018-11-23.
[2]东南大学. 一种金属聚合物、金属聚合物纳米胶束及其制备方法和应用:CN202010668194.8[P]. 2020-11-17.
[3]上海阳帆医药科技有限公司. 硝基咪唑类化合物及其制备方法和用途:CN201910711937.2[P]. 2021-02-02.
 1
1
3-苯丙酸甲酯,英文名:Methyl 3-phenylpropanoate,CAS号:103-25-3,分子量:164.201,密度:1.0±0.1 g/cm3,沸点:238.5±0.0°C at 760 mmHg,分子式:C10H12O2,闪点:100.0±0.0°C,蒸汽压:0.0±0.4 mmHg at 25°C,白色晶体,储存于阴凉、通风的库房。

将苯丙酸(100mg,0.67mmol),DMF(4 mL),叔丁醇钾(224 mg,2.0mmol,3eq)依次加入反应瓶中,常温搅拌5分钟后,待叔丁醇钾均匀分散后,向反应瓶中缓慢注入三氟乙酸甲酯(0.27mL,2.7mmol,4eq),反应4个小时后,TLC点板,原料点消失,停止搅拌。用乙酸乙酯和蒸馏水萃取两次,再用饱和NaC1溶液洗涤,合并有机相,无水硫酸镁干燥有机相,过滤除去硫酸镁,旋蒸蒸除溶剂,柱层析提纯得无色液体3-苯丙酸甲酯(80mg,产率73%)。1HNMR(400MHz,CDCl3)δ-7.30(d,J=7.0Hz,2H),7.22(d,J=7.8 Hz,3H),3.70(s,3H),2.98(t,J=7.8Hz,2H),2.66(t,J=7.9Hz,2H);13CNMR(100MHz,CDCl3)δ-173.32,140.54,128.52,128.29,126.29,51.58,35.71,30.97[1]。
1、专利CN201710874743.5公开了一种以羧酸酯,氢气为原料或者以二氧化碳、氢气和胺类化合物为原料,在过渡金属络合物为催化剂,在有机溶剂中或者无溶剂条件下反应,形成相应的醇类化合物。其中实施例62以万分之一摩尔当量钌络合物催化3-苯丙酸甲酯氢化制得苯丙醇,产率达99%[2]。
2、专利CN202210285486.2提供了一种5?硝基亚氨基?4H?1,2,4?三唑类化合物及其制备方法,实施例1中以3?苯丙酸甲酯(0.1168mol)为原料,在100mL甲醇溶剂中,加入80%水合肼(0 .5840mol)并加热至回流过夜反应,经后处理得到3-苯基丙酰肼(化合物1),产率99.6%[3]。
3、专利CN201910281377.1公开一种一种不饱和酮类化合物的制备方法中,实施例1的化合物的合成中,N2保护下,将甲基磷酸二甲酯(1.3mL,12.2mmol)溶于干燥的THF(15mL)后,冷却至-78℃,滴加n-BuLi溶液(2.4M in THF,5.6mL),于-78℃下搅拌30min后,加入3-苯基丙酸甲酯(1.0g,6.1mmol)的四氢呋喃溶液(5mL)于-78℃下搅拌1h后,TLC监测反应完全。经后处理得到中间体2-氧代-4-苯基丁基磷酸二甲酯[4]。
[1]广东石油化工学院. 一种甲基化反应的方法:CN201811224832.6[P]. 2019-01-11.
[2]中国科学院上海有机化学研究所. 新型钳形金属络合物及其应用:CN201710874743.5[P]. 2019-04-02.
[3]赣南师范大学. 一种5-硝基亚氨基-4H-1,2,4-三唑类化合物及其制备方法和应用:CN202210285486.2[P]. 2022-06-17.
[4]中国科学院上海药物研究所,复旦大学. 一种不饱和酮类化合物、其制备方法和用途:CN201910281377.1[P]. 2020-10-20. 显示全部
3-苯丙酸甲酯,英文名:Methyl 3-phenylpropanoate,CAS号:103-25-3,分子量:164.201,密度:1.0±0.1 g/cm3,沸点:238.5±0.0°C at 760 mmHg,分子式:C10H12O2,闪点:100.0±0.0°C,蒸汽压:0.0±0.4 mmHg at 25°C,白色晶体,储存于阴凉、通风的库房。

将苯丙酸(100mg,0.67mmol),DMF(4 mL),叔丁醇钾(224 mg,2.0mmol,3eq)依次加入反应瓶中,常温搅拌5分钟后,待叔丁醇钾均匀分散后,向反应瓶中缓慢注入三氟乙酸甲酯(0.27mL,2.7mmol,4eq),反应4个小时后,TLC点板,原料点消失,停止搅拌。用乙酸乙酯和蒸馏水萃取两次,再用饱和NaC1溶液洗涤,合并有机相,无水硫酸镁干燥有机相,过滤除去硫酸镁,旋蒸蒸除溶剂,柱层析提纯得无色液体3-苯丙酸甲酯(80mg,产率73%)。1HNMR(400MHz,CDCl3)δ-7.30(d,J=7.0Hz,2H),7.22(d,J=7.8 Hz,3H),3.70(s,3H),2.98(t,J=7.8Hz,2H),2.66(t,J=7.9Hz,2H);13CNMR(100MHz,CDCl3)δ-173.32,140.54,128.52,128.29,126.29,51.58,35.71,30.97[1]。
1、专利CN201710874743.5公开了一种以羧酸酯,氢气为原料或者以二氧化碳、氢气和胺类化合物为原料,在过渡金属络合物为催化剂,在有机溶剂中或者无溶剂条件下反应,形成相应的醇类化合物。其中实施例62以万分之一摩尔当量钌络合物催化3-苯丙酸甲酯氢化制得苯丙醇,产率达99%[2]。
2、专利CN202210285486.2提供了一种5?硝基亚氨基?4H?1,2,4?三唑类化合物及其制备方法,实施例1中以3?苯丙酸甲酯(0.1168mol)为原料,在100mL甲醇溶剂中,加入80%水合肼(0 .5840mol)并加热至回流过夜反应,经后处理得到3-苯基丙酰肼(化合物1),产率99.6%[3]。
3、专利CN201910281377.1公开一种一种不饱和酮类化合物的制备方法中,实施例1的化合物的合成中,N2保护下,将甲基磷酸二甲酯(1.3mL,12.2mmol)溶于干燥的THF(15mL)后,冷却至-78℃,滴加n-BuLi溶液(2.4M in THF,5.6mL),于-78℃下搅拌30min后,加入3-苯基丙酸甲酯(1.0g,6.1mmol)的四氢呋喃溶液(5mL)于-78℃下搅拌1h后,TLC监测反应完全。经后处理得到中间体2-氧代-4-苯基丁基磷酸二甲酯[4]。
[1]广东石油化工学院. 一种甲基化反应的方法:CN201811224832.6[P]. 2019-01-11.
[2]中国科学院上海有机化学研究所. 新型钳形金属络合物及其应用:CN201710874743.5[P]. 2019-04-02.
[3]赣南师范大学. 一种5-硝基亚氨基-4H-1,2,4-三唑类化合物及其制备方法和应用:CN202210285486.2[P]. 2022-06-17.
[4]中国科学院上海药物研究所,复旦大学. 一种不饱和酮类化合物、其制备方法和用途:CN201910281377.1[P]. 2020-10-20.
 1
1
环己基氯化镁,英文名:chlorocyclohexylmagnesium,CAS号:931-51-1,分子量:142.91000,密度:0.871 g/mL at 25oC,沸点:80.7oC at 760 mmHg,分子式:C6H11ClMg,闪点:-40°F,为透明非常暗棕色溶液,密封贮藏,储存在阴凉、干燥的地方,远离火源,易燃易爆区,腐蚀区,水区。避免阳光直射。室温储存。常用氮气保护。

将三甲氧基苯(1.0062g,6mmol)溶液加入20mL干燥的四氢呋喃中,在N2下滴入正丁基锂(2.6mL,2.5M正己烷溶液,6.6mmol)。室温搅拌4.5小时,冷却至-78℃,滴加二环己基膦。混合物搅拌30分钟后,将反应系统加热至室温,再搅拌18小时。乙酸乙酯萃取,水洗,无水硫酸钠干燥,柱层析纯化(石油醚/乙酸乙酯=10-15/1),所得环己氯化镁产品0.5514g。收率是25%。1HNMR(300MHz,CDCl3)δ-6.08(d,J=1.5Hz,2H),3.81(s,3H),3.77(s,6H),2.30-2.16(m,2H),1.92-1.54(m,8H),1.48-0.90(m,12H);31PNMR(121 MHz,CDCl3)δ-14.6[1]。
1、在专利CN201610030857.7实施例十六中介绍了[Fe(PR3)X3][(R1NCHnCHnNR1)CH](R1为2,6-二异丙基苯基,R为环己基,n为1,X为Br)催化的环己基氯化镁与磷酸二乙-2-吡啶酯的交叉偶联反应:在经过脱水脱氧处理过的反应瓶中,在氩气保护下依次加入催化剂的四氢呋喃溶液1.0毫升(5.0×105毫摩尔/毫升),磷酸二乙-2-吡啶酯0.12克(0.5毫摩尔)和四氢呋喃2.0毫升。在0°C下缓慢滴加环己基氯化镁的四氢呋喃溶液2.0毫升(1.0毫摩尔/毫升),搅拌5分钟。升至25℃搅拌反应10小时,用去离子水终止反应,反应产物用乙酸乙酯萃取,层析柱提纯(以石油醚为展开剂),产率80%[2]。
2、专利CN200780032144.3实施例1中步骤B关于[4-(环己基-羟基-甲基)-苯基1-(4-异丙基-哌嗪-1-基)-甲酮的合成,在-78°C向4-(4-异丙基-哌嗪-1-羰基)-苯甲醛(351mg,1.35mmol)在THF(15mL)内的溶液中加入环己基氯化镁(2.0M在Et2O中的溶液;0.81mL,1.62mmol)。让该混合物温热至室温并且搅拌5小时。用饱和NH4Cl水溶液中止该反应,倒入H2O内,并且用3批CH2Cl2萃取。将合并的有机层干燥(Na2SO4)并浓缩。通过制备反相HPLC来纯化残余粗产物,获得了目标产物[3]。
[1]ZHEJIANG UNIVERSITY. Structure and method for synthesizing and using dialkyl(2,4,6- or 2,6-alkoxyphenyl)phosphine and its tetrafluoroborate:US200913383208[P]. 2015-04-14.
[2]苏州大学. 一种离子型铁(II)配合物及其制备方法与应用:CN201610030857.7[P]. 2016-05-04.
[3]詹森药业有限公司. 组胺H<sub>3</sub>受体的取代的苯甲酰胺调节剂:CN200780032144.3[P]. 2009-08-19.
显示全部环己基氯化镁,英文名:chlorocyclohexylmagnesium,CAS号:931-51-1,分子量:142.91000,密度:0.871 g/mL at 25oC,沸点:80.7oC at 760 mmHg,分子式:C6H11ClMg,闪点:-40°F,为透明非常暗棕色溶液,密封贮藏,储存在阴凉、干燥的地方,远离火源,易燃易爆区,腐蚀区,水区。避免阳光直射。室温储存。常用氮气保护。

将三甲氧基苯(1.0062g,6mmol)溶液加入20mL干燥的四氢呋喃中,在N2下滴入正丁基锂(2.6mL,2.5M正己烷溶液,6.6mmol)。室温搅拌4.5小时,冷却至-78℃,滴加二环己基膦。混合物搅拌30分钟后,将反应系统加热至室温,再搅拌18小时。乙酸乙酯萃取,水洗,无水硫酸钠干燥,柱层析纯化(石油醚/乙酸乙酯=10-15/1),所得环己氯化镁产品0.5514g。收率是25%。1HNMR(300MHz,CDCl3)δ-6.08(d,J=1.5Hz,2H),3.81(s,3H),3.77(s,6H),2.30-2.16(m,2H),1.92-1.54(m,8H),1.48-0.90(m,12H);31PNMR(121 MHz,CDCl3)δ-14.6[1]。
1、在专利CN201610030857.7实施例十六中介绍了[Fe(PR3)X3][(R1NCHnCHnNR1)CH](R1为2,6-二异丙基苯基,R为环己基,n为1,X为Br)催化的环己基氯化镁与磷酸二乙-2-吡啶酯的交叉偶联反应:在经过脱水脱氧处理过的反应瓶中,在氩气保护下依次加入催化剂的四氢呋喃溶液1.0毫升(5.0×105毫摩尔/毫升),磷酸二乙-2-吡啶酯0.12克(0.5毫摩尔)和四氢呋喃2.0毫升。在0°C下缓慢滴加环己基氯化镁的四氢呋喃溶液2.0毫升(1.0毫摩尔/毫升),搅拌5分钟。升至25℃搅拌反应10小时,用去离子水终止反应,反应产物用乙酸乙酯萃取,层析柱提纯(以石油醚为展开剂),产率80%[2]。
2、专利CN200780032144.3实施例1中步骤B关于[4-(环己基-羟基-甲基)-苯基1-(4-异丙基-哌嗪-1-基)-甲酮的合成,在-78°C向4-(4-异丙基-哌嗪-1-羰基)-苯甲醛(351mg,1.35mmol)在THF(15mL)内的溶液中加入环己基氯化镁(2.0M在Et2O中的溶液;0.81mL,1.62mmol)。让该混合物温热至室温并且搅拌5小时。用饱和NH4Cl水溶液中止该反应,倒入H2O内,并且用3批CH2Cl2萃取。将合并的有机层干燥(Na2SO4)并浓缩。通过制备反相HPLC来纯化残余粗产物,获得了目标产物[3]。
[1]ZHEJIANG UNIVERSITY. Structure and method for synthesizing and using dialkyl(2,4,6- or 2,6-alkoxyphenyl)phosphine and its tetrafluoroborate:US200913383208[P]. 2015-04-14.
[2]苏州大学. 一种离子型铁(II)配合物及其制备方法与应用:CN201610030857.7[P]. 2016-05-04.
[3]詹森药业有限公司. 组胺H<sub>3</sub>受体的取代的苯甲酰胺调节剂:CN200780032144.3[P]. 2009-08-19.
 1
1
10-十一烯醛,英文名为10-Undecenal,是一种不饱和醛类化合物,具有特殊且强烈的椰子香气。它天然存在于桃子、杏子、番茄、朗姆酒和炒大麦等食物中,可用作多种食品的香料添加剂,在冷饮和糖果的加工生产领域中有较好的应用。

图1 10-十一烯醛的性状图
10-十一烯醛具有较低的熔点,常温下为液体状态,但在较低温度下会转变为固体。
10-十一烯醛是一种具有长烷基链的不饱和烯醛类化合物,具有较好的化学转化性质。其结构中含有末端双键单元和醛基结构,可发生多种化学反应。
10-十一烯醛在食品、化妆品和个人护理产品等领域有广泛应用,是一种重要的食品香料。其独特的椰子香气使其成为冷饮、糖果和甜点制作中常用的香料。
[1] 边瑞芳,汤坚,顾晓红等. 10-十一烯醛乙二醇缩醛的合成及在卷烟中的应用[J]. 烟草科技, 2006(5): 4.
显示全部10-十一烯醛,英文名为10-Undecenal,是一种不饱和醛类化合物,具有特殊且强烈的椰子香气。它天然存在于桃子、杏子、番茄、朗姆酒和炒大麦等食物中,可用作多种食品的香料添加剂,在冷饮和糖果的加工生产领域中有较好的应用。

图1 10-十一烯醛的性状图
10-十一烯醛具有较低的熔点,常温下为液体状态,但在较低温度下会转变为固体。
10-十一烯醛是一种具有长烷基链的不饱和烯醛类化合物,具有较好的化学转化性质。其结构中含有末端双键单元和醛基结构,可发生多种化学反应。
10-十一烯醛在食品、化妆品和个人护理产品等领域有广泛应用,是一种重要的食品香料。其独特的椰子香气使其成为冷饮、糖果和甜点制作中常用的香料。
[1] 边瑞芳,汤坚,顾晓红等. 10-十一烯醛乙二醇缩醛的合成及在卷烟中的应用[J]. 烟草科技, 2006(5): 4.
 1
1
7-氯-1H-吲哚,英文名为7-Chloroindole,是一种白色结晶固体,不溶于水但溶于甲醇、乙酸乙酯和氯仿。它属于吲哚类衍生物,具有特殊的刺激性气味,可用作有机合成中间体,用于制备含有7-卤代吲哚结构的功能有机分子。
7-氯-1H-吲哚具有较高的化学反应活性,可在钠氢的作用下发生亲核取代反应,形成N-烷基化的衍生物。此外,它还可在过渡金属催化作用下和有机硼酸类化合物发生交叉偶联反应。
7-氯-1H-吲哚可在还原剂的作用下发生还原反应,得到相应的苯并吡咯类衍生物。

图1 7-氯-1H-吲哚的还原反应
在一个干燥的反应器中将7-氯- 1h -吲哚溶解于乙酸中,然后加入三硼氢化钠,反应后用NaOH水溶液萃取反应混合物,最终得到目标产物分子。
7-氯-1H-吲哚作为一种具有特殊结构和化学反应活性的吲哚类衍生物,在有机合成、医药化学和材料科学领域有广泛应用。它可用于合成含有7-卤代吲哚结构的功能有机分子,在药物合成和材料科学等领域具有广泛应用。
[1] Sato, Kenjiro; et al Bioorganic & Medicinal Chemistry (2014), 22(5), 1649-1666. 显示全部
7-氯-1H-吲哚,英文名为7-Chloroindole,是一种白色结晶固体,不溶于水但溶于甲醇、乙酸乙酯和氯仿。它属于吲哚类衍生物,具有特殊的刺激性气味,可用作有机合成中间体,用于制备含有7-卤代吲哚结构的功能有机分子。
7-氯-1H-吲哚具有较高的化学反应活性,可在钠氢的作用下发生亲核取代反应,形成N-烷基化的衍生物。此外,它还可在过渡金属催化作用下和有机硼酸类化合物发生交叉偶联反应。
7-氯-1H-吲哚可在还原剂的作用下发生还原反应,得到相应的苯并吡咯类衍生物。

图1 7-氯-1H-吲哚的还原反应
在一个干燥的反应器中将7-氯- 1h -吲哚溶解于乙酸中,然后加入三硼氢化钠,反应后用NaOH水溶液萃取反应混合物,最终得到目标产物分子。
7-氯-1H-吲哚作为一种具有特殊结构和化学反应活性的吲哚类衍生物,在有机合成、医药化学和材料科学领域有广泛应用。它可用于合成含有7-卤代吲哚结构的功能有机分子,在药物合成和材料科学等领域具有广泛应用。
[1] Sato, Kenjiro; et al Bioorganic & Medicinal Chemistry (2014), 22(5), 1649-1666.
 1
1
2-甲基-3-四氢呋喃硫醇(2-Methyltetrahydrofuran-3-thiol,FEMA号3787)是一种重要的含硫香料,具有浓郁的肉香和烤肉香,是肉类香精配方中常用的香料之一。

本文介绍了一种制备2-甲基-3-四氢呋喃硫醇的方法,通过更换主要原料和调整反应条件,降低生产成本,提高产品收率。
详细的制备方法包括多个步骤,从原料准备到反应条件控制,最终得到高收率的2-甲基-3-四氢呋喃硫醇。
[1]滕州瑞元香料有限公司. 一种2-甲基-3-四氢呋喃硫醇的制备方法:CN202210728245.0[P]. 2022-09-16. 显示全部
2-甲基-3-四氢呋喃硫醇(2-Methyltetrahydrofuran-3-thiol,FEMA号3787)是一种重要的含硫香料,具有浓郁的肉香和烤肉香,是肉类香精配方中常用的香料之一。

本文介绍了一种制备2-甲基-3-四氢呋喃硫醇的方法,通过更换主要原料和调整反应条件,降低生产成本,提高产品收率。
详细的制备方法包括多个步骤,从原料准备到反应条件控制,最终得到高收率的2-甲基-3-四氢呋喃硫醇。
[1]滕州瑞元香料有限公司. 一种2-甲基-3-四氢呋喃硫醇的制备方法:CN202210728245.0[P]. 2022-09-16.
 1
1
肌氨酸乙酯盐酸盐(Ethyl sarcosinate hydrochloride),分子式C5H12ClNO2,对水体有危害。外观为白色针状结晶或粉末。

图一 肌氨酸乙酯盐酸盐
称取5?氟?2?硝基苯甲酸(1.0g,5.4mmol,CAS No.320?98?9;安耐吉化学)、1?乙 基?(3?二甲基氨基丙基)碳酰二亚胺盐酸盐(1.2g,6.5mmol;EDCI,CAS No.:25952?53?8,安 耐吉化学)、1?羟基苯并三唑(0.87g,6.5mmol;CAS No:2592?95?2,安耐吉化学)置于反应瓶 (100mL),加入二氯甲烷(20mL)搅拌溶解,室温活化30min;另分别称取肌氨酸甲酯盐酸盐 (0.75g,5.4mmol,CAS No.13515?93?0,安耐吉化学)、三乙胺(1.0g,10.8mmol,国药集团)溶 于二氯甲烷(10mL)后,依次加入到反应瓶中,室温反应12h。以水/二氯甲烷(v:v=1:1,50ml×2)淬灭反应液,合并有机相,以无水硫酸 钠干燥后减压浓缩得棕色黄色油状物a;将a经硅胶柱层析,以二氯甲烷/乙酸乙酯(v:v=8: 1)为洗脱液,分得淡黄色油状物b;将油状物b溶于乙酸乙酯/石油醚(4mL,v:v=1:3,)混合 溶液,超声处理30min,有大量后固体析出,抽滤,得淡黄色固体约1.1g,收率为85.4%。称取7?氟?3,4?二氢?4?甲基?1H?[1,4]苯并二氮卓?2,5?二酮(2.0g,9.6mmol)、五 氯化磷(2.4g,11.5mmol)置于反应瓶(50mL),加入N,N?二甲基甲酰胺(0.2mL)和四氢呋喃 (20mL),70℃回流5h。反应液旋转蒸发浓缩近干,得糖浆状物,称重2.15g,收率为95%,称取碳酸铯(4.7g,14mmol)置于反应瓶(50mL),加入四氢呋喃(20mL)搅拌使溶解, 再加入异氰基乙酸乙酯(1.3g,11.5mmol;CAS No 2999?46?4)。冰水浴使体系温度降至0℃。 将步骤(3)所得2.15g糖浆状物溶于四氢呋喃(10mL),滴加入反应瓶,30分钟加入完毕,然后 室温反应4h。减压浓缩得棕色油状物,将此油状物以乙腈溶解,经0.24um滤膜过滤处理后高效液相法分析,收率为30.5%[1]。
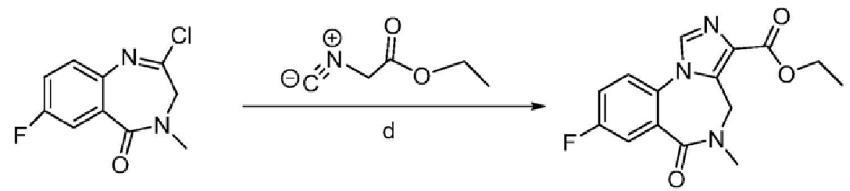
图二 肌氨酸乙酯盐酸盐制备氟马西尼
[1]何新华,张学敏,周涛等. 一种氟马西尼的制备方法[P]. 浙江省:CN112979658B,2022-05-31.
显示全部肌氨酸乙酯盐酸盐(Ethyl sarcosinate hydrochloride),分子式C5H12ClNO2,对水体有危害。外观为白色针状结晶或粉末。

图一 肌氨酸乙酯盐酸盐
称取5?氟?2?硝基苯甲酸(1.0g,5.4mmol,CAS No.320?98?9;安耐吉化学)、1?乙 基?(3?二甲基氨基丙基)碳酰二亚胺盐酸盐(1.2g,6.5mmol;EDCI,CAS No.:25952?53?8,安 耐吉化学)、1?羟基苯并三唑(0.87g,6.5mmol;CAS No:2592?95?2,安耐吉化学)置于反应瓶 (100mL),加入二氯甲烷(20mL)搅拌溶解,室温活化30min;另分别称取肌氨酸甲酯盐酸盐 (0.75g,5.4mmol,CAS No.13515?93?0,安耐吉化学)、三乙胺(1.0g,10.8mmol,国药集团)溶 于二氯甲烷(10mL)后,依次加入到反应瓶中,室温反应12h。以水/二氯甲烷(v:v=1:1,50ml×2)淬灭反应液,合并有机相,以无水硫酸 钠干燥后减压浓缩得棕色黄色油状物a;将a经硅胶柱层析,以二氯甲烷/乙酸乙酯(v:v=8: 1)为洗脱液,分得淡黄色油状物b;将油状物b溶于乙酸乙酯/石油醚(4mL,v:v=1:3,)混合 溶液,超声处理30min,有大量后固体析出,抽滤,得淡黄色固体约1.1g,收率为85.4%。称取7?氟?3,4?二氢?4?甲基?1H?[1,4]苯并二氮卓?2,5?二酮(2.0g,9.6mmol)、五 氯化磷(2.4g,11.5mmol)置于反应瓶(50mL),加入N,N?二甲基甲酰胺(0.2mL)和四氢呋喃 (20mL),70℃回流5h。反应液旋转蒸发浓缩近干,得糖浆状物,称重2.15g,收率为95%,称取碳酸铯(4.7g,14mmol)置于反应瓶(50mL),加入四氢呋喃(20mL)搅拌使溶解, 再加入异氰基乙酸乙酯(1.3g,11.5mmol;CAS No 2999?46?4)。冰水浴使体系温度降至0℃。 将步骤(3)所得2.15g糖浆状物溶于四氢呋喃(10mL),滴加入反应瓶,30分钟加入完毕,然后 室温反应4h。减压浓缩得棕色油状物,将此油状物以乙腈溶解,经0.24um滤膜过滤处理后高效液相法分析,收率为30.5%[1]。

图二 肌氨酸乙酯盐酸盐制备氟马西尼
[1]何新华,张学敏,周涛等. 一种氟马西尼的制备方法[P]. 浙江省:CN112979658B,2022-05-31.

|